Foscan คืออะไร?
Foscan เป็นสารละลายสำหรับฉีดที่มีสารออกฤทธิ์ temoporfin (1 หรือ 4 มก. / มล.)
Foscan ใช้ทำอะไร?
Foscan ใช้เพื่อบรรเทาอาการของมะเร็ง squamous cell carcinoma ระยะลุกลามของศีรษะและคอ (มะเร็งชนิดหนึ่งที่เริ่มต้นในเซลล์ที่เรียงกันในปาก จมูก คอ หรือหู) ในผู้ป่วยที่รักษาด้วยวิธีอื่นไม่ มีประสิทธิภาพนานกว่าและไม่เหมาะสำหรับการฉายรังสี (การรักษาด้วยรังสี) การผ่าตัดหรือเคมีบำบัดที่เป็นระบบ (ยาที่ใช้ในการรักษาโรคมะเร็ง "ระบบ" หมายความว่ายาเหล่านี้มีจุดมุ่งหมายเพื่อออกฤทธิ์กับทั้งร่างกาย)
สามารถรับยาได้เฉพาะเมื่อมีใบสั่งยาเท่านั้น
Foscan ใช้อย่างไร?
ควรให้ Foscan ในศูนย์ที่เชี่ยวชาญด้านการรักษามะเร็งเท่านั้น ซึ่งทีมสามารถประเมินการรักษาของผู้ป่วยได้ภายใต้การดูแลของแพทย์ผู้มีประสบการณ์ในการบำบัดด้วยแสง (การรักษาที่ใช้แสง) การรักษาด้วย Foscan เป็นกระบวนการสองขั้นตอน: ยาจะได้รับครั้งแรกและเปิดใช้งานโดยใช้เลเซอร์ ยาจะได้รับผ่านทางสายสวนทางหลอดเลือดดำถาวร (หลอดบาง ๆ สอดเข้าไปในหลอดเลือดดำอย่างถาวร) ในการฉีดช้าเพียงครั้งเดียวในระยะเวลาไม่น้อยกว่าหกนาที ปริมาณคือ 0.15 มก. ต่อกิโลกรัมของน้ำหนักตัว สี่วันต่อมา พื้นที่ทั้งหมดที่ได้รับผลกระทบจากเนื้องอกควรสว่างขึ้น โดยอยู่ห่างจากขอบโดยรอบไม่เกิน 0.5 ซม. ด้วยแสงที่สร้างจากแหล่งกำเนิดแสงเลเซอร์ที่ความยาวคลื่นเฉพาะประมาณ 3 นาที 20 วินาที โดยใช้สายไฟเบอร์ออปติก แต่ละพื้นที่ของเนื้อเยื่อเนื้องอกควรได้รับแสงสว่างเพียงครั้งเดียวในระหว่างการรักษาแต่ละครั้ง ในระหว่างการรักษา พื้นที่อื่น ๆ ของร่างกายควรได้รับการปกป้องจากแสงเพื่อให้ยาทำงานเฉพาะกับเนื้องอกเท่านั้น หากต้องการรอบที่สอง ควรทำอย่างน้อยสี่สัปดาห์
Foscan ทำงานอย่างไร?
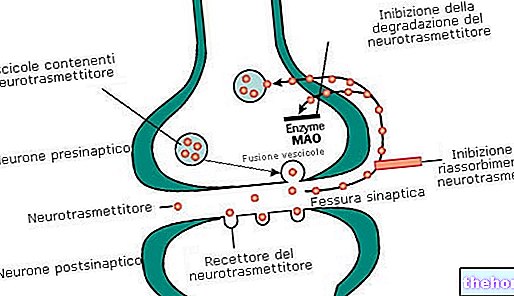
สารออกฤทธิ์ที่มีอยู่ใน Foscan, temoporfin เป็นสารไวแสง (สารที่เปลี่ยนแปลงเมื่อสัมผัสกับแสง) หลังจากฉีด Foscan แล้ว temoporfin จะกระจายไปทั่วร่างกาย รวมถึงมวลเนื้องอกด้วย เมื่อส่องสว่างด้วยแสงเลเซอร์ที่หนึ่ง
ความยาวคลื่นที่กำหนด temoporfin จะถูกกระตุ้นและทำปฏิกิริยากับออกซิเจนที่มีอยู่ในเซลล์ ทำให้เกิดออกซิเจนประเภทที่มีปฏิกิริยาและเป็นพิษสูง มันฆ่าเซลล์โดยทำปฏิกิริยากับส่วนประกอบ (โปรตีนและ DNA) และทำลายเซลล์เหล่านั้น โดยการจำกัดความสว่างของเนื้องอก เฉพาะเซลล์เนื้องอกเท่านั้นที่เสียหาย โดยไม่ส่งผลกระทบต่อส่วนอื่นของร่างกาย
Foscan ได้รับการศึกษาอย่างไร?
Foscan ได้รับการศึกษาในการศึกษาหลักสี่เรื่องที่เกี่ยวข้องกับผู้ป่วยมะเร็งศีรษะหรือคอทั้งหมด 409 ราย การศึกษาสามชิ้นแรกมีวัตถุประสงค์เพื่อตรวจสอบว่ามะเร็งหายจากการรักษาด้วย Foscan สูงสุด 3 หลักสูตรในผู้ป่วยทั้งหมด 189 รายหรือไม่ การศึกษาครั้งที่สี่มุ่งเน้นไปที่การลดอาการในผู้ป่วยมะเร็งศีรษะและคอระยะลุกลาม 220 รายที่ไม่สามารถผ่าตัดหรือฉายรังสีรักษาได้ ในการศึกษาทั้งหมด การตอบสนองต่อการรักษาได้รับการประเมินระหว่างสัปดาห์ที่ 12 และ 16 หลังจากรอบสุดท้ายด้วย Foscan อย่างไรก็ตาม Foscan ไม่ได้ถูกนำไปเปรียบเทียบกับยาอื่นใด
Foscan ได้แสดงให้เห็นประโยชน์อะไรบ้างในระหว่างการศึกษา?
ผลของการศึกษาสามครั้งแรกดูเหมือนจะไม่เพียงพอที่จะยืนยันประสิทธิภาพของ Foscan ในการกำจัดมะเร็งศีรษะและคอในทางกลับกัน ในการศึกษาที่ประเมินการปรับปรุงของอาการในผู้ป่วยมะเร็งศีรษะและคอระยะลุกลาม ผู้ป่วย 28 ราย (22%) จาก 128 คนที่สังเกตพบพบว่าอาการที่เป็นปัญหาดีขึ้นอย่างเห็นได้ชัด ขนาดของเนื้องอกลดลงยังพบในผู้ป่วยประมาณหนึ่งในสี่ที่เกี่ยวข้องกับการศึกษานี้
ความเสี่ยงที่เกี่ยวข้องกับ Foscan คืออะไร?
ผลข้างเคียงที่พบบ่อยที่สุดจาก Foscan (พบในผู้ป่วยมากกว่า 1 ใน 10 ราย) คือความเจ็บปวดที่บริเวณที่ฉีด ที่เนื้องอกหรือที่ใบหน้า เลือดออก แผลเป็น เนื้อร้ายในปาก (การตายของเซลล์หรือเนื้อเยื่อในปาก) , กลืนลำบาก (กลืนลำบาก), ใบหน้าบวมน้ำ (บวม) และท้องผูก สำหรับรายการผลข้างเคียงทั้งหมดที่รายงานด้วย Foscan โปรดดูที่แผ่นพับบรรจุภัณฑ์
ไม่ควรใช้ Foscan ในผู้ที่อาจแพ้ง่าย (แพ้) ต่อ temoporfin หรือส่วนผสมใดๆ ไม่ควรใช้ Foscan ในผู้ป่วยที่มี porphyria (ไม่สามารถเผาผลาญ porphyrins) โรคอื่น ๆ ที่กำเริบด้วยแสง อาการแพ้ porphyrin หรือเนื้องอกที่แพร่กระจายไปยังหลอดเลือดหรืออยู่ใกล้กับบริเวณที่มีแสงสว่าง จะต้องไม่ให้ Foscan แก่ผู้ป่วยที่จะรับการผ่าตัดภายใน 30 วันข้างหน้า, ให้กับผู้ป่วยโรคตาที่ต้องใช้การประเมิน "slit lamp" (เครื่องมือที่จักษุแพทย์ใช้ในการมองเข้าไปในดวงตา) "ตา) สำหรับ ในอีก 30 วันข้างหน้าหรือกับผู้ป่วยที่ได้รับการรักษาด้วยยาตัวอื่นที่เพิ่มความไวต่อแสงอยู่แล้ว
เป็นเวลาหกเดือนหลังการฉีด Foscan ผู้ป่วยควรหลีกเลี่ยงการสัมผัสกับแสงจ้าเพื่อหลีกเลี่ยงความเสี่ยงที่ผิวหนังจะไหม้ โปรดดูรายละเอียดเพิ่มเติมที่แผ่นพับบรรจุภัณฑ์
ทำไม Foscan ถึงได้รับการอนุมัติ?
คณะกรรมการผลิตภัณฑ์ยาเพื่อการใช้งานของมนุษย์ (CHMP) สรุปว่าผลของ Foscan ในการบรรเทาอาการที่เกี่ยวข้องกับมะเร็งศีรษะและคอระยะลุกลามเป็นที่น่าสังเกต ดังนั้น คณะกรรมการจึงตัดสินใจว่าประโยชน์ของ Foscan มากกว่าความเสี่ยงในการรักษาแบบประคับประคองของผู้ป่วย ด้วยมะเร็งเซลล์ squamous ขั้นสูงของศีรษะและคอที่ล้มเหลวในการรักษาก่อนหน้านี้และไม่เหมาะสำหรับการรักษาด้วยรังสี การผ่าตัด หรือเคมีบำบัดทั่วร่างกาย คณะกรรมการแนะนำให้ปล่อยการอนุญาตทางการตลาดสำหรับ Foscan
Foscan ได้รับอนุญาตในขั้นต้นภายใต้ "สถานการณ์พิเศษ" เพราะเนื่องจากโรคนี้หายากและด้วยเหตุผลทางวิทยาศาสตร์ข้อมูลจึงหายากในเวลาที่อนุญาต เนื่องจาก บริษัท ให้ข้อมูลเพิ่มเติมที่ร้องขอข้อ จำกัด ใน "สถานการณ์พิเศษ " ถูกเอาออกเมื่อ 21 พฤษภาคม 2008
ข้อมูลอื่น ๆ เกี่ยวกับ Foscan:
เมื่อวันที่ 24 ตุลาคม พ.ศ. 2544 คณะกรรมาธิการยุโรปได้ออก "การอนุญาตทางการตลาด" สำหรับ Foscan ซึ่งมีผลทั่วทั้งสหภาพยุโรป "การอนุญาตทางการตลาด" สำหรับ
ได้ต่ออายุการค้าเมื่อวันที่ 24 ตุลาคม พ.ศ. 2549 ผู้ได้รับอนุญาตทางการตลาดคือบริษัท Biolitec Pharma ltd.
สำหรับเวอร์ชันเต็มของ Foscan EPAR คลิกที่นี่
อัพเดทล่าสุดของสรุปนี้: 05-2008
ข้อมูลเกี่ยวกับ Foscan - temoporfin ที่เผยแพร่ในหน้านี้อาจล้าสมัยหรือไม่สมบูรณ์ สำหรับการใช้ข้อมูลนี้อย่างถูกต้อง โปรดดูที่หน้าข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์