ของแคลเซียมและกรดอนินทรีย์ เช่น กรดไนตริก กรดไฮโดรคลอริก หรือกรดซัลฟิวริก ด้านล่างนี้คือปฏิกิริยาเคมีที่เกี่ยวข้องกับการใช้กรดสุดท้ายนี้:
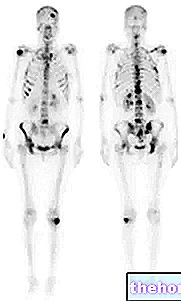
Ca3 (PO4) 2 + 3 H2SO4 → 3 CaSO4 + 2 H3PO4
ในทางกลับกัน กระบวนการทางความร้อนเกี่ยวข้องกับการรับฟอสฟอริกแอนไฮไดรด์โดยเริ่มจากฟอสฟอรัสธาตุ เมื่อก่อตัวขึ้นแล้ว แอนไฮไดรด์จะต้องถูกไฮเดรทจนกว่าจะได้กรดออร์โธฟอสฟอริก ดังที่แสดงไว้ในปฏิกิริยาต่อไปนี้:
P2O5 + 3 H2O → 2 H3PO4
กระบวนการหลังนี้โดยทั่วไปทำให้เกิดกรดออร์โธฟอสฟอริกที่บริสุทธิ์กว่ากระบวนการแบบเปียก
สิ่งแวดล้อมปรากฏเป็นของแข็งสีขาวที่ละลายที่อุณหภูมิประมาณ 42 องศาเซลเซียส
อย่างไรก็ตาม กรดฟอสฟอริกโดยทั่วไปจะวางตลาดในรูปของสารละลายในน้ำเข้มข้น 85% เป็นสารละลายที่ไม่มีสี ไม่มีกลิ่น และไม่ระเหย แต่มีฤทธิ์กัดกร่อนและมีความคงตัวของ "น้ำเชื่อม" ที่ค่อนข้างหนาแน่น
นอกจากจะละลายในน้ำแล้ว กรดออร์โธฟอสฟอริกยังละลายได้ในเอทานอล ไม่ระเบิดหรือติดไฟ แต่เนื่องจากการกัดกร่อนของกรดออร์โธฟอสฟอริกจึงต้องใช้ความระมัดระวังเป็นอย่างยิ่ง
เพื่อให้เกิดการยึดเกาะของวัสดุประสานสำหรับแคปซูล สะพาน วีเนียร์ อุดฟัน ฯลฯ ในบริบทนี้ กรดออร์โธฟอสฟอริกมักใช้ในสารละลาย 37%





.jpg)