สารออกฤทธิ์: เฟโลดิพีน
Prevex 5 มก. ยาเม็ดที่ออกฤทธิ์นาน
Prevex 10 มก. ยาเม็ดที่ออกฤทธิ์นาน
เหตุใดจึงใช้ Prevex? มีไว้เพื่ออะไร?
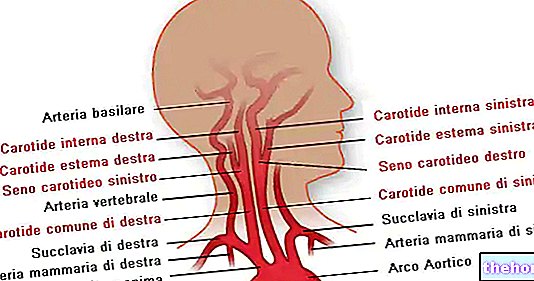
อนุพันธ์ไดไฮโดรไพริดีนที่มีฤทธิ์ลดความดันโลหิตและต้านหลอดเลือด
ความดันโลหิตสูง เจ็บหน้าอกที่มีเสถียรภาพ
ข้อห้าม เมื่อไม่ควรใช้ Prevex
การตั้งครรภ์; แพ้ที่รู้จักกับเฟโลดิพีนหรือสารเพิ่มปริมาณใด ๆ ; ภาวะหัวใจล้มเหลวที่ไม่ได้รับการชดเชย กล้ามเนื้อหัวใจตายเฉียบพลัน โรคหลอดเลือดหัวใจตีบที่ไม่เสถียร; การอุดตันของลิ้นหัวใจที่มีนัยสำคัญทางโลหิตวิทยา; การอุดตันแบบไดนามิกของการไหลออกของหัวใจ ช็อกจากโรคหัวใจ
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนใช้ Prevex
ยาเฟโลดิพีนอาจทำให้เกิดความดันเลือดต่ำได้อย่างมีนัยสำคัญ ส่งผลให้หัวใจเต้นเร็ว ซึ่งอาจทำให้กล้ามเนื้อหัวใจขาดเลือดในผู้ป่วยที่มีแนวโน้ม
ควรใช้ Felodipine ด้วยความระมัดระวังในผู้ป่วยที่มีแนวโน้มที่จะพัฒนาอิศวร
Felodipine ถูกกำจัดออกทางตับ ดังนั้น ความเข้มข้นในการรักษาที่สูงขึ้นและการตอบสนองที่เหนือกว่าสามารถคาดหวังได้ในผู้ป่วยที่มีการทำงานของตับลดลงอย่างชัดเจน (ดูเพิ่มเติมในส่วนปริมาณ วิธีและเวลาในการให้ยา)
มีรายงานผู้ป่วยที่เป็นโรคเหงือกอักเสบ / โรคปริทันต์อักเสบเล็กน้อย hyperplasia ดังกล่าวสามารถหลีกเลี่ยงหรือย้อนกลับได้โดย "การดูแลทันตกรรมอย่างระมัดระวัง
ปฏิกิริยา ยาหรืออาหารชนิดใดที่อาจเปลี่ยนผลของPrevex
ปฏิกิริยาของเอนไซม์
Felodipine ถูกเผาผลาญในตับโดย cytochrome P450 3A4 (CYP3A4) สารยับยั้งและสารกระตุ้น CYP3A4 อาจส่งผลต่อความเข้มข้นของยาเฟโลดิพีนในพลาสมา
ปฏิกิริยาที่ก่อให้เกิดการเพิ่มขึ้นของความเข้มข้นในพลาสมาของ felodipine
สารยับยั้งเอนไซม์ของ cytochrome P450 3A4 เช่น cimetidine, erythromycin, itraconazole, ketoconazole, anti-HIV / protease inhibitors (เช่น ritonavir) และ flavonoids บางชนิดที่มีอยู่ในน้ำเกรพฟรุตทำให้ความเข้มข้นของ felodipine ในพลาสมาเพิ่มขึ้น
ปฏิกิริยาที่ทำให้ความเข้มข้นของเอนไซม์ felodipine ในพลาสมาลดลงของ cytochrome P450 3A4 เช่น phenytoin, carbamazepine, rifampicin, barbiturates, efavirenz, nevirapine และ Hypericum Perforatum (St. John's wort) อาจทำให้ความเข้มข้นของ felodipine ในพลาสมาลดลง
ปฏิสัมพันธ์อื่นๆ
Ciclosporin: Felodipine ไม่ก่อให้เกิดการเปลี่ยนแปลงในความเข้มข้นของ cyclosporine ในพลาสมา
Tacrolimus: Felodipine อาจเพิ่มความเข้มข้นของ Tacrolimus เมื่อนำมารวมกัน ควรควบคุมความเข้มข้นของยาทาโครลิมัสในซีรัมและอาจต้องปรับขนาดยาทาโครลิมัส
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
พรีเว็กซ์มีแลคโตส ดังนั้นในกรณีที่ตรวจพบการแพ้น้ำตาล โปรดติดต่อแพทย์ก่อนรับประทานยา
ภาวะเจริญพันธุ์ การตั้งครรภ์ และให้นมบุตร
การตั้งครรภ์: ไม่ควรใช้ Prevex ในระหว่างตั้งครรภ์
การให้นมบุตร: ตรวจพบเฟโลดิพีนในน้ำนมแม่ อย่างไรก็ตาม หากมารดาใช้ยารักษาในขณะที่ให้นม ยานี้ไม่น่าจะส่งผลกระทบต่อทารก
การเจริญพันธุ์: ไม่มีข้อมูลเกี่ยวกับภาวะเจริญพันธุ์ของผู้ป่วย
ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
ผู้ป่วยควรทราบว่าพวกเขาตอบสนองต่อการรักษาด้วยยาเฟโลดิพีนอย่างไรก่อนขับรถหรือใช้เครื่องจักร เนื่องจากอาการวิงเวียนศีรษะหรือเหนื่อยล้าอาจเกิดขึ้นเป็นระยะๆ
ปริมาณและวิธีการใช้ วิธีใช้ Prevex: Dosage
ความดันโลหิตสูง
ควรปรับขนาดยาเป็นรายบุคคล
การรักษาสามารถเริ่มต้นด้วยขนาด 5 มก. วันละครั้ง เมื่อจำเป็น สามารถลดขนาดยาลงเหลือ 2.5 มก. หรือเพิ่มเป็น 10 มก. ต่อวัน ขึ้นอยู่กับการตอบสนองของผู้ป่วย หากจำเป็น สามารถเพิ่มยาลดความดันโลหิตชนิดอื่นได้
ปริมาณการบำรุงรักษาปกติคือ 5 มก. วันละครั้ง
การด้อยค่าของตับ
ผู้ป่วยที่เป็นโรคตับอาจมีความเข้มข้นของยาเฟโลดิพีนในพลาสมาสูง และอาจตอบสนองต่อการรักษาด้วยขนาดยาที่น้อยกว่า (ดูหัวข้อ ข้อควรระวังในการใช้งาน)
เจ็บหน้าอก
ควรปรับขนาดยาเป็นรายบุคคล
การรักษาควรเริ่มต้นด้วยขนาด 5 มก. วันละครั้ง และควรเพิ่มเป็น 10 มก. วันละครั้งตามความจำเป็น
การรักษาประชากรสูงอายุควรเริ่มต้นด้วยขนาดยาที่ต่ำที่สุด
การด้อยค่าของไต
ไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยที่มีความบกพร่องทางไต
ประชากรเด็ก
ประสบการณ์ที่ได้รับจากการทดลองทางคลินิกเกี่ยวกับการใช้เฟโลดิพีนในผู้ป่วยความดันโลหิตสูงในเด็กนั้นมีจำกัด
การบริหาร
ควรรับประทานยาเม็ดในตอนเช้า กลืนทั้งตัวด้วยน้ำ และไม่ควรหัก บด หรือเคี้ยว เพื่อรักษาคุณสมบัติการปลดปล่อยอย่างต่อเนื่อง ยาเม็ดสามารถรับประทานในขณะท้องว่างหรือหลังอาหารมื้อเบาที่มีไขมันหรือคาร์โบไฮเดรตต่ำ
ยาเกินขนาด จะทำอย่างไรถ้าคุณได้รับ Prevex มากเกินไป
อาการ: การให้ยาเกินขนาดอาจทำให้เกิดการขยายหลอดเลือดส่วนปลายมากเกินไป โดยมีอาการความดันเลือดต่ำและบางครั้งหัวใจเต้นช้า
การรักษา: ถ่านกัมมันต์ ถ้าจำเป็น ให้ล้างกระเพาะ
หากเกิดภาวะความดันเลือดต่ำอย่างรุนแรง ควรให้การรักษาตามอาการ
วางผู้ป่วยหงายโดยยกแขนขาล่างขึ้น
ในกรณีของภาวะหัวใจล้มเหลวร่วมด้วย ควรให้ atropine 0.5-1 มก. ทางหลอดเลือดดำ
หากยังไม่เพียงพอ ให้เพิ่มปริมาตรโดยผสมสารละลายทางสรีรวิทยา (น้ำเกลือ กลูโคส หรือเดกซ์แทรน) หากมาตรการที่อธิบายไว้ข้างต้นไม่เพียงพอ สามารถใช้ยาซิมพาโทมิเมติกที่มีผลเด่นต่อตัวรับ α1-adrenergic ได้
ผลข้างเคียง ผลข้างเคียงของ Prevex . คืออะไร
เฟโลดิพีนอาจทำให้หน้าแดง ปวดศีรษะ ใจสั่น เวียนศีรษะ อ่อนเพลีย
ปฏิกิริยาเหล่านี้ ซึ่งมักจะปรากฏขึ้นในช่วงเริ่มต้นของการรักษาหรือเมื่อเพิ่มขนาดยาที่ให้ โดยทั่วไปจะเกิดขึ้นชั่วคราวและค่อยๆ ลดความรุนแรงลงเมื่อเวลาผ่านไป
นอกจากนี้ เฟโลดิพีนยังสามารถทำให้เกิดอาการบวมน้ำที่ข้อเท้าโดยขึ้นกับขนาดยา ซึ่งเกิดจากการขยายหลอดเลือดในเส้นเลือดฝอยก่อนกำหนดและไม่เกี่ยวข้องกับการกักเก็บของเหลวโดยทั่วไป
จากประสบการณ์ที่ได้รับจากการศึกษาทางคลินิก 2% ของผู้ป่วยหยุดการรักษาเนื่องจากมีอาการบวมน้ำที่ข้อเท้า
มีการสังเกตการเกิด hyperplasia เหงือกเล็กน้อยในผู้ป่วยโรคเหงือกอักเสบ / โรคปริทันต์อักเสบที่เด่นชัด hyperplasia นี้สามารถหลีกเลี่ยงหรือรักษาด้วย "สุขอนามัยช่องปากอย่างระมัดระวัง นอกจากนี้ยังมีรายงานอาการคลื่นไส้, ปวดท้อง, ผื่น, อิศวร, ความดันเลือดต่ำ, เวียนศีรษะ, อาชา, อาการคัน, อาการอ่อนเปลี้ยเพลียแรง, อาการบวมน้ำที่ส่วนปลายมีรายงานเกี่ยวกับข้อเข่าเสื่อมและปวดกล้ามเนื้อ , ลมพิษ, อาเจียน, เป็นลม, กรณีของความอ่อนแอและความผิดปกติของทรงกลมทางเพศ .. ไม่ค่อยมีรายงานปฏิกิริยาภูมิไวเกิน (เช่น angioedema และไข้), เอนไซม์ตับเพิ่มขึ้น, ไวแสง, vasculitis เม็ดเลือดขาว, กระตุ้นให้ปัสสาวะบ่อย
การปฏิบัติตามคำแนะนำในเอกสารบรรจุภัณฑ์ช่วยลดความเสี่ยงของผลกระทบที่ไม่พึงประสงค์
สิ่งสำคัญคือต้องแจ้งให้แพทย์หรือเภสัชกรทราบถึงผลกระทบที่ไม่พึงประสงค์ แม้ว่าจะไม่ได้อธิบายไว้ในใบปลิวบรรจุภัณฑ์ก็ตาม
การหมดอายุและการเก็บรักษา
วันหมดอายุ: ดูวันหมดอายุที่พิมพ์บนบรรจุภัณฑ์
คำเตือน: อย่าใช้ยาหลังจากวันหมดอายุที่ระบุไว้บนบรรจุภัณฑ์ วันที่นี้หมายถึงบรรจุภัณฑ์ที่ไม่เสียหายและจัดเก็บไว้อย่างเหมาะสม
เก็บที่อุณหภูมิต่ำกว่า 30 องศาเซลเซียส
เก็บผลิตภัณฑ์ยาให้พ้นมือเด็ก
ข้อมูลอื่น ๆ
องค์ประกอบ
Prevex 5 มก. ยาเม็ดที่ออกฤทธิ์นาน
หนึ่งเม็ดที่ได้รับการปลดปล่อยเป็นเวลานานประกอบด้วย:
สารออกฤทธิ์: เฟโลดิพีน 5 มก.
Prevex 5 มก. เม็ดมีสีชมพู วงกลม สองด้าน สลัก "A / Fm" ที่ด้านหนึ่งและ "5" อีกด้านหนึ่ง เส้นผ่านศูนย์กลาง 9 มม.
สารเพิ่มปริมาณ: 40 น้ำมันละหุ่งพอลิออกซีเลตไฮโดรเจน; ไฮดรอกซีโพรพิลเซลลูโลส; โพรพิลแกลเลต; ไฮโปรเมลโลส; โซเดียมอลูมิเนียมซิลิเกต เซลลูโลส microcrystalline; ปราศจากแลคโตส; โซเดียมสเตียริลฟูมาเรต; โพลีเอทิลีนไกลคอล 6000; ไทเทเนียมไดออกไซด์ E171; เหล็กออกไซด์ E172; ขี้ผึ้ง carnauba; น้ำบริสุทธิ์
Prevex 10 มก. ยาเม็ดที่ออกฤทธิ์นาน
หนึ่งเม็ดที่ได้รับการปลดปล่อยเป็นเวลานานประกอบด้วย:
สารออกฤทธิ์: เฟโลดิพีน 10 มก.
Prevex 10 มก. เม็ดมีสีน้ำตาลแดง, วงกลม, สองด้าน, สลัก "A / FE" ที่ด้านหนึ่งและ "10" ที่อีกด้านหนึ่ง, เส้นผ่านศูนย์กลาง 9 มม.
สารเพิ่มปริมาณ: 40 น้ำมันละหุ่งพอลิออกซีเลตไฮโดรเจน; ไฮดรอกซีโพรพิลเซลลูโลส; โพรพิลแกลเลต; ไฮโปรเมลโลส; โซเดียมอลูมิเนียมซิลิเกต เซลลูโลส microcrystalline; ปราศจากแลคโตส; โซเดียมสเตียริลฟูมาเรต; โพลีเอทิลีนไกลคอล 6000; ไทเทเนียมไดออกไซด์ E171; เหล็กออกไซด์ E176; ขี้ผึ้ง carnauba; น้ำบริสุทธิ์
รูปแบบยาและเนื้อหา
ยาเม็ดที่ได้รับการปลดปล่อยเป็นเวลานาน Prevex 5 มก.:
28 เม็ดที่ได้รับการปลดปล่อยเป็นเวลานาน 5 มก.
Prevex 10 มก. แท็บเล็ตที่ปล่อยเป็นเวลานาน:
14 เม็ดที่ออกฤทธิ์นาน 10 มก.
28 เม็ดที่ออกฤทธิ์นาน 10 มก. - บรรจุภัณฑ์ที่ไม่ใช่เพื่อการตลาด
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่แสดงอาจไม่ทันสมัย
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
PREVEX
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
Prevex 5 มก. ยาเม็ดที่ออกฤทธิ์นาน
แต่ละเม็ดประกอบด้วย felodipine 5 มก.
สารเพิ่มปริมาณที่มีผลกระทบที่ทราบ:
แต่ละเม็ดประกอบด้วยแลคโตส 28 มก. และแมคโครกลีเซอรอลไฮดรอกซีสเตียเรต 5 มก.
Prevex 10 มก. ยาเม็ดที่ออกฤทธิ์นาน
แต่ละเม็ดประกอบด้วยเฟโลดิพีน 10 มก.
สารเพิ่มปริมาณที่มีผลกระทบที่ทราบ:
แต่ละเม็ดประกอบด้วยแลคโตส 28 มก. และแมคโครกลีเซอรอลไฮดรอกซีสเตียเรต 10 มก.
สำหรับรายการสารปรุงแต่งทั้งหมด โปรดดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
Prevex 5 มก. ยาเม็ดที่ออกฤทธิ์นาน
แท็บเล็ตเป็นสีชมพู กลม สองด้าน สลักด้วย A / Fm ด้านหนึ่งและด้านอื่น ๆ 5 ด้าน โดยมีเส้นผ่านศูนย์กลาง 9 มม.
Prevex 10 มก. ยาเม็ดที่ออกฤทธิ์นาน
แท็บเล็ตมีสีน้ำตาลแดง กลม สองด้าน สลัก A / FE ที่ด้านหนึ่งและ 10 อันที่อีกด้านหนึ่ง เส้นผ่านศูนย์กลาง 9 มม.
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
ความดันโลหิตสูง
เจ็บหน้าอกที่มีเสถียรภาพ
04.2 วิทยาและวิธีการบริหาร
ปริมาณ
ความดันโลหิตสูง
ควรปรับขนาดยาเป็นรายบุคคล การรักษาสามารถเริ่มต้นด้วยขนาด 5 มก. วันละครั้ง เมื่อจำเป็น สามารถลดขนาดยาลงเหลือ 2.5 มก. หรือเพิ่มเป็น 10 มก. ต่อวัน ขึ้นอยู่กับการตอบสนองของผู้ป่วย หากจำเป็น สามารถเพิ่มยาลดความดันโลหิตชนิดอื่นได้ ปริมาณการบำรุงรักษาปกติคือ 5 มก. วันละครั้ง
เจ็บหน้าอก
ควรปรับขนาดยาเป็นรายบุคคล การรักษาควรเริ่มต้นด้วยขนาด 5 มก. วันละครั้ง และหากจำเป็น ให้เพิ่มเป็น 10 มก. วันละครั้ง
ประชากรสูงอายุ
ควรพิจารณาการรักษาเบื้องต้นด้วยขนาดยาที่ต่ำที่สุด
การด้อยค่าของไต
ไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยที่มีความบกพร่องทางไต
การด้อยค่าของตับ
ผู้ป่วยที่เป็นโรคตับอาจมีความเข้มข้นของยาเฟโลดิพีนในพลาสมาสูงและอาจตอบสนองต่อการรักษาด้วยขนาดยาที่น้อยกว่า (ดูหัวข้อ 4.4)
ประชากรเด็ก
ประสบการณ์จากการทดลองทางคลินิกเกี่ยวกับการใช้เฟโลดิพีนในผู้ป่วยโรคความดันโลหิตสูงในเด็กมีจำกัด (ดูหัวข้อ 5.1 และ 5.2)
วิธีการบริหาร
ควรรับประทานยาเม็ดในตอนเช้าและกลืนด้วยน้ำ ไม่ควรแบ่งแท็บเล็ตบดหรือเคี้ยวเพื่อรักษาคุณสมบัติการปลดปล่อยเป็นเวลานาน สามารถรับประทานยาเม็ดโดยไม่มีอาหารหรือหลังอาหารมื้อเบาที่มีไขมันหรือคาร์โบไฮเดรตต่ำ
04.3 ข้อห้าม
• การตั้งครรภ์
• แพ้ยาเฟโลดิพีนหรือสารเพิ่มปริมาณที่ระบุในข้อ 6.1
• ภาวะหัวใจล้มเหลวที่ไม่ได้รับการชดเชย
• กล้ามเนื้อหัวใจตายเฉียบพลัน
• โรคหลอดเลือดหัวใจตีบที่ไม่เสถียร
• การอุดตันของลิ้นหัวใจที่มีนัยสำคัญทางโลหิตวิทยา
• การอุดตันแบบไดนามิกของการไหลออกของหัวใจ
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
ยังไม่มีการศึกษาประสิทธิภาพและความปลอดภัยของเฟโลดิพีนในการรักษาภาวะฉุกเฉินจากความดันโลหิตสูง
ยาเฟโลดิพีนอาจทำให้เกิดความดันเลือดต่ำได้อย่างมีนัยสำคัญ ส่งผลให้หัวใจเต้นเร็ว ซึ่งอาจทำให้กล้ามเนื้อหัวใจขาดเลือดในผู้ป่วยที่อ่อนแอได้
Felodipine ถูกกำจัดออกทางตับ ดังนั้น ความเข้มข้นในการรักษาที่สูงขึ้นและการตอบสนองที่เหนือกว่าสามารถคาดหวังได้ในผู้ป่วยที่มีการทำงานของตับลดลงอย่างชัดเจน (ดูหัวข้อ 4.2)
การใช้ผลิตภัณฑ์ยาร่วมกันซึ่งกระตุ้นหรือยับยั้งเอนไซม์ CYP3A4 อย่างมีนัยสำคัญส่งผลให้ระดับ felodipine ในพลาสมาลดลงหรือเพิ่มขึ้นตามลำดับ ดังนั้นควรหลีกเลี่ยงการบริหารร่วมกัน (ดูหัวข้อ 4.5)
Prevex มีแลคโตส ผู้ป่วยที่มีปัญหาทางพันธุกรรมที่หายากของการแพ้กาแลคโตสหรือการดูดซึมน้ำตาลกลูโคส - กาแลคโตส malabsorption ไม่ควรรับประทานยานี้
Prevex มีน้ำมันละหุ่งซึ่งอาจทำให้ปวดท้องและท้องร่วง
มีรายงานการขยายตัวของเหงือกที่ไม่รุนแรงในผู้ป่วยที่เป็นโรคเหงือกอักเสบ / โรคปริทันต์อักเสบ การขยายนี้สามารถหลีกเลี่ยงหรือย้อนกลับได้ด้วย "สุขอนามัยฟันอย่างระมัดระวัง
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
Felodipine ถูกเผาผลาญในตับโดย cytochrome P450 3A4 (CYP3A4) การใช้ยาร่วมกับสารที่รบกวนเอนไซม์ CYP3A4 อาจส่งผลต่อความเข้มข้นของยาเฟโลดิพีนในพลาสมา
ปฏิกิริยาของเอนไซม์
สารยับยั้งและตัวกระตุ้นของ cytochrome P450 isoenzyme 3A4 อาจส่งผลต่อความเข้มข้นของยา felodipine ในพลาสมา
ปฏิกิริยาที่ก่อให้เกิดการเพิ่มขึ้นของความเข้มข้นในพลาสมาของ felodipine
สารยับยั้งเอนไซม์ของเอนไซม์ CYP3A4 แสดงให้เห็นว่าทำให้ความเข้มข้นของเฟโลดิพีนในพลาสมาเพิ่มขึ้น
Felodipine Cmax และ AUC เพิ่มขึ้น 8 เท่าและ 6 เท่าตามลำดับเมื่อให้ felodipine ร่วมกับ itraconazole ตัวยับยั้ง CYP3A4 ที่มีศักยภาพ เมื่อให้ felodipine และ erythromycin ร่วมกัน felodipine Cmax และ AUC เพิ่มขึ้น ประมาณ 2.5 เท่า Cimetidine เพิ่ม felodipine Cmax และ AUC ประมาณ 55% ควรหลีกเลี่ยงการใช้ร่วมกับสารยับยั้ง CYP3A4 ที่มีศักยภาพ
ในกรณีของเหตุการณ์ไม่พึงประสงค์ที่มีนัยสำคัญทางคลินิกอันเนื่องมาจากการรับเฟโลดิพีนที่เพิ่มขึ้นเมื่อให้ร่วมกับสารยับยั้ง CYP3A4 ที่มีศักยภาพ ควรพิจารณาปรับขนาดยาเฟโลดิพีนและ / หรือการหยุดยายับยั้ง CYP3A4
ตัวอย่าง:
• ซิเมทิดีน
• อีริโทรมัยซิน
• ไอทราโคนาโซล
• คีโตโคนาโซล
• ยาต้านเอชไอวี / สารยับยั้งการเทียม (เช่น ริโทนาเวียร์)
• สารฟลาโวนอยด์บางชนิดที่มีอยู่ในน้ำเกรพฟรุต
ยาเม็ด Felodipine ไม่ควรรับประทานกับน้ำเกรพฟรุต
ปฏิกิริยาที่ทำให้ความเข้มข้นของยา felodipine ในพลาสมาลดลง
ตัวกระตุ้นเอนไซม์ของระบบ cytochrome P4503A4 แสดงให้เห็นว่าทำให้ความเข้มข้นของ felodipine ในพลาสมาลดลง
เมื่อให้ felodipine ร่วมกับ carbamazepine, phenytoin หรือ phenobarbital, felodipine Cmax และ AUC ลดลง 82% และ 96% ตามลำดับ ควรหลีกเลี่ยงการเชื่อมโยงกับตัวกระตุ้น CYP3A4 ที่มีศักยภาพ
ในกรณีที่ขาดประสิทธิภาพเนื่องจากการได้รับ felodipine ลดลง เมื่อให้ยากระตุ้น CYP3A4 ที่มีฤทธิ์ ควรพิจารณาปรับขนาดยา felodipine และ / หรือการหยุดยา CYP3A4 inducer
ตัวอย่าง:
• ฟีนิโทอิน
• คาร์บามาเซพีน
• ไรแฟมพิซิน
• บาร์บิทูเรตส์
• เอฟาวิเรนซ์
• เนวิราพีน
• Hypericum perforatum (สาโทเซนต์จอห์น)
ปฏิสัมพันธ์อื่นๆ
Tacrolimus: Felodipine อาจเพิ่มความเข้มข้นของ Tacrolimus เมื่อนำมารวมกัน ควรตรวจสอบความเข้มข้นของยาทาโครลิมัสในซีรัมและอาจจำเป็นต้องปรับขนาดยาทาโครลิมัส
Ciclosporin: Felodipine ไม่ก่อให้เกิดการเปลี่ยนแปลงในความเข้มข้นของ cyclosporine ในพลาสมา
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์
ไม่ควรใช้ Felodipine ในระหว่างตั้งครรภ์ มีรายงานการศึกษาเกี่ยวกับความเป็นพิษต่อระบบสืบพันธุ์ในพรีคลินิกเกี่ยวกับผลกระทบต่อพัฒนาการของทารกในครรภ์เนื่องจากการกระทำทางเภสัชวิทยาของเฟโลดิพีน
เวลาให้อาหาร
ตรวจพบเฟโลดิพีนในน้ำนมแม่ เนื่องจากไม่มีข้อมูลเกี่ยวกับผลกระทบที่อาจเกิดกับเด็กแรกเกิด จึงไม่แนะนำให้รักษาในระหว่างการให้นม
ภาวะเจริญพันธุ์
ไม่มีข้อมูลเกี่ยวกับผลของยาเฟโลดิพีนต่อภาวะเจริญพันธุ์ของผู้ป่วย ในการศึกษาพรีคลินิกเกี่ยวกับความเป็นพิษต่อระบบสืบพันธุ์ในหนูแรท (ดูหัวข้อ 5.3) ผลต่อพัฒนาการของทารกในครรภ์แต่ไม่มีผลกระทบต่อภาวะเจริญพันธุ์ในปริมาณที่ใกล้เคียงกับการรักษา
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
เฟโลดิพีนมีผลเล็กน้อยหรือปานกลางต่อความสามารถในการขับหรือใช้เครื่องจักร หากผู้ป่วยที่ใช้ยาเฟโลดิพีนมีอาการปวดศีรษะ คลื่นไส้ เวียนศีรษะ หรือเหนื่อยล้า ความสามารถในการตอบสนองอาจลดลง ขอแนะนำให้ใช้ความระมัดระวังเป็นพิเศษเมื่อเริ่มการรักษา
04.8 ผลกระทบที่ไม่พึงประสงค์
สรุปข้อมูลความปลอดภัย
เฟโลดิพีนอาจทำให้หน้าแดง ปวดศีรษะ ใจสั่น วิงเวียนศีรษะ และเมื่อยล้า ปฏิกิริยาเหล่านี้ส่วนใหญ่ขึ้นอยู่กับขนาดยาและปรากฏขึ้นในช่วงเริ่มต้นของการรักษาหรือหลังจากเพิ่มขนาดยา หากเกิดขึ้น ปฏิกิริยาเหล่านี้มักจะเกิดขึ้นชั่วคราวและลดลงเมื่อเวลาผ่านไป
ผู้ป่วยที่ได้รับยาเฟโลดิพีนอาจพบอาการบวมน้ำที่ข้อเท้าโดยขึ้นกับขนาดยา นี่เป็นเพราะการขยายหลอดเลือดในเส้นเลือดฝอยก่อนกำหนดและไม่เกี่ยวข้องกับการกักเก็บน้ำโดยทั่วไป
มีรายงานการขยายตัวของเหงือกที่ไม่รุนแรงในผู้ป่วยที่เป็นโรคเหงือกอักเสบ / โรคปริทันต์อักเสบ การขยายนี้สามารถหลีกเลี่ยงหรือย้อนกลับได้ด้วย "สุขอนามัยฟันอย่างระมัดระวัง
ตารางอาการไม่พึงประสงค์
อาการข้างเคียงที่แสดงด้านล่างได้รับการระบุในระหว่างการทดลองทางคลินิกและในระยะหลังการขาย
ใช้คำจำกัดความความถี่ต่อไปนี้:
พบบ่อยมาก ≥1 / 10
ทั่วไป ≥1 / 100,
ผิดปกติ ≥1 / 1,000,
หายาก ≥1 / 10,000,
หายากมาก
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านระบบการรายงานระดับประเทศ "ที่อยู่ www. agenziafarmaco.gov.it/it/responsabili.
04.9 ใช้ยาเกินขนาด
อาการ
การให้ยาเกินขนาดอาจทำให้เกิดการขยายหลอดเลือดส่วนปลายมากเกินไป โดยมีอาการความดันเลือดต่ำและบางครั้งหัวใจเต้นช้า
การรักษา ถ้ามีเหตุผล: ถ่านกัมมันต์จากพืช ล้างกระเพาะอาหารหากดำเนินการภายในหนึ่งชั่วโมงหลังการกลืนกิน
หากเกิดภาวะความดันเลือดต่ำอย่างรุนแรง ควรให้การรักษาตามอาการ
ผู้ป่วยควรอยู่ในตำแหน่งหงายโดยยกขาขึ้น ในกรณีของภาวะหัวใจล้มเหลวร่วมด้วย ควรให้ atropine 0.5-1 มก. ทางหลอดเลือดดำ หากไม่เพียงพอ ควรเพิ่มปริมาณเลือดโดยการให้ยาเช่น กลูโคส น้ำเกลือ หรือเดกซ์ทราน)
หากมาตรการที่อธิบายไว้ข้างต้นไม่เพียงพอ สามารถให้ยา sympathomimetic ที่มีผลเหนือกว่า adrenergic receptors ได้หรือไม่?
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มเภสัชบำบัด: ตัวบล็อกช่องแคลเซียม, อนุพันธ์ไดไฮโดรไพริดีน
รหัส ATC: C08CA02
กลไกการออกฤทธิ์
Felodipine เป็นตัวป้องกันแคลเซียมแชนเนลของหลอดเลือดที่คัดเลือกมาอย่างดี ซึ่งช่วยลดความดันโลหิตโดยการลดความต้านทานของหลอดเลือดทั้งระบบ เนื่องจากเฟโลดิพีนมีความสามารถในการคัดเลือกกล้ามเนื้อเรียบของหลอดเลือดในระดับสูง ในปริมาณที่ใช้ในการรักษาจึงไม่มีผลโดยตรงต่อการหดตัวและการนำของหัวใจ
เนื่องจากไม่มีผลต่อกล้ามเนื้อเรียบของผนังหลอดเลือดดำหรือการควบคุมการหลั่งของหลอดเลือด ดังนั้นยาเฟโลดิพีนจึงไม่สัมพันธ์กับความดันเลือดต่ำแบบมีพยาธิสภาพ
เฟโลดิพีนมีฤทธิ์เป็นยาขับปัสสาวะ / ขับปัสสาวะที่ไม่รุนแรงและไม่ก่อให้เกิดการกักเก็บน้ำ
ผลกระทบทางเภสัชพลศาสตร์
Felodipine มีประสิทธิภาพในทุกขั้นตอนของความดันโลหิตสูง สามารถใช้ได้ทั้งแบบเดี่ยวและร่วมกับยาลดความดันโลหิตอื่นๆ เช่น beta-blockers ยาขับปัสสาวะ หรือ ACE inhibitors เพื่อให้ได้ผลลดความดันโลหิตที่มากขึ้น Felodipine มีประสิทธิภาพในการลดทั้งความดันโลหิตซิสโตลิก (PAS) และความดันโลหิตตัวล่าง (PAD) และสามารถใช้ในการรักษาความดันโลหิตสูงซิสโตลิกแบบแยกเดี่ยว
เฟโลดิพีนมีฤทธิ์ต้านหลอดเลือดและต้านภาวะขาดเลือดเนื่องจากการปรับปรุงสมดุลของอุปทาน/อุปสงค์ของออกซิเจน การลดลงของความต้านทานของหลอดเลือดหัวใจและการเพิ่มขึ้นของการไหลของหลอดเลือดและการจัดหาออกซิเจนโดย felodipine เกิดจากการขยายของหลอดเลือดแดง epicardial และ arterioles
การลดลงของความดันโลหิตในระบบที่เกิดจากยาเฟโลดิพีนทำให้มีหัวใจห้องล่างซ้ายลดลงและความต้องการออกซิเจนในกล้ามเนื้อหัวใจลดลง
Felodipine ช่วยเพิ่มความทนทานต่อการออกกำลังกายและลดการโจมตีของ angina ในผู้ป่วยที่มี angina pectoris ที่ออกแรงอย่างมีเสถียรภาพ Felodipine สามารถใช้คนเดียวหรือใช้ร่วมกับ beta blocker ในผู้ป่วยที่เป็นโรคหลอดเลือดหัวใจตีบที่มีเสถียรภาพ
เอฟเฟกต์การไหลเวียนโลหิต
ผลทางโลหิตวิทยาเบื้องต้นของยาเฟโลดิพีนคือการลดความต้านทานของหลอดเลือดส่วนปลายทั้งหมด ส่งผลให้ความดันโลหิตลดลง ผลกระทบเหล่านี้ขึ้นอยู่กับขนาดยา โดยทั่วไป ความดันโลหิตจะลดลงสองชั่วโมงหลังจากให้ยาครั้งแรกและการลดลงนี้ยังคงมีอยู่ เป็นเวลาอย่างน้อย 24 ชั่วโมง โดยมีอัตราส่วนหุบเขา/ยอดสูงสุดมากกว่า 50%
ความเข้มข้นของเฟโลดิพีนในพลาสมามีความสัมพันธ์โดยตรงกับการลดความต้านทานของหลอดเลือดส่วนปลายและความดันโลหิต
ผลต่อหัวใจ
ในปริมาณที่ใช้ในการรักษา เฟโลดิพีนไม่มีผลต่อการหดตัวของหัวใจ การนำ atrioventricular หรือการหักเหของแสง
การรักษาด้วยยาลดความดันโลหิตด้วยยาเฟโลดิพีนสัมพันธ์กับการถดถอยอย่างมีนัยสำคัญของภาวะหลอดเลือดหัวใจตีบซ้ายที่มีอยู่ก่อน
ผลกระทบของไต
เฟโลดิพีนมีฤทธิ์ขับปัสสาวะและขับปัสสาวะเนื่องจากการลดการดูดซึมซ้ำของโซเดียมที่กรองในท่อ เฟโลดิพีนไม่ได้แก้ไขการขับโพแทสเซียมในแต่ละวัน ยาเฟโลดิพีน ดื้อต่อหลอดเลือดในไตลดลง
Felodipine ไม่ส่งผลต่อการขับอัลบูมินในปัสสาวะ
ในผู้ป่วยที่รักษาด้วย cyclosporine หลังการปลูกถ่ายไต felodipine ช่วยลดความดันโลหิต เพิ่มการไหลเวียนของเลือดในไต และอัตราการกรองไต เฟโลดิพีนยังสามารถปรับปรุงการทำงานของไตที่ปลูกถ่ายได้ตั้งแต่เนิ่นๆ
ประสิทธิภาพทางคลินิก
ในการทดลองทางคลินิก HOT (Hypertension Optimal Optimal Treatment) กับเฟโลดิพีนเป็นการรักษาเบื้องหลัง ความสัมพันธ์ระหว่างเหตุการณ์หัวใจและหลอดเลือดที่สำคัญ (เช่น กล้ามเนื้อหัวใจตายเฉียบพลัน โรคหลอดเลือดสมองและการเสียชีวิตจากสาเหตุโรคหัวใจและหลอดเลือด) และระดับความดันโลหิตไดแอสโตลิกเป้าหมาย 3 ระดับ ≤90 ได้รับการตรวจสอบ mmHg, ≤ 85 mmHg และ ≤80 mmHg และความดันโลหิตที่ได้รับจากยาเฟโลดิพีน
ผู้ป่วยความดันโลหิตสูงจำนวน 18,790 ราย (PAD 100-115 mmHg) ที่มีอายุระหว่าง 50 ถึง 80 ปีได้รับการติดตามเป็นระยะเวลาเฉลี่ย 3.8 ปี (ช่วง 3.3-4.9) Felodipine ได้รับเป็นยาเดี่ยวหรือใช้ร่วมกับ beta blocker และ / หรือ ACE inhibitor และ / หรือยาขับปัสสาวะ การศึกษาแสดงให้เห็นประโยชน์ของการลด PAS และ PAD ถึงระดับ 139 และ 83 mmHg ตามลำดับ
จากการศึกษา STOP-2 (Swedish Trial in Old Patients with Hypertension-2 study) ที่ดำเนินการในผู้ป่วย 6614 รายที่มีอายุระหว่าง 70 ถึง 84 ปี พบว่าแคลเซียมคู่อริในกลุ่ม dihydropyridine (felodipine และ isradipine) แสดงผลการป้องกันแบบเดียวกัน และการเจ็บป่วยของยาลดความดันโลหิตประเภทอื่นที่ใช้กันทั่วไป เช่น ยายับยั้ง ACE ยาเบต้าบล็อกเกอร์ และยาขับปัสสาวะ
ประชากรเด็ก
ประสบการณ์ทางคลินิกของการใช้เฟโลดิพีนในผู้ป่วยเด็กโรคความดันโลหิตสูงมีจำกัด ในการศึกษาแบบ randomized, double-blind, parallel-group, สามสัปดาห์ในเด็กอายุ 6 ถึง 16 ปีที่มีความดันโลหิตสูงขั้นต้น, ฤทธิ์ลดความดันโลหิตของ felodipine 2.5 มก. (n = 33), 5 มก. (n = 33) และ 10 มก. (n = 31) ที่ให้ยาวันละครั้งเปรียบเทียบกับยาหลอก (n = 35) การศึกษาล้มเหลวในการแสดงประสิทธิภาพของยาเฟโลดิพีนในการลดความดันโลหิตในเด็กอายุ 6 และ 16 ปี (ดูหัวข้อ 4.2)
ยังไม่มีการศึกษาผลกระทบระยะยาวของเฟโลดิพีนต่อการเจริญเติบโต วัยแรกรุ่น และการพัฒนาทั่วไป นอกจากนี้ ยังไม่มีการกำหนดประสิทธิภาพของการรักษาด้วยยาลดความดันโลหิตระยะยาวของเฟโลดิพีนในการรักษาด้วยยาเฟโลดิพีนในวัยเด็กเพื่อลดการเจ็บป่วยจากโรคหัวใจและหลอดเลือดและอัตราการเสียชีวิตในวัยผู้ใหญ่
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
การดูดซึม
หลังจากได้รับยาเม็ดที่ได้รับการปลดปล่อยเป็นเวลานานแล้ว felodipine จะถูกดูดซึมจากทางเดินอาหารได้อย่างสมบูรณ์ การดูดซึมทางระบบของเฟโลดิพีนอยู่ที่ประมาณ 15% และเป็นอิสระจากขนาดยาตลอดช่วงการรักษา
ยาเม็ดที่ได้รับการปลดปล่อยเป็นเวลานานส่งผลให้ felodipine ดูดซึมเป็นเวลานาน ส่งผลให้มีเส้นโค้งความเข้มข้นในพลาสมาที่สม่ำเสมอและความเข้มข้นในการรักษายังคงมีอยู่ 24 ชั่วโมงหลังการให้ยา ความเข้มข้นในพลาสมาสูงสุด (tmax) ที่มีรูปแบบการปลดปล่อยเป็นเวลานานจะถึงหลังจาก 3-5 ชั่วโมง อัตราแต่ไม่ถึงขอบเขตของการดูดซึมเฟโลดิพีนจะเพิ่มขึ้นเมื่อรับประทานอาหารที่มีไขมันสูง
การกระจาย
การจับโปรตีนในพลาสมาอยู่ที่ประมาณ 99% ส่วนใหญ่มีส่วนของอัลบูมิน ปริมาณการกระจายที่สภาวะคงตัวคือ 10 L / kg
การเปลี่ยนแปลงทางชีวภาพ
Felodipine ถูกเผาผลาญอย่างกว้างขวางในตับโดย cytochrome P450 3A4 (CYP3A4) และสารที่ระบุทั้งหมดจะไม่ทำงาน
Felodipine เป็นผลิตภัณฑ์ยาที่มีอัตราการกวาดล้างสูง ค่าเฉลี่ยการกวาดล้างเลือดคือ 1200 มล. / นาที ไม่มีการสะสมอย่างมีนัยสำคัญในระหว่างการรักษาเป็นเวลานาน
ผู้ป่วยสูงอายุและผู้ที่มีการทำงานของตับบกพร่องมีความเข้มข้นของยา felodipine ในพลาสมาสูงกว่าผู้ป่วยที่อายุน้อยกว่า เภสัชจลนศาสตร์ของเฟโลดิพีนไม่เปลี่ยนแปลงในผู้ป่วยที่มีความบกพร่องทางไต รวมถึงการฟอกไต
การกำจัด
ค่าครึ่งชีวิตในการกำจัดเฟโลดิพีนเฉลี่ยอยู่ที่ประมาณ 25 ชั่วโมงและถึงสภาวะคงตัวหลังจาก 5 วัน ในระหว่างการรักษาเป็นเวลานานจะไม่มีความเสี่ยงต่อการสะสม ประมาณ 70% ของขนาดยาจะถูกขับออกมาในรูปของสารเมตาโบไลต์ในปัสสาวะ ส่วนที่เหลือจะถูกขับออกทางอุจจาระ
พบว่าน้อยกว่า 0.5% ของขนาดยาที่ให้มาไม่เปลี่ยนแปลงในปัสสาวะ
ความเป็นลิเนียร์ / ความไม่เป็นเชิงเส้น
ความเข้มข้นในพลาสมาเป็นสัดส่วนโดยตรงกับขนาดยาที่อยู่ในช่วงการรักษา 2.5-10 มก.
ประชากรเด็ก
ในการศึกษาเภสัชจลนศาสตร์ในขนาดเดียว (ยาเฟโลดิพีนแบบขยายระยะเวลา 5 มก.) กับเด็กอายุ 6 ถึง 16 ปีจำนวนจำกัด (n = 12) ไม่มีความสัมพันธ์ที่ชัดเจนระหว่างอายุและ AUC, C felodipine
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ความเป็นพิษต่อระบบสืบพันธุ์
ในการศึกษาภาวะเจริญพันธุ์และสมรรถภาพการเจริญพันธุ์โดยทั่วไปในหนูที่ได้รับการรักษาด้วย felodipine การยืดเวลาการคลอดซึ่งนำไปสู่ความยากลำบากในการคลอดบุตรพบได้ในกลุ่มที่ได้รับยาขนาดปานกลางและขนาดสูง การเสียชีวิตของทารกในครรภ์เพิ่มขึ้นและการเสียชีวิตหลังคลอดก่อนกำหนด ผลกระทบเหล่านี้เป็นผลมาจากการยับยั้งการหดตัวของมดลูกของ felodipine ในปริมาณที่สูง ไม่มีผลต่อภาวะเจริญพันธุ์เมื่อให้หนูที่ได้รับยาในช่วงการรักษา
การศึกษาการสืบพันธุ์ในกระต่ายได้แสดงให้เห็นการขยายตัวของต่อมน้ำนมในมารดาที่เกี่ยวข้องกับขนาดยาและสามารถย้อนกลับได้ และความผิดปกติทางดิจิทัลที่เกี่ยวข้องกับปริมาณยาในทารกในครรภ์ พบความผิดปกติเหล่านี้เมื่อให้เฟโลดิพีนในช่วงแรกของการพัฒนาของทารกในครรภ์ (ก่อนวันที่ 15 ของการตั้งครรภ์) พบตำแหน่งที่ผิดปกติของพรรคพวกส่วนปลายในการศึกษาการสืบพันธุ์ของลิง
ไม่มีข้อกังวลใดๆ ในการตรวจพรีคลินิกและผลการสืบพันธุ์ได้รับการพิจารณาว่าเกี่ยวข้องกับผลทางเภสัชวิทยาของยาเฟโลดิพีนเมื่อให้ยา felodipine กับสัตว์ควบคุมปริมาณปกติ ไม่ทราบความเกี่ยวข้องทางคลินิกของข้อค้นพบเหล่านี้สำหรับผู้ป่วยที่ได้รับยาเฟโลดิพีน อย่างไรก็ตาม จากผลการวิจัยพบว่า ข้อมูลฐานข้อมูลเพื่อความปลอดภัยของผู้ป่วย ไม่มีรายงานกรณีความผิดปกติของพรรคในทารกในครรภ์/ทารกแรกเกิดที่ได้รับยาเฟโลดิพีนในครรภ์
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
แกนหลักของแท็บเล็ต
ไฮดรอกซีโพรพิลเซลลูโลส
ไฮโปรเมลโลส 50 mPa • s
ไฮโปรเมลโลส 10,000 mPa • s
ปราศจากแลคโตส
แมคโครกอลกลีเซอรอล ไฮดรอกซีสเตียเรต
ไมโครคริสตัลลีน เซลลูโลส
โพรพิลแกลเลต
โซเดียมอลูมิเนียมซิลิเกต
โซเดียม สเตียริล ฟูมาเรต
การเคลือบผิว
คาร์นูบาแว็กซ์
เหล็กออกไซด์สีน้ำตาลแดง (E 172)
เหล็กออกไซด์สีเหลือง (E 172)
ไฮโปรเมลโลส 6 mPa • s
Macrogol 6000
ไทเทเนียมไดออกไซด์ (E 171)
06.2 ความเข้ากันไม่ได้
ไม่เกี่ยวข้อง
06.3 ระยะเวลาที่มีผลบังคับใช้
3 ปี
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
อย่าเก็บที่อุณหภูมิสูงกว่า 30 ° C
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
PVC / PVDC หรือตุ่มอลูมิเนียม
Prevex 5 มก. ยาเม็ดที่ออกฤทธิ์นาน
ขนาดบรรจุ : 1 เม็ด 28 เม็ด หรือ 2 เม็ด 14 เม็ด หรือ 4 เม็ด 7 เม็ด
Prevex 10 มก. ยาเม็ดที่ออกฤทธิ์นาน
ขนาดบรรจุ : 1 เม็ด 14 เม็ด หรือ 1 เม็ด 28 เม็ด หรือ 2 เม็ด 14 เม็ด หรือ 4 เม็ด 7 เม็ด
ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
06.6 คำแนะนำในการใช้งานและการจัดการ
ยาที่ไม่ได้ใช้และของเสียที่ได้จากยานี้ต้องกำจัดตามระเบียบข้อบังคับของท้องถิ่น
07.0 ผู้ทรงอำนาจการตลาด
ไซเมซ่า เอส.พี.เอ.
พระราชวังเฟอร์รารี
Via Ludovico il Moro 6 / C - Basiglio (MI)
08.0 หมายเลขอนุญาตการตลาด
027372010 "5 MG EXTENDED RABLETS" 28 เม็ด
027372022 "10 MG EXTENDED RABLETS" 14 เม็ด
027372034 "10 MG EXTENDED RABLETS" 28 เม็ด
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
วันที่ได้รับอนุญาตครั้งแรก: 17 ธันวาคม 1991
วันที่ต่ออายุครั้งล่าสุด: 2 มกราคม 2550
10.0 วันที่แก้ไขข้อความ
17 มิถุนายน 2017