สารออกฤทธิ์: Alfacalcidol
DERIL 1.0 mcg แคปซูล
เหตุใดจึงใช้เดอริล? มีไว้เพื่ออะไร?
วิตามิน: Alfacalcidol เมแทบอไลต์ของวิตามินดี
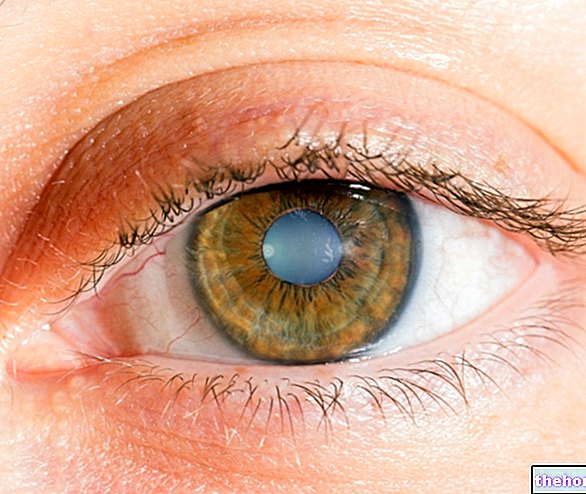
ภาวะไตวาย osteodystrophy เมื่อฟอกไตหรือไม่ ภาวะพร่องพาราไทรอยด์ โรคกระดูกอ่อนที่ดื้อต่อ D หรือขึ้นอยู่กับ D (ขาดหลอก) และโรคกระดูกพรุนRickets และ osteomalacia เนื่องจากการเปลี่ยนแปลงของไตเนื่องจากการเผาผลาญของวิตามินดี โรคกระดูกพรุนในวัยหมดประจำเดือน
ข้อห้าม เมื่อไม่ควรใช้ Derill
ภาวะแคลเซียมในเลือดสูง ไม่ควรให้ผลิตภัณฑ์ระหว่างตั้งครรภ์และให้นมบุตร บุคคล แพ้วิตามินดีหรือส่วนประกอบอื่น ๆ ของผลิตภัณฑ์
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนรับประทานเดอริล
เนื่องจากการใช้ยา DERIL เกินขนาดสามารถทำให้เกิดภาวะแคลเซียมในเลือดสูงได้ และในบางกรณี แคลเซียมในปัสสาวะสูงควรให้แคลเซียมอย่างน้อยสัปดาห์ละ 2 ครั้งในช่วงการปรับขนาดยา เมื่อกำหนดขนาดยาที่เหมาะสมในแต่ละวันแล้ว การควบคุมระดับแคลเซียมทุกเดือนก็เพียงพอแล้ว ของ อัลคาไลน์ฟอสฟาเตสโดยทั่วไปคาดว่าจะเริ่มมีอาการของภาวะแคลเซียมในเลือดสูง ดังนั้นจึงอาจเป็นอาการผิดปกติในระยะหลังได้
หากภาวะแคลเซียมในเลือดสูงเกิดขึ้น ควรหยุดยาและอาหารเสริมแคลเซียมใดๆ ชั่วคราวจนกว่าแคลเซียมในเลือดจะกลับเข้าสู่สภาวะปกติอย่างรวดเร็ว จากนั้นจึงค่อยเริ่มการรักษาต่อในขนาดที่ต่ำกว่า
ควรให้ DERIL ด้วยความระมัดระวังในผู้ป่วยที่ได้รับการรักษาด้วย digitalis เนื่องจากภาวะน้ำตาลในเลือดต่ำอาจทำให้ภาวะหัวใจเต้นผิดจังหวะรุนแรงขึ้นในผู้ป่วยรายดังกล่าว เนื่องจาก DERIL มีอิทธิพลต่อการขนส่งฟอสเฟตในลำไส้ ไต และกระดูก การใช้สารตรึงฟอสฟอรัสร่วมกันจึงต้องปรับให้เข้ากับค่าของฟอสเฟต (อัตราปกติ: 2-5 มก. / 100 มล.)
การตั้งครรภ์และให้นมบุตร
ไม่ควรให้ผลิตภัณฑ์ระหว่างตั้งครรภ์และให้นมบุตร
ปฏิกิริยา ยาหรืออาหารชนิดใดที่สามารถปรับเปลี่ยนฤทธิ์เดริลได้
การใช้ยากันชักพร้อม ๆ กันที่มีคุณสมบัติในการเหนี่ยวนำของเอนไซม์ (barbiturates, diphenylhydantoin) อาจทำให้การตอบสนองของ Alfacalcidol ลดลงโดยจำเป็นต้องเพิ่มปริมาณการใช้สารเตรียมที่มีอลูมิเนียมมากเกินไปอาจรบกวนประสิทธิภาพของยาได้ การศึกษาในสัตว์ทดลองได้ชี้ให้เห็นถึงศักยภาพที่เป็นไปได้ของการกระทำของวาร์ฟารินเมื่อให้ calciferol แม้ว่าจะไม่มีหลักฐานที่คล้ายคลึงกันกับการใช้ Alfacalcidol แต่ควรใช้ความระมัดระวังเมื่อใช้ยาทั้งสองพร้อมกัน ไม่ควรใช้ยาที่มีแมกนีเซียม ในระหว่างการรักษาด้วย DERIL เพื่อหลีกเลี่ยงการเกิดภาวะ hypermagnesaemia Colestyramine สามารถลดการดูดซึมวิตามินที่ละลายในไขมันในลำไส้และ DERIL ด้วย
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
เนื่องจาก Alfacalcidol เป็นสารตั้งต้นของสารออกฤทธิ์ของวิตามิน D3 ไม่ควรให้วิตามินดีและอนุพันธ์ของมันในระหว่างการรักษาด้วย DERIL การใช้ยาเกินขนาดของวิตามินดีในรูปแบบใด ๆ ทำให้เกิดอาการรุนแรงได้ แคลเซียมในเลือดสูงที่เกิดจากปริมาณวิตามินดีในปริมาณที่มากเกินไปหรือสารเมตาโบไลต์ของวิตามินดีอาจต้องได้รับการรักษาฉุกเฉิน แคลเซียมในเลือดสูงหากเป็นเรื้อรังจริง ๆ แล้วอาจทำให้เกิดการกลายเป็นปูนในหลอดเลือดโดยทั่วไป ภาวะแคลเซียมในไต และการกลายเป็นปูนของเนื้อเยื่ออ่อนอื่น ๆ ดังนั้นจึงจำเป็นต้องตรวจสอบให้แน่ใจว่าตัวเลขที่ได้จากการคูณค่าแคลเซียมด้วยค่าฟอสเฟตเมีย (Ca x P) ไม่เกิน 70 .
การตรวจด้วยภาพรังสีของบริเวณกายวิภาคซึ่งเป็นที่ตั้งของการกลายเป็นปูนอาจเป็นประโยชน์สำหรับการวินิจฉัยโรคในระยะเริ่มแรก DERIL ไม่มีผลต่อการใช้เครื่องจักรและความสามารถในการขับขี่
ปริมาณและวิธีการใช้ วิธีการใช้ Deril: Dosage
ปริมาณที่แนะนำเริ่มต้นสำหรับการบ่งชี้ทั้งหมด: ผู้ใหญ่และเด็กที่มีน้ำหนักเกิน 20 กก.: 1 ไมโครกรัมต่อวัน เด็กที่มีน้ำหนักต่ำกว่า 20 กก.: 0.05 ไมโครกรัม / กก. / วัน หลังจากนั้นสามารถปรับขนาดยาได้ตามการตอบสนอง
ยาเกินขนาด จะทำอย่างไรถ้าคุณได้รับ Deril มากเกินไป
ในกรณีของภาวะแคลเซียมในเลือดสูงอย่างรุนแรงเนื่องจากการให้ยาเกินขนาดโดยไม่ได้ตั้งใจ หลังจากหยุดยาชั่วคราวแล้ว สามารถให้ยาขับปัสสาวะร่วมกับของเหลวทางหลอดเลือดดำหรือคอร์ติโคสเตียรอยด์
ผลข้างเคียง ผลข้างเคียงของแดริลคืออะไร?
หากขนาดยาเป็นไปตามความต้องการที่แท้จริงของแต่ละบุคคล DERIL สามารถทนต่อยาได้ดี มิฉะนั้น เนื่องจากผลิตภัณฑ์มีกิจกรรม D-vitamin ผลข้างเคียงอาจปรากฏขึ้นซึ่งคล้ายกับของ hypervitaminosis D เช่น hypercalcemic syndrome หรืออาการที่เป็นพิษของแคลเซียม (ขึ้นอยู่กับความรุนแรงและระยะเวลาของ hypercalcemia) อาการเหล่านี้มีทั้ง เฉียบพลันและเรื้อรัง
อดีต ได้แก่ อ่อนแรง ปวดหัว ง่วงนอน คลื่นไส้ อาเจียน ปากแห้ง ท้องผูก ปวดกระดูกและกล้ามเนื้อ ความผิดปกติของเนื้อเยื่อ, เยื่อบุตาอักเสบ (เนื่องจากการกลายเป็นปูน), แสง, ตับอ่อนอักเสบ, น้ำมูกไหล, อาการคัน, hyperthermia, ความใคร่ที่ลดลง, อัลบูมินูเรีย, ไขมันในเลือดสูง, SGOT และ SGPT ที่เพิ่มขึ้น, การกลายเป็นปูนนอกมดลูก, ความดันโลหิตสูง, ภาวะหัวใจเต้นผิดจังหวะและไม่ค่อยมีอาการทางจิต
เนื่องจากครึ่งชีวิตของแคลซิทริออลสั้น ภาวะแคลเซียมในเลือดสูงปกติจะเกิดขึ้นภายในสองสามวันหลังจากหยุดการรักษาด้วย DERIL แต่จะเร็วกว่าระหว่างการรักษาด้วยวิตามินดีหรือสารเมตาโบไลต์ของวิตามินดี
แจ้งให้แพทย์ที่เข้าร่วมหรือเภสัชกรทราบถึงการเริ่มมีอาการไม่พึงประสงค์ใดๆ ที่ไม่ได้อธิบายไว้ในเอกสารฉบับนี้
เก็บให้ห่างจากแหล่งความร้อน ความชื้น และแสง
การหมดอายุและการเก็บรักษา
คำเตือน: ห้ามใช้ยาหลังจากวันหมดอายุที่ระบุไว้บนบรรจุภัณฑ์
วันที่นี้หมายถึงผลิตภัณฑ์ในบรรจุภัณฑ์ที่ไม่บุบสลาย จัดเก็บอย่างเหมาะสม
ข้อมูลอื่น ๆ
องค์ประกอบ
แต่ละแคปซูลประกอบด้วย:
สารออกฤทธิ์: Alfacalcidol (1 α-Hydroxy Vitamin D3) 1.0 mcg
สารเพิ่มปริมาณ:
Covi-ox T70 (E306), น้ำมันมะพร้าวสกัดเย็น, เจลาติน, กลีเซอรอล, น้ำบริสุทธิ์, ไททาเนียมไดออกไซด์ (E171), เหล็กออกไซด์ (E172) รูปแบบเภสัชกรรมและบรรจุภัณฑ์ 1.0 - 30 แคปซูล 1.0 mcg.
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่แสดงอาจไม่ทันสมัย
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
DERIL 1.0 MCG แคปซูล
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
แต่ละแคปซูลประกอบด้วย: Alfacalcidol (1? -Hydroxy vitamin D3) 1.0 mcg
03.0 รูปแบบเภสัชกรรม
แคปซูลสำหรับใช้ในช่องปาก
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
ภาวะไตวาย osteodystrophy เมื่อฟอกไตหรือไม่ ภาวะพร่องพาราไทรอยด์ โรคกระดูกอ่อนที่ดื้อต่อ D หรือขึ้นอยู่กับ D (ขาดหลอก) และโรคกระดูกพรุน Rickets และ osteomalacia เนื่องจากการเปลี่ยนแปลงของไตเนื่องจากการเผาผลาญของวิตามินดี โรคกระดูกพรุนในวัยหมดประจำเดือน
04.2 วิทยาและวิธีการบริหาร
ปริมาณเริ่มต้นที่แนะนำสำหรับข้อบ่งชี้ทั้งหมด:
ผู้ใหญ่และเด็กที่มีน้ำหนักตัวมากกว่า 20 กก.: 1 ไมโครกรัมต่อวัน
เด็กต่ำกว่า 20 กก. ของน้ำหนักตัว: 0.05 mcg / kg / วัน หลังจากนั้นสามารถปรับขนาดยาได้ตามการตอบสนอง
04.3 ข้อห้าม
ภาวะแคลเซียมในเลือดสูง ไม่ควรให้ผลิตภัณฑ์ระหว่างตั้งครรภ์และให้นมบุตร บุคคล แพ้วิตามินดีหรือส่วนประกอบอื่น ๆ ของผลิตภัณฑ์
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
เนื่องจากการใช้ยา DERIL เกินขนาดสามารถทำให้เกิดภาวะแคลเซียมในเลือดสูงได้ และในบางกรณี แคลเซียมในปัสสาวะสูงควรให้แคลเซียมอย่างน้อยสัปดาห์ละ 2 ครั้งในช่วงการปรับขนาดยา เมื่อกำหนดขนาดยาที่เหมาะสมในแต่ละวันแล้ว การควบคุมระดับแคลเซียมทุกเดือนก็เพียงพอแล้ว ของ อัลคาไลน์ฟอสฟาเตสโดยทั่วไปคาดว่าจะเริ่มมีอาการของภาวะแคลเซียมในเลือดสูงดังนั้นจึงอาจเป็นอาการผิดปกติในระยะหลัง หากภาวะแคลเซียมในเลือดสูงเกิดขึ้น ยาและอาหารเสริมแคลเซียมใดๆ จะต้องหยุดชะงักชั่วคราวจนกว่าแคลเซียมจะเข้าสู่ภาวะปกติอย่างรวดเร็ว จากนั้นจึงเริ่มการรักษาต่อได้ในขนาดที่ต่ำกว่า
ควรใช้ DERIL ด้วยความระมัดระวังในผู้ป่วยที่ได้รับการรักษาด้วย digitalis เนื่องจากภาวะแคลเซียมในเลือดสูงอาจทำให้ภาวะหัวใจเต้นผิดจังหวะรุนแรงขึ้นในผู้ป่วยรายดังกล่าว เนื่องจาก DERIL มีอิทธิพลต่อการขนส่งฟอสเฟตในลำไส้ ไต และกระดูก การใช้สารตรึงฟอสฟอรัสร่วมกันจึงต้องปรับให้เข้ากับค่าของฟอสเฟต (อัตราปกติ: 2-5 มก. / 100 มล.)
เนื่องจาก Alfacalcidol เป็นสารตั้งต้นของสารออกฤทธิ์ของวิตามิน D3 ไม่ควรให้วิตามินดีและอนุพันธ์ของมันในระหว่างการรักษาด้วย DERIL การใช้ยาเกินขนาดของวิตามินดีในรูปแบบใด ๆ ทำให้เกิดอาการร้ายแรงได้
แคลเซียมในเลือดสูงที่เกิดจากปริมาณวิตามินดีในปริมาณที่มากเกินไปหรือสารเมตาโบไลต์ของวิตามินดีอาจต้องได้รับการรักษาฉุกเฉิน "ภาวะแคลเซียมในเลือดสูง หากเป็นเรื้อรัง อันที่จริงอาจทำให้เกิดการกลายเป็นปูนในหลอดเลือด ภาวะแคลเซียมในไต และการกลายเป็นปูนของเนื้อเยื่ออ่อนอื่นๆ ดังนั้นจึงจำเป็นต้องตรวจสอบให้แน่ใจว่าตัวเลขที่ได้จากการคูณค่าแคลเซียมด้วยค่าฟอสเฟต (Ca x P) ไม่เกิน 70. L" การตรวจด้วยภาพรังสีของบริเวณกายวิภาค ตำแหน่งที่อาจเกิดการกลายเป็นปูน อาจมีประโยชน์สำหรับการวินิจฉัยเบื้องต้น
เก็บให้พ้นมือเด็ก
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
การใช้ยากันชักพร้อม ๆ กันที่มีคุณสมบัติในการเหนี่ยวนำของเอนไซม์ (barbiturates, diphenylhydantoin) อาจทำให้การตอบสนองของ Alfacalcidol ลดลงโดยจำเป็นต้องเพิ่มปริมาณการใช้สารเตรียมที่มีอลูมิเนียมมากเกินไปอาจรบกวนประสิทธิภาพของยาได้ การศึกษาในสัตว์ทดลองได้ชี้ให้เห็นถึงศักยภาพที่เป็นไปได้ของการกระทำของวาร์ฟารินเมื่อใช้กับแคลซิเฟอรอล แม้ว่าจะไม่มีหลักฐานที่คล้ายคลึงกันกับการใช้อัลฟาแคลซิดอล แต่ควรใช้ความระมัดระวังเมื่อใช้ยาสองชนิดพร้อมกัน ไม่ควรใช้ยาที่มีแมกนีเซียม ในระหว่างการรักษาด้วย DERIL เพื่อหลีกเลี่ยงการเกิดภาวะ hypermagnesaemia
Cholestyramine สามารถลดการดูดซึมวิตามินที่ละลายในไขมันในลำไส้ได้ และ DERIL ด้วยเช่นกัน
04.6 การตั้งครรภ์และให้นมบุตร
ไม่ควรให้ผลิตภัณฑ์ระหว่างตั้งครรภ์และให้นมบุตร
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
ไม่มีใครรู้จัก
04.8 ผลกระทบที่ไม่พึงประสงค์
หากขนาดยาเป็นไปตามความต้องการที่แท้จริงของแต่ละบุคคล DERIL สามารถทนต่อยาได้ดี มิฉะนั้น เนื่องจากผลิตภัณฑ์มีกิจกรรม D-vitamin ผลข้างเคียงอาจปรากฏขึ้นซึ่งคล้ายกับของ hypervitaminosis D เช่น hypercalcemic syndrome หรืออาการที่เป็นพิษของแคลเซียม (ขึ้นอยู่กับความรุนแรงและระยะเวลาของ hypercalcemia) อาการเหล่านี้มีทั้ง เฉียบพลันและเรื้อรัง
อดีต ได้แก่ อ่อนแรง ปวดหัว ง่วงนอน คลื่นไส้ อาเจียน ปากแห้ง ท้องผูก ปวดกระดูกและกล้ามเนื้อ ความผิดปกติของเนื้อเยื่อ, เยื่อบุตาอักเสบ (เนื่องจากการกลายเป็นปูน), แสง, ตับอ่อนอักเสบ, น้ำมูกไหล, อาการคัน, hyperthermia, ความใคร่ที่ลดลง, อัลบูมินูเรีย, ไขมันในเลือดสูง, SGOT และ SGPT ที่เพิ่มขึ้น, การกลายเป็นปูนนอกมดลูก, ความดันโลหิตสูง, ภาวะหัวใจเต้นผิดจังหวะและไม่ค่อยมีอาการทางจิต
เนื่องจากครึ่งชีวิตของแคลซิทริออลสั้น ภาวะแคลเซียมในเลือดสูงปกติจะเกิดขึ้นภายในสองสามวันหลังจากหยุดการรักษาด้วย DERIL แต่จะเร็วกว่าระหว่างการรักษาด้วยวิตามินดีหรือสารเมตาโบไลต์ของวิตามินดี
04.9 ใช้ยาเกินขนาด
ในกรณีของภาวะแคลเซียมในเลือดสูงอย่างรุนแรงเนื่องจากการให้ยาเกินขนาดโดยไม่ได้ตั้งใจ หลังจากหยุดยาชั่วคราวแล้ว สามารถให้ยาขับปัสสาวะร่วมกับของเหลวทางหลอดเลือดดำหรือคอร์ติโคสเตียรอยด์
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
l "1? -hydroxycholecalciferol (1? -OH D3) เป็นผลิตภัณฑ์ที่ได้จากการสังเคราะห์และถูกแปลงในตับเป็น 1,25- (OH) 2D3 ซึ่งแสดงถึงเมตาบอไลต์ที่ใช้งานอยู่ซึ่งวิตามินดีออกฤทธิ์ต่อ สภาวะสมดุลของฟอสโฟแคลซิก
ในร่างกาย เมแทบอลิซึมของวิตามินดีนั้นมีลักษณะเฉพาะด้วยการไฮดรอกซิเลชันครั้งแรกซึ่งเกิดขึ้นในตับด้วยการก่อตัวของ 25 OHD3 และโดยไฮดรอกซิเลชันของไตที่สองซึ่งกำหนดการก่อตัวของ 1,25- (OH) 2D3 การบริหาร 1? -Hydroxycholecalciferol จึงช่วยให้หลีกเลี่ยงขั้นตอนการเผาผลาญที่ระดับไตของการเปลี่ยนแปลงของวิตามินดีและยังได้รับการผลิต metabolite ที่ใช้งานอยู่ ดังนั้นกิจกรรมทางเภสัชวิทยาและทางคลินิกจึงแสดงในกรณีที่ 1? - ไตขาดหรือลดลงทั้งสำหรับความเสียหายของไตและสำหรับการขาดปัจจัยภายนอกที่ควบคุมการแปลง 25 OH D3 เป็น 1,25- (OH) 2D3 การรักษาด้วย 1? -OH D3 มีลักษณะเฉพาะโดยใช้โดสที่ต่ำและมีความรวดเร็วในการดำเนินการซึ่งจะเป็นตัวกำหนดการดูดซึมแคลเซียมในลำไส้ที่เพิ่มขึ้นและการเพิ่มความเข้มข้นของแคลเซียมในซีรัม นอกจากนี้ ความเสี่ยงของภาวะแคลเซียมในเลือดสูงจะลดลงด้วยเนื่องจาก ความสั้นของระยะเวลาของการกระทำของ DERIL และความจริงที่ว่าการแปลง 1? -OH D3 เป็น 1.25 - (OH) 2D3 ถูกควบคุมด้วยกลไกป้อนกลับโดยสารประกอบไดไฮดรอกซีเลตเอง
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
L "1? -OH D3 (DERIL) มีลักษณะทางเภสัชจลนศาสตร์ดังต่อไปนี้: - มันถูกดูดซึมในลำไส้เล็ก - มันถูกกระจายเป็นหลักในตับและมีเพียงร้อยละเล็กน้อยในเยื่อบุลำไส้ - ในตับจะถูกเผาผลาญที่ 1.25 - (OH) 2D3 ถูกกำจัดอย่างรวดเร็วมากในรูปของ 1,25- (OH) 2D3 ด้วยอุจจาระ การกำจัดยังเกิดขึ้นบางส่วนผ่านทางปัสสาวะในรูปของสารประกอบที่มีขั้วมากกว่า 1? -OH D3
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ความเป็นพิษเฉียบพลัน LD50: ในหนู หนู และสุนัข p.o. (ชายและหญิง): 476-440 mcg / kg; 340-720 mcg / kg:> 500 mcg / kg. LD50: ในหนูและสุนัข iv.: 71-56 mcg / kg; > 200 ไมโครกรัม / กก.
ความเป็นพิษกึ่งเฉียบพลัน ปริมาณตั้งแต่ 0.5 ถึง 50 ไมโครกรัม / กิโลกรัมต่อวันได้รับการบริหารเป็นเวลาหนึ่งเดือนในหนู Wistar พารามิเตอร์ทางคลินิกและห้องปฏิบัติการถูกนำมาพิจารณาและทำการชันสูตรพลิกศพหลังจากการเสียสละ การกระทำหลักของ 1? -OH D3 (DERIL) อยู่ในรูปของเนื้อร้ายของหลอดเลือดแดงในกล้ามเนื้อหัวใจ ทางเดินอาหาร และกล้ามเนื้อโดยสมัครใจที่มีการเสื่อมสภาพและพังผืดของกล้ามเนื้อ .
ความเป็นพิษเรื้อรัง 1? -OH D3 (DERIL) ให้กับหนูเป็นเวลา 6 เดือนโดยให้ขนาดยาตั้งแต่ 0.02 ถึง 2.5 mcg / kg ต่อวัน พบการเปลี่ยนแปลงทางเนื้อเยื่อในไต หัวใจ หลอดเลือดแดงใหญ่ อัณฑะ ไธมัส และเยื่อบุลำไส้ พบว่าผลกระทบหลักขึ้นอยู่กับภาวะแคลเซียมในเลือดสูง การบริหารช่องปากทุกวัน 0.02 mcg / kg เป็นเวลา 6 เดือนพบว่าไม่มีพิษ พบว่าขนาดเดียวกันไม่เป็นพิษในสุนัขหลังจากให้ยาซ้ำเป็นเวลาหนึ่งปี
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
Covi-ox T70 (E306), น้ำมันมะพร้าวสกัดเย็น, เจลาติน, กลีเซอรอล, น้ำบริสุทธิ์, ไททาเนียมไดออกไซด์ (E171), ไอรอนออกไซด์ (E172)
06.2 ความเข้ากันไม่ได้
ไม่มีใครรู้จัก
06.3 ระยะเวลาที่มีผลบังคับใช้
ในบรรจุภัณฑ์ที่ไม่บุบสลาย 24 เดือน
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
เก็บให้ห่างจากแสง ความชื้น และแหล่งความร้อน
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
DERIL 1.0 ไมโครกรัม แคปซูล : กล่อง 30 แคปซูล
06.6 คำแนะนำในการใช้งานและการจัดการ
ไม่มีคำแนะนำพิเศษ
ผลิตภัณฑ์ที่ไม่ได้ใช้และของเสียที่ได้จากยานี้ต้องถูกกำจัดตามข้อกำหนดทางกฎหมายในท้องถิ่น
07.0 ผู้ทรงอำนาจการตลาด
ไอ.บี.เอ็น. - National Biotherapy Institute srl
Via Vittorio Grassi 9/15 - 00155 โรม
08.0 หมายเลขอนุญาตการตลาด
DERIL "1.0": A.I.C. NS. 032832026
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
มิถุนายน 2542
10.0 วันที่แก้ไขข้อความ
มิถุนายน 2552








-allenamento-per-dimagrire.jpg)
-a-cosa-serve.jpg)