สารออกฤทธิ์: Paricalcitol
Zemplar 5 micrograms / ml สารละลายสำหรับฉีด
เม็ดมีดบรรจุภัณฑ์ Zemplar มีจำหน่ายสำหรับขนาดบรรจุภัณฑ์:- Zemplar 1 ไมโครกรัม แคปซูลนิ่ม
- Zemplar 2 ไมโครกรัม แคปซูลนิ่ม
- Zemplar 5 micrograms / ml สารละลายสำหรับฉีด
ทำไมถึงใช้เซมพลาร์? มีไว้เพื่ออะไร?
Zemplar เป็นอะนาลอกสังเคราะห์ของวิตามินดีที่ออกฤทธิ์ซึ่งระบุในการป้องกันและรักษาระดับฮอร์โมนพาราไทรอยด์ในเลือดสูงในผู้ป่วยไตวายที่ได้รับการฟอกไต ระดับฮอร์โมนพาราไธรอยด์ในระดับสูงอาจเกิดจากระดับวิตามินดี "ออกฤทธิ์" ในระดับต่ำในผู้ป่วยไตวาย
วิตามินดีในรูปแบบแอคทีฟช่วยให้การทำงานของเนื้อเยื่อต่างๆ ในร่างกายของเราเป็นปกติ รวมทั้งไตและกระดูก
ข้อห้าม เมื่อไม่ควรใช้ Zemplar
อย่าใช้เซมพลาร์
- หากคุณแพ้ (แพ้ง่าย) ต่อ paricalcitol หรือส่วนผสมอื่นๆ ของ Zemplar (ดูหัวข้อ 6)
- หากคุณมีแคลเซียมหรือวิตามินดีในเลือดสูงมาก แพทย์ของคุณจะตรวจสอบระดับเลือดของคุณและจะสามารถแจ้งให้คุณทราบหากกรณีของคุณอยู่ในเงื่อนไขข้างต้น
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนรับประทานเซมพลาร์
ดูแลเป็นพิเศษกับ Zemplar
- ก่อนเริ่มการรักษา คุณจำเป็นต้องจำกัดปริมาณฟอสฟอรัสในอาหารของคุณ ตัวอย่างอาหารที่มีฟอสฟอรัสสูง ได้แก่ ชา โซดา เบียร์ ชีส นม ครีม ปลา ตับไก่หรือเนื้อวัว ถั่ว ถั่ว ซีเรียล ถั่ว และข้าวสาลี
- อาจจำเป็นต้องใช้สารยึดเกาะฟอสเฟตซึ่งป้องกันการดูดซึมฟอสเฟตจากอาหาร เพื่อควบคุมระดับฟอสฟอรัส
- หากคุณกำลังใช้สารยึดเกาะฟอสเฟตที่มีแคลเซียมเป็นส่วนประกอบ แพทย์อาจจำเป็นต้องปรับปริมาณของคุณ
- แพทย์ของคุณจะสั่งการตรวจเลือดเพื่อตรวจสอบการรักษาของคุณ
ปฏิกิริยา ยาหรืออาหารชนิดใดที่อาจเปลี่ยนผลของเซมพลาร์
แจ้งให้แพทย์ พยาบาล หรือเภสัชกรทราบ หากคุณกำลังรับประทานหรือเพิ่งกำลังใช้ยาอื่น ๆ รวมถึงยาที่ได้รับโดยไม่มีใบสั่งยา
ยาบางชนิดอาจส่งผลต่อการทำงานของ Zemplar หรือทำให้มีโอกาสเกิดผลข้างเคียงมากขึ้น ควรแจ้งให้แพทย์ทราบหากคุณกำลังใช้ยาใดๆ ต่อไปนี้:
- ยารักษาโรคติดเชื้อรา เช่น เชื้อราในเชื้อรา (candidiasis) หรือเชื้อรา (thrush) (ketoconazole)
- ยารักษาโรคหัวใจหรือความดันโลหิต (เช่น ดิจอกซินและยาขับปัสสาวะ หรือยาขับน้ำส่วนเกินออกจากร่างกายของเรา)
- ยาที่มีแมกนีเซียม (เช่น ยาย่อยอาหารบางชนิดที่เรียกว่ายาลดกรด เช่น แมกนีเซียมไตรซิลิเกต)
- ยาที่มีอะลูมิเนียม (เช่น สารยึดเกาะฟอสเฟต เช่น อะลูมิเนียมไฮดรอกไซด์)
ปรึกษาแพทย์ พยาบาล หรือเภสัชกรเพื่อขอคำแนะนำก่อนรับประทานยาใดๆ
พา Zemplar กับอาหารและเครื่องดื่ม
Zemplar สามารถรับประทานพร้อมหรือระหว่างมื้ออาหารได้
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
การตั้งครรภ์และให้นมบุตร
หากคุณกำลังตั้งครรภ์หรือวางแผนที่จะตั้งครรภ์ ให้แจ้งแพทย์หรือพยาบาลของคุณก่อนใช้ยาเซมพลาร์
ไม่ทราบว่าเซมพลาร์ปลอดภัยสำหรับสตรีมีครรภ์หรือให้นมบุตรหรือไม่ ดังนั้นอย่าใช้จนกว่าคุณจะได้พูดคุยกับแพทย์ของคุณซึ่งจะช่วยให้คุณตัดสินใจได้ดีที่สุดสำหรับคุณ
ปรึกษาแพทย์ พยาบาล หรือเภสัชกรเพื่อขอคำแนะนำก่อนรับประทานยาใดๆ
การขับรถและการใช้เครื่องจักร
ไม่มีการศึกษาเกี่ยวกับผลกระทบที่เกี่ยวข้องกับความสามารถในการขับขี่หรือใช้เครื่องจักร Zemplar อาจส่งผลต่อความสามารถในการขับขี่ยานพาหนะได้อย่างปลอดภัยหรือใช้เครื่องจักรกลหนัก อาการวิงเวียนศีรษะอ่อนเพลียและ / หรือง่วงนอนเป็นผลข้างเคียงจากการรักษาด้วย Zemplar
อย่าขับรถหรือใช้เครื่องจักรหากคุณแสดงอาการเหล่านี้
ข้อมูลสำคัญเกี่ยวกับส่วนผสมบางอย่างของ Zemplar
ยานี้มีเอทานอล 20% v / v (แอลกอฮอล์) แต่ละโดสสามารถบรรจุเอทานอลได้มากถึง 1.3 กรัม การปรากฏตัวของเอทานอลในยานี้เป็นอันตรายต่อผู้ที่เป็นโรคพิษสุราเรื้อรังและควรได้รับการพิจารณาอย่างเหมาะสมเมื่อให้ยาแก่สตรีมีครรภ์หรือให้นมบุตร เด็ก และกลุ่มที่มีความเสี่ยงสูง เช่น ผู้ป่วยโรคตับหรือโรคลมชัก
ปริมาณและวิธีการใช้ วิธีใช้ Zemplar: Dosage
จากผลการทดสอบในห้องปฏิบัติการ แพทย์ของคุณจะตัดสินใจเลือกขนาดยาเริ่มต้นที่เหมาะสมสำหรับคุณ เมื่อเริ่มการรักษาด้วย Zemplar แล้ว มีแนวโน้มว่าจะมีการปรับขนาดยา ขึ้นอยู่กับผลการทดสอบในห้องปฏิบัติการเป็นประจำ จากผลการทดสอบในห้องปฏิบัติการ แพทย์ของคุณจะช่วยคุณกำหนดขนาดยาเซมพลาร์ที่เหมาะสม
แพทย์หรือพยาบาลจะจ่าย Zemplar ให้กับคุณในระหว่างการฟอกเลือดผ่านสายเลือดที่ใช้เชื่อมต่อคุณกับเครื่อง คุณไม่จำเป็นต้องฉีดยา เนื่องจาก Zemplar สามารถใส่ลงในหลอดที่ใช้สำหรับการรักษาได้โดยตรง Zemplar จะมอบให้คุณวันเว้นวัน ไม่เกินสามครั้งต่อสัปดาห์
ยาเกินขนาด จะทำอย่างไรถ้าคุณทานเซมพลามากเกินไป
การใช้ยาเกินขนาดของ Zemplar อาจทำให้แคลเซียม (ในเลือดและปัสสาวะ) เพิ่มขึ้นผิดปกติและระดับฟอสเฟตในเลือดซึ่งอาจต้องได้รับการรักษา นอกจากนี้ การใช้ยาเกินขนาดของ Zemplar สามารถลดระดับฮอร์โมนพาราไทรอยด์ได้ อาการที่อาจเกิดขึ้นไม่นานหลังจากรับประทานยา Zemplar เกินขนาด ได้แก่:
- ความรู้สึกอ่อนแอและ / หรือชา
- ปวดหัว
- คลื่นไส้หรือรู้สึกไม่สบาย
- ปากแห้ง ท้องผูก
- ปวดกล้ามเนื้อหรือกระดูก
- เปลี่ยนรสชาติ
อาการที่อาจเกิดขึ้นในระยะเวลานานของการใช้ Zemplar มากเกินไป ได้แก่:
- เบื่ออาหาร
- อาการง่วงนอน
- ลดน้ำหนัก
- ไม่สบายตา
- น้ำมูกไหล
- คันผิวหนัง
- รู้สึกร้อนและเป็นไข้
- สูญเสียความใคร่
- ปวดท้องรุนแรง
- นิ่วในไต
- ความดันโลหิตสามารถเปลี่ยนแปลงได้และหัวใจเต้นผิดปกติ (ใจสั่น) อาจปรากฏขึ้น
Zemplar มีโพรพิลีนไกลคอล 30% v / v เป็นสารเพิ่มปริมาณ มีรายงานแยกเกี่ยวกับผลกระทบที่เป็นพิษที่เกี่ยวข้องกับการใช้โพรพิลีนไกลคอลในปริมาณสูง กรณีดังกล่าวไม่ควรเกิดขึ้นเมื่อให้ผู้ป่วยไตเทียม เนื่องจากโพรพิลีนไกลคอลจะถูกล้างออกจากเลือดในระหว่างกระบวนการฟอกไต
หากคุณมีระดับแคลเซียมในเลือดสูงหลังจากรับประทานเซมพลาร์ แพทย์จะดูแลให้แน่ใจว่าคุณได้รับการรักษาที่เหมาะสมเพื่อฟื้นฟูระดับแคลเซียมในเลือดให้เป็นปกติ เมื่อระดับแคลเซียมในเลือดของคุณกลับมาเป็นปกติ คุณอาจได้รับยาเซมพลาร์ในปริมาณที่น้อยลง
แพทย์ของคุณจะยังตรวจระดับเลือดของคุณ และหากคุณสังเกตเห็นอาการข้างต้น ให้ปรึกษาแพทย์ทันที
ผลข้างเคียง ผลข้างเคียงของ Zemplar คืออะไร?
เช่นเดียวกับยาทั้งหมด Zemplar สามารถทำให้เกิดผลข้างเคียงได้แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
มีรายงานอาการแพ้ต่างๆ กับ Zemplar
สำคัญ: แจ้งให้แพทย์หรือพยาบาลทราบทันที หากคุณสังเกตเห็นผลข้างเคียงใด ๆ ต่อไปนี้:
- หายใจดังเสียงฮืด ๆ
- หายใจลำบากหรือกลืนลำบาก
- หายใจลำบาก
- ผดผื่น คันผิวหนัง หรือลมพิษ
- อาการบวมที่ใบหน้า ริมฝีปาก ปาก ลิ้นหรือลำคอ
บอกแพทย์หรือเภสัชกรของคุณหากคุณสังเกตเห็นผลข้างเคียงใด ๆ ต่อไปนี้:
ผลข้างเคียงที่พบบ่อยที่สุด (อย่างน้อย 1 ใน 100 คน):
- ปวดหัว
- เปลี่ยนรสชาติ
- คันผิวหนัง
- ระดับฮอร์โมนพาราไทรอยด์ต่ำ
- ระดับแคลเซียมสูง (คลื่นไส้หรือรู้สึกไม่สบายท้องผูกหรือสับสน); ฟอสฟอรัสในเลือด (อาจไม่มีอาการ แต่มีความไวต่อการแตกหักมากกว่า)
ผลข้างเคียงที่พบได้น้อย (อย่างน้อย 1 ใน 1,000 คน):
- อาการแพ้ (เช่น หายใจมีเสียงหวีด หายใจมีเสียงหวีด มีผื่น คันหรือบวมที่ใบหน้าและริมฝีปาก) ตุ่มคัน
- การติดเชื้อในเลือด ลดจำนวนเม็ดเลือดแดง (โรคโลหิตจาง - อ่อนเพลีย, หายใจถี่, ซีด); ลดจำนวนเม็ดเลือดขาว (เพิ่มความไวต่อการติดเชื้อ); ต่อมบวมที่คอ รักแร้ และ / หรือขาหนีบ; เลือดออกเป็นเวลานาน (เลือดไม่จับตัวเป็นลิ่มง่าย)
- หัวใจวาย; จังหวะ; อาการเจ็บหน้าอก; หัวใจเต้นผิดปกติ / เร็ว; ความดันโลหิตต่ำ (ความดันเลือดต่ำ); ความดันโลหิตสูง (ความดันโลหิตสูง);
- อาการโคม่า (ภาวะหมดสติในระหว่างที่บุคคลไม่สามารถตอบสนองต่อสิ่งแวดล้อมได้)
- ความเหนื่อยล้าอ่อนเพลียผิดปกติ อาการวิงเวียนศีรษะ เป็นลม
- ปวดบริเวณที่ฉีด
- โรคปอดบวม (การติดเชื้อในปอด); ของเหลวในปอด โรคหอบหืด (หายใจลำบาก, ไอ, หายใจลำบาก);
- เจ็บคอ; เย็น; ไข้; อาการคล้ายไข้หวัดใหญ่ ตาสีชมพู (คัน / ตาแห้ง); ความดันตาเพิ่มขึ้น ปวดหู เลือดกำเดาไหล
- เส้นประสาทกระตุก; ความสับสนบางครั้งรุนแรง (เพ้อ); ความปั่นป่วน (ความวิตกกังวล); ความกังวลใจ; ความผิดปกติทางบุคลิกภาพ (ไม่รู้สึกเหมือนตัวเอง);
- รู้สึกเสียวซ่าหรือชา; การลดความรู้สึกสัมผัส นอนไม่หลับ; เหงื่อออกตอนกลางคืน; กล้ามเนื้อกระตุกที่แขนและขารวมทั้งระหว่างการนอนหลับ
- ปากแห้ง; ความกระหายน้ำ; คลื่นไส้ กลืนลำบาก เขาถอย; สูญเสียความกระหาย; ลดน้ำหนัก; ปวดท้อง; ท้องร่วงและปวดท้อง ท้องผูก: เลือดออกทางทวารหนัก;
- ความยากลำบากในการแข็งตัวของอวัยวะเพศ โรคมะเร็งเต้านม; การติดเชื้อในช่องคลอด
- ปวดเต้านม; ปวดหลัง; ปวดข้อ / กล้ามเนื้อ; ความรู้สึกหนักที่เกิดจากการบวมทั่วไปหรือเฉพาะที่ของข้อเท้าเท้าและขา (บวมน้ำ); การเดินผิดปกติ
- ผมร่วง; การเจริญเติบโตของเส้นผมมากเกินไป
- เพิ่มขึ้นในเอนไซม์ตับ; ระดับฮอร์โมนพาราไทรอยด์สูง โพแทสเซียมในเลือดสูง ลดระดับแคลเซียมในเลือด
ไม่ทราบความถี่:
- อาการบวมที่ใบหน้า ริมฝีปาก ปาก ลิ้น หรือลำคอ ซึ่งอาจทำให้กลืนหรือหายใจลำบาก คันผิวหนัง (ลมพิษ) เลือดออกในกระเพาะอาหาร ปรึกษาแพทย์ทันที
คุณอาจไม่สามารถบอกได้ว่าคุณมีผลข้างเคียงใดๆ ข้างต้นหรือไม่ เว้นแต่คุณจะแจ้งให้แพทย์ทราบ
หากมีผลข้างเคียงที่ร้ายแรง หรือหากคุณสังเกตเห็นผลข้างเคียงใดๆ ที่ไม่ได้ระบุไว้ในเอกสารฉบับนี้ โปรดแจ้งให้แพทย์ พยาบาล หรือเภสัชกรทราบทันที
การหมดอายุและการเก็บรักษา
เก็บยานี้ให้พ้นมือเด็ก
ยานี้ไม่ต้องการเงื่อนไขการเก็บรักษาพิเศษใด ๆ
เมื่อเปิดแล้วควรใช้ Zemplar ทันที
อย่าใช้ Zemplar หลังจากวันหมดอายุซึ่งระบุไว้ในกล่องหลัง EXP วันหมดอายุหมายถึงวันสุดท้ายของเดือน อย่าใช้ Zemplar หากคุณสังเกตเห็นอนุภาคหรือความขุ่น
ยาไม่ควรทิ้งทางน้ำเสียหรือของเสียในครัวเรือน ถามเภสัชกรว่าจะทิ้งยาที่คุณไม่ใช้แล้วทิ้งอย่างไร ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
ข้อมูลอื่น ๆ
Zemplar ประกอบด้วยอะไรบ้าง
- สารออกฤทธิ์คือ paricalcitol สารละลายแต่ละมิลลิลิตรประกอบด้วย paricalcitol 5 ไมโครกรัม
- ส่วนผสมอื่นๆ ได้แก่ เอทานอล (แอลกอฮอล์) โพรพิลีนไกลคอล และน้ำสำหรับฉีด
Zemplar หน้าตาเป็นอย่างไรและเนื้อหาของแพ็คเกจ
สารละลายเซมพลาร์สำหรับการฉีดเป็นสารละลายใส ไม่มีสี ปราศจากอนุภาคที่มองเห็นได้ บรรจุในหลอดแก้ว 5 หลอดขนาด 1 มล. หรือ 2 มล.
ข้อมูลต่อไปนี้มีไว้สำหรับบุคลากรทางการแพทย์เท่านั้น:
สารละลาย Zemplar 5 ไมโครกรัม/มล. สำหรับฉีด
การเตรียมสารละลายสำหรับฉีด Zemplar 5 ไมโครกรัม/มล. สารละลายสำหรับฉีดใช้ครั้งเดียวเท่านั้น เช่นเดียวกับผลิตภัณฑ์ยาทั้งหมดที่ใช้โดยการฉีด สารละลายเจือจางควรตรวจดูการปรากฏตัวของอนุภาคหรือความขุ่นก่อนการบริหาร
ความเข้ากันได้
โพรพิลีนไกลคอลทำปฏิกิริยากับเฮปารินและทำให้ผลของของมันเป็นกลาง สารละลาย Zemplar สำหรับการฉีดประกอบด้วยโพรพิลีนไกลคอลเป็นสารเพิ่มปริมาณและต้องได้รับการดูแลผ่านช่องทางการเข้าถึงอื่นนอกเหนือจากการใช้เฮปาริน
ยานี้ต้องไม่ผสมกับยาอื่น ๆ
การอนุรักษ์และความถูกต้อง
ผลิตภัณฑ์ยาที่ฉีดเข้าเส้นเลือดต้องได้รับ "การตรวจสอบด้วยสายตาสำหรับการมีอยู่ของสารเกี่ยวกับเม็ดเลือดและอาจทำให้ขุ่นมัวได้ก่อนที่จะดำเนินการให้ยา สารละลายมีความชัดเจนและไม่มีสี
ยานี้ไม่ต้องการเงื่อนไขการเก็บรักษาพิเศษใด ๆ
ยานี้มีอายุ 2 ปี
ปริมาณ วิธีการ และเวลาให้ยา
สารละลายเซมพลาร์สำหรับการฉีดต้องผ่านการฟอกไต
ผู้ใหญ่
- ควรคำนวณขนาดยาเริ่มต้นตามระดับฮอร์โมนพาราไทรอยด์ที่ตรวจวัดพื้นฐาน (PTH) โดยกำหนดขนาดยาเริ่มต้นของ paricalcitol โดยใช้สูตรต่อไปนี้:
ปริมาณเริ่มต้น (เป็นไมโครกรัม) = ระดับพื้นฐานของ PTH ที่ไม่เสียหาย แสดงเป็น pmol / l: 8; O = ระดับพื้นฐานของ PTH ที่ไม่เสียหาย แสดงเป็น pg / ml: 80
และควรให้ทางหลอดเลือดดำเป็นขนาดยาลูกใหญ่ วันเว้นวัน ตลอดเวลาระหว่างการฟอกเลือดด้วยเครื่องไตเทียม
ในการทดลองทางคลินิก ปริมาณยาที่ปลอดภัยสูงสุดคือ 40 ไมโครกรัม
- การไตเตรทปริมาณ:
ช่วงอ้างอิงที่ยอมรับในปัจจุบันสำหรับระดับ PTH ในผู้ป่วยฟอกไตที่มีภาวะไตวายเรื้อรังระยะสุดท้ายไม่ควรเกิน 1.5-3 เท่าของขีดจำกัดบนที่ไม่ใช่ปัสสาวะของค่าปกติที่ 15.9-31 8 pmol / l (150-300 pg / ml) สำหรับ PTH ที่ไม่เสียหายเพื่อให้ได้ผลลัพธ์ที่เพียงพอทางสรีรวิทยา ผู้ป่วยควรได้รับการตรวจสอบอย่างรอบคอบและกำหนดขนาดยาเป็นรายบุคคล หากพบว่ามีแคลเซียมในเลือดสูงหรือผลิตภัณฑ์ Ca x P ที่ยกระดับอย่างต่อเนื่องและมีค่ามากกว่า 5.2 mmol2 / l2 (65 mg2 / dl2) ควรลดขนาดยาหรือหยุดการบริหารจนกว่าพารามิเตอร์เหล่านี้จะไม่รวมอยู่ในมาตรฐาน หลังจากนั้นจะต้องให้ paricalcitol อีกครั้งในขนาดที่ต่ำกว่า ปริมาณ Paricalcitol อาจต้องลดลงเนื่องจากระดับ PTH ลดลงในการตอบสนองต่อการรักษา
ตารางต่อไปนี้แสดงตัวอย่างแนวทางที่แนะนำสำหรับการกำหนดขนาดยา:
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่นำเสนออาจไม่ใช่ข้อมูลล่าสุด
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
ZEMPLAR INJECTABLE SOLUTION
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
สารละลาย Zemplar 2 mcg / ml สำหรับฉีด:
สารละลายสำหรับฉีดแต่ละมิลลิลิตรมี paricalcitol 2 ไมโครกรัม
ขวดละ 1 มล. ประกอบด้วย paricalcitol 2 ไมโครกรัม
ขวดละ 1 มล. ประกอบด้วย paricalcitol 2 ไมโครกรัม
สารละลาย Zemplar 5 mcg / ml สำหรับฉีด:
สารละลายสำหรับฉีดแต่ละมิลลิลิตรประกอบด้วย paricalcitol 5 ไมโครกรัม
ขวดละ 1 มล. ประกอบด้วย paricalcitol 5 ไมโครกรัม
ขวดละ 2 มล. ประกอบด้วย paricalcitol 10 ไมโครกรัม
ขวดละ 1 มล. ประกอบด้วย paricalcitol 5 ไมโครกรัม
ขวดละ 2 มล. ประกอบด้วย paricalcitol 10 ไมโครกรัม
สารเพิ่มปริมาณ: เอทานอล (20% v / v) และโพรพิลีนไกลคอล (30% v / v)
สำหรับรายการสารปรุงแต่งทั้งหมด โปรดดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
น้ำยาฉีด
สารละลายในน้ำใสและไม่มีสี ไม่มีอนุภาคที่มองเห็นได้
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
Paricalcitol ถูกระบุในผู้ใหญ่เพื่อป้องกันและรักษา hyperparathyroidism ทุติยภูมิในผู้ป่วยไตวายเรื้อรังที่ได้รับการฟอกไต
04.2 วิทยาและวิธีการบริหาร
ปริมาณ
ผู้ใหญ่
1) ปริมาณเริ่มต้นควรคำนวณตามระดับพื้นฐานของฮอร์โมนพาราไทรอยด์ (PTH):
ควรกำหนดขนาดยาเริ่มต้นของ paricalcitol โดยใช้สูตรต่อไปนี้:
หรือ
และควรให้ทางหลอดเลือดดำเป็นขนาดยาลูกกลอนด้วยความถี่สูงสุดวันเว้นวัน ตลอดเวลาระหว่างการฟอกไต
ในการทดลองทางคลินิก ปริมาณยาที่ปลอดภัยสูงสุดคือ 40 ไมโครกรัม
2) การไตเตรทปริมาณ:
ช่วงอ้างอิงที่ยอมรับในปัจจุบันสำหรับระดับ PTH ในผู้ป่วยฟอกไตที่มีภาวะไตวายเรื้อรังระยะสุดท้ายไม่ควรเกิน 1.5-3 เท่าของขีดจำกัดบนที่ไม่ใช่ปัสสาวะของค่าปกติที่ 15.9 - 31 8 pmol / l (150 - 300 pg / ml) สำหรับ PTH ที่ไม่เสียหาย
เพื่อให้ได้ผลลัพธ์ที่เพียงพอทางสรีรวิทยา ผู้ป่วยควรได้รับการตรวจสอบอย่างรอบคอบและทำการไตเตรทขนาดยาเป็นรายบุคคล
หากพบว่ามีแคลเซียมในเลือดสูงหรือผลิตภัณฑ์ Ca x P ที่ยกระดับอย่างต่อเนื่องและมีค่ามากกว่า 5.2 mmol2 / l2 (65 mg2 / dl2) ควรลดขนาดยาหรือหยุดการบริหารจนกว่าพารามิเตอร์เหล่านี้จะไม่รวมอยู่ในมาตรฐาน หลังจากนั้นจะต้องให้ paricalcitol อีกครั้งในขนาดที่ต่ำกว่า ปริมาณ Paricalcitol อาจต้องลดลงเนื่องจากระดับ PTH ลดลงในการตอบสนองต่อการรักษา
ตารางต่อไปนี้แสดงตัวอย่างแนวทางที่แนะนำสำหรับการไทเทรตขนาดยา:
เมื่อกำหนดขนาดยา paricalcitol แล้ว ควรวัดระดับแคลเซียมและฟอสเฟตในเลือดอย่างน้อยเดือนละครั้ง แนะนำให้ตรวจสอบ PTH ในซีรัมที่ไม่บุบสลายทุกสามเดือน
ในระหว่างขั้นตอนการปรับขนาดยา paricalcitol อาจต้องทำการทดสอบในห้องปฏิบัติการบ่อยขึ้น
การด้อยค่าของตับ
ความเข้มข้นของ paricalcitol ฟรีในผู้ป่วยที่มีตับบกพร่องเล็กน้อยถึงปานกลางมีความคล้ายคลึงกับที่พบในคนที่มีสุขภาพดี และไม่จำเป็นต้องปรับขนาดยาในประชากรผู้ป่วยรายนี้ ยังไม่มีประสบการณ์ในผู้ป่วยตับวายขั้นรุนแรง
ประชากรเด็ก (0-18 ปี)
ความปลอดภัยและประสิทธิภาพของ Zemplar ไม่ได้รับการกำหนดในเด็ก ไม่มีข้อมูลในเด็กอายุต่ำกว่า 5 ปี ข้อมูลที่มีอยู่ในปัจจุบันในผู้ป่วยเด็กได้อธิบายไว้ในหัวข้อ 5.1 แต่ไม่มีคำแนะนำเกี่ยวกับ posology .
ผู้ป่วยสูงอายุ (> 65 ปี)
ประสบการณ์กับผู้ป่วยอายุ 65 ปีขึ้นไปที่ได้รับ paricalcitol ในการศึกษาระยะที่ 3 ค่อนข้างจำกัด ในระหว่างการศึกษาเหล่านี้ ไม่พบความแตกต่างอย่างมีนัยสำคัญในประสิทธิภาพหรือความปลอดภัยของยาระหว่างผู้ป่วยที่อายุ 65 ปีขึ้นไปและผู้ป่วยที่อายุน้อยกว่า
วิธีการบริหาร
สารละลายเซมพลาร์สำหรับการฉีดต้องผ่านการฟอกไต
04.3 ข้อห้าม
ภูมิไวเกินต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อ 6.1
ความเป็นพิษของวิตามินดี
ภาวะแคลเซียมในเลือดสูง
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
การยับยั้งการหลั่งฮอร์โมนพาราไทรอยด์มากเกินไปอาจทำให้ระดับแคลเซียมในซีรัมเพิ่มขึ้น และอาจนำไปสู่การเกิดโรคเกี่ยวกับการเผาผลาญอาหาร เพื่อให้ได้ค่าอ้างอิงทางสรีรวิทยาที่เพียงพอ ผู้ป่วยควรได้รับการตรวจสอบอย่างรอบคอบและทำการไตเตรทขนาดยาเป็นรายบุคคล
หากเกิดภาวะแคลเซียมในเลือดสูงที่มีนัยสำคัญทางคลินิก และผู้ป่วยได้รับการรักษาด้วยคีเลเตอร์ฟอสเฟตไอออนที่มีแคลเซียมเป็นส่วนประกอบ ควรลดขนาดยาคีเลเตอร์นี้หรือหยุดให้ยา
ภาวะแคลเซียมในเลือดสูงเรื้อรังอาจเกี่ยวข้องกับการกลายเป็นปูนในหลอดเลือดทั่วไปและการกลายเป็นปูนในเนื้อเยื่ออ่อนอื่นๆ
ไม่ควรรับประทานผลิตภัณฑ์ยาที่เกี่ยวข้องกับฟอสเฟตหรือวิตามินดีร่วมกับ paricalcitol เนื่องจากอาจมีความเสี่ยงที่จะเกิดภาวะแคลเซียมในเลือดสูงและอาจส่งผลให้ผลิตภัณฑ์ Ca x P เพิ่มขึ้น (ดูหัวข้อ 4.5)
ความเป็นพิษของ Digitalis เกิดขึ้นได้จากภาวะแคลเซียมในเลือดสูงจากแหล่งกำเนิดใดๆ ดังนั้น ควรใช้ความระมัดระวังอย่างยิ่งในผู้ป่วยที่ได้รับการรักษาด้วย paricalcitol ที่รับประทาน digitalis ร่วมกัน (ดูหัวข้อ 4.5)
ควรใช้ความระมัดระวังหากใช้ยา paricalcitol และ ketoconazole ร่วมกัน (ดูหัวข้อ 4.5)
ยานี้มีเอทานอล 20% v / v (แอลกอฮอล์) แต่ละโดสสามารถบรรจุเอทานอลได้มากถึง 1.3 กรัม การปรากฏตัวของเอธานอลในผลิตภัณฑ์ยานี้อาจเป็นอันตรายต่อผู้ที่เป็นโรคพิษสุราเรื้อรังและต้องนำมาพิจารณาเมื่อให้ยาแก่สตรีมีครรภ์และให้นมบุตร ผู้ป่วยเด็ก และกลุ่มที่มีความเสี่ยงสูง เช่น ผู้ป่วยโรคตับหรือโรคลมชัก
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
ไม่มีการศึกษาปฏิสัมพันธ์กับ paricalcitol ในรูปแบบที่ฉีดได้. อย่างไรก็ตาม มีการศึกษาเพื่อประเมินการทำงานร่วมกันระหว่าง ketoconazole และ paricalcitol โดยใช้สูตรแคปซูล
ผลิตภัณฑ์ฟอสเฟตหรือวิตามินดีที่คล้ายคลึงกันไม่ควรรับประทานร่วมกับ paricalcitol เนื่องจากมีความเสี่ยงที่จะเกิดภาวะแคลเซียมในเลือดสูง และการเพิ่มขึ้นของผลิตภัณฑ์ CaxP (ดูหัวข้อ 4.4)
การใช้ยาที่มีแคลเซียมในปริมาณสูงหรือยาขับปัสสาวะ thiazide อาจเพิ่มความเสี่ยงต่อภาวะแคลเซียมในเลือดสูงได้
ไม่ควรใช้ผลิตภัณฑ์สมุนไพรที่มีอะลูมิเนียม (เช่น ยาลดกรดหรือสารคีเลเตอร์ฟอสเฟตไอออน) ในการรักษาระยะยาวร่วมกับผลิตภัณฑ์ยาที่มีวิตามินดี เนื่องจากอาจทำให้ระดับอะลูมิเนียมในเลือดเพิ่มขึ้น และความเป็นพิษต่อกระดูกจากอะลูมิเนียม
ยาที่มีแมกนีเซียม (เช่น ยาลดกรด) ไม่ควรรับประทานควบคู่กับยาที่มีวิตามินดี เนื่องจากอาจเกิดภาวะแมกนีเซียมในเลือดสูงได้
เป็นที่ทราบกันดีว่า Ketoconazole เป็นตัวยับยั้งที่ไม่เฉพาะเจาะจงของเอนไซม์ cytochrome P450 หลายตัว
ข้อมูลที่มีอยู่ในร่างกายและในหลอดทดลองชี้ให้เห็นว่า ketoconazole อาจโต้ตอบกับเอนไซม์ที่มีหน้าที่ในการเผาผลาญของ paricalcitol และสารคล้ายคลึงวิตามินดีอื่น ๆ
ควรใช้ความระมัดระวังเป็นพิเศษเมื่อให้ paricalcitol ร่วมกับ ketoconazole (ดูหัวข้อ 4.4) ผลของการใช้ยา ketoconazole หลายขนาดในขนาด 200 มก. วันละสองครั้ง (BID) เป็นเวลา 5 วัน ต่อเภสัชจลนศาสตร์ของแคปซูล paricalcitol ได้รับการศึกษาในคนที่มีสุขภาพดี เมื่อมี ketoconazole Cmax ของ paricalcitol ได้รับผลกระทบในค่าเฉลี่ย ครึ่งชีวิตของ paricalcitol เท่ากับ 17.0 ชั่วโมงเมื่อมี ketoconazole เทียบกับ 9.8 ชั่วโมงเมื่อให้ paricalcitol เพียงอย่างเดียว ผลการศึกษานี้บ่งชี้ว่าภายหลังการให้ paricalcitol ทางปาก การเพิ่มขึ้นของ AUCo-? of paricalcitol เนื่องจากปฏิกิริยาระหว่างยากับ ketoconazole ไม่ควรเกินสองเท่า
ความเป็นพิษของ Digitalis เพิ่มขึ้นเมื่อมีภาวะแคลเซียมในเลือดสูงจากแหล่งกำเนิดใดๆ ดังนั้น ควรใช้ความระมัดระวังอย่างยิ่งหากกำหนด digitalis ร่วมกับ paricalcitol (ดูหัวข้อ 4.4)
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์
มีข้อมูลไม่เพียงพอเกี่ยวกับการใช้ paricalcitol ในหญิงตั้งครรภ์ การศึกษาในสัตว์ทดลองแสดงให้เห็นถึงความเป็นพิษต่อการเจริญพันธุ์ (ดูหัวข้อ 5.3) ความเสี่ยงที่อาจเกิดขึ้นในมนุษย์ไม่เป็นที่รู้จัก ไม่ควรใช้ Zemplar ในระหว่างตั้งครรภ์เว้นแต่จำเป็นอย่างยิ่ง
ให้นมลูก
การศึกษาในสัตว์ทดลองแสดงให้เห็นว่า paricalcitol หรือสารเมตาบอลิซึมถูกขับออกมาในน้ำนมแม่ในปริมาณเล็กน้อย ต้องตัดสินใจว่าจะยุติการให้นมแม่หรือยุติการรักษาด้วยยา paricalcitol โดยคำนึงถึงประโยชน์ของการให้นมบุตรสำหรับเด็กและประโยชน์ของการรักษาด้วย paricalcitol สำหรับสตรี
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
Paricalcitol มีผลเพียงเล็กน้อยต่อความสามารถในการขับหรือใช้เครื่องจักร อาการวิงเวียนศีรษะอาจเกิดขึ้นหลังจากให้ยา paricalcitol (ดูหัวข้อ 4.8)
04.8 ผลกระทบที่ไม่พึงประสงค์
ในการทดลองทางคลินิกระยะที่ II / III / IV ผู้ป่วยประมาณ 600 รายได้รับการรักษาด้วย Zemplar โดยรวมแล้ว 6% ของผู้ป่วยที่รักษาด้วย Zemplar รายงานอาการไม่พึงประสงค์
อาการไม่พึงประสงค์ที่พบบ่อยที่สุดที่เกี่ยวข้องกับการรักษาด้วย Zemplar คือภาวะแคลเซียมในเลือดสูงซึ่งเกิดขึ้นในผู้ป่วย 4.7% ภาวะแคลเซียมในเลือดสูงขึ้นอยู่กับระดับของการปราบปรามฮอร์โมนพาราไทรอยด์มากเกินไปและสามารถลดลงได้โดยการไตเตรทขนาดยาที่เพียงพอ
อาการข้างเคียงที่อาจเกิดขึ้นจากการใช้ยา paricalcitol ทั้งทางคลินิกและทางห้องปฏิบัติการ แสดงไว้ในตารางต่อไปนี้ตามระเบียบข้อบังคับของ MedDRA โดยการจำแนกอวัยวะของระบบและความถี่ เกี่ยวกับความถี่ ใช้หมวดหมู่ต่อไปนี้: พบบ่อยมาก (≥ 1 / 1O); ทั่วไป (≥ 1/100,
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านการดูแลสุขภาพรายงานอาการไม่พึงประสงค์ใดๆ ผ่านระบบการรายงานระดับประเทศ ที่อยู่ www.agenziafarmaco.gov .it/it/responsabili.
04.9 ใช้ยาเกินขนาด
ไม่มีรายงานกรณีที่ให้ยาเกินขนาด
การให้ยา Paricalcitol เกินขนาดสามารถนำไปสู่ภาวะแคลเซียมในเลือดสูง, แคลเซียมในปัสสาวะสูง, ภาวะฟอสฟอรัสในเลือดสูง และการปราบปราม PHT มากเกินไป (ดูหัวข้อ 4.4)
ในกรณีที่ให้ยาเกินขนาด ควรตรวจสอบและรายงานอาการและอาการแสดงของภาวะแคลเซียมในเลือดสูง (ระดับแคลเซียมในซีรัม) ต่อแพทย์ ต้องเริ่มการรักษาอย่างเหมาะสม
Paricalcitol ไม่ได้ถูกกำจัดโดยการฟอกไตอย่างมีนัยสำคัญ การรักษาผู้ป่วยที่มี "ภาวะแคลเซียมในเลือดสูงที่มีนัยสำคัญทางคลินิก" คือการลดขนาดยาทันทีหรือหยุดการรักษาด้วย paricalcitol ทันทีและการรับประทานอาหารที่มีแคลเซียมสูง การระงับการเสริมแคลเซียม การเคลื่อนย้ายผู้ป่วย การควบคุมอิเล็กโทรไลต์ และ ความไม่สมดุลของของเหลว การประเมินการเปลี่ยนแปลงของคลื่นไฟฟ้าหัวใจ (ที่มีความสำคัญพื้นฐานในผู้ป่วยที่ได้รับการรักษาด้วยดิจิไทลิส) และ "การฟอกไตหรือการล้างไตทางช่องท้องด้วย dialysate ที่ปราศจากแคลเซียมตามที่อนุญาต
เมื่อระดับแคลเซียมในซีรัมกลับสู่ระดับปกติแล้ว สามารถให้ paricalcitol อีกครั้งในขนาดที่ต่ำกว่า หากระดับแคลเซียมในเลือดเพิ่มขึ้นอย่างต่อเนื่องและเด่นชัด ควรพิจารณาทางเลือกในการรักษาที่หลากหลาย ซึ่งรวมถึงการใช้ยา เช่น ฟอสเฟตและคอร์ติโคสเตียรอยด์ ตลอดจนมาตรการกระตุ้นการขับปัสสาวะ
สารละลายเซมพลาร์สำหรับการฉีดประกอบด้วยโพรพิลีนไกลคอล 30% v / v เป็นสารเพิ่มปริมาณ กรณีที่แยกได้ของภาวะซึมเศร้าของระบบประสาทส่วนกลาง ภาวะเม็ดเลือดแดงแตกและกรดแลคติกได้รับรายงานว่าเป็นพิษที่เกี่ยวข้องกับการใช้โพรพิลีนไกลคอลในปริมาณสูง แม้ว่าจะไม่คาดว่าจะเกิดพิษดังกล่าวหลังจากใช้ Zemplar เนื่องจากโพรพิลีนไกลคอลถูกกำจัดในระหว่างกระบวนการฟอกไต แต่ความเสี่ยงของผลกระทบที่เป็นพิษในกรณีที่ให้ยาเกินขนาดยังคงต้องได้รับการพิจารณา
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มยารักษาโรค: ยาต้านพาราไทรอยด์ รหัส ATC: H05BX02
กลไกการออกฤทธิ์
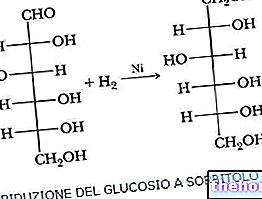
Paricalcitol เป็นอะนาล็อกสังเคราะห์ของ calcitriol ซึ่งเป็นรูปแบบที่ออกฤทธิ์ทางชีวภาพของวิตามินดีโดยมีการดัดแปลงที่สายโซ่ด้านข้าง (D2) และวงแหวน A (19-nor) ซึ่งแตกต่างจาก calcitriol Paricalcitol เป็นตัวกระตุ้นที่เลือกของวิตามินดี (VDR) ) Paricalcitol คัดเลือกกระตุ้นตัวรับวิตามินดีในต่อมพาราไทรอยด์โดยไม่ทำให้ตัวรับวิตามินดีเพิ่มขึ้นในลำไส้และทำงานน้อยลงในการสลายของกระดูก นอกจากนี้ paricalcitol ยังกระตุ้นตัวรับที่ไวต่อแคลเซียม (CaSR) ที่มีอยู่ในต่อมพาราไทรอยด์ ดังนั้น paricalcitol ช่วยลดระดับฮอร์โมนพาราไทรอยด์ (PTH) โดยการยับยั้งการแพร่กระจายของพาราไทรอยด์และลดการสังเคราะห์และการหลั่ง PTH โดยส่งผลกระทบต่อระดับแคลเซียมและฟอสฟอรัสน้อยที่สุด paricalcitol สามารถทำหน้าที่โดยตรงกับเซลล์สร้างกระดูกเพื่อรักษาปริมาตรของกระดูกและปรับปรุงพื้นผิวของแร่ธาตุ การแก้ไขระดับฮอร์โมนพาราไทรอยด์ที่เปลี่ยนแปลงไป ร่วมกับการทำให้แคลเซียมและฟอสฟอรัสสมดุลเป็นปกติ สามารถป้องกันหรือรักษาโรคกระดูกเมตาบอลิซึมที่เกี่ยวข้องกับภาวะไตวายเรื้อรังได้
ประชากรเด็ก
ความปลอดภัยและประสิทธิภาพของ Zemplar ได้รับการประเมินในการศึกษาแบบ randomized double-blind และ placebo-controlled แบบ randomized double-blind ระยะเวลา 12 สัปดาห์ ในผู้ป่วยไตวายเรื้อรังระยะสุดท้าย 29 คนในวัย 5 ถึง 19 ปี ในการศึกษานี้ ผู้ป่วยที่อายุน้อยที่สุด 6 คนที่ได้รับการรักษาด้วย เซมพลาร์มีอายุตั้งแต่ 5 ถึง 12 ปี ปริมาณเริ่มต้นของ Zemplar คือ 0.04 mcg / kg 3 ครั้งต่อสัปดาห์ตามลำดับ ถ้าระดับ iPTH พื้นฐานต่ำกว่า 500 pg / mL หรือ 0.08 mcg / kg 3 ครั้งต่อสัปดาห์หากระดับพื้นฐานคือ iPTH ≥ 500 pg / mL ปริมาณของ Zemplar ได้รับการปรับเพิ่มขึ้น 0.04 ไมโครกรัมต่อกิโลกรัมตามระดับซีรั่มของผลิตภัณฑ์ iPTH แคลเซียมและ Ca x P 67% ของผู้ป่วยที่ได้รับ Zemplar และ 14% ของผู้ป่วยที่ได้รับการรักษาเสร็จสิ้นการศึกษา ด้วยยาหลอก 60% ของอาสาสมัครในกลุ่ม Zemplar มีระดับ iPTH ลดลง 2 ครั้งติดต่อกัน 30% จากระดับพื้นฐานเมื่อเทียบกับ 21% ของผู้ป่วยในกลุ่มยาหลอก เนื่องจากระดับ iPTH เพิ่มขึ้นมากเกินไป ผู้ป่วย 71% ในกลุ่มยาหลอกต้องออกจากการศึกษา ทั้งในกลุ่ม Zemplar และในกลุ่มยาหลอกไม่พัฒนาภาวะแคลเซียมในเลือดสูง ไม่มีข้อมูลสำหรับผู้ป่วยที่อายุต่ำกว่า 5 ปี
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
การกระจาย
เภสัชจลนศาสตร์ของ paricalcitol ได้รับการศึกษาในผู้ป่วยที่มีภาวะไตวายเรื้อรัง (CRF) ซึ่งจำเป็นต้องมีการฟอกไต Paricalcitol เป็นยาฉีดเข้าเส้นเลือดดำ ภายใน 2 ชั่วโมงของการบริหารขนาดยาตั้งแต่ 0.04 และ 0.24 ไมโครกรัมต่อกิโลกรัม ความเข้มข้นของ paricalcitol ลดลงอย่างรวดเร็ว ต่อมา ความเข้มข้นของ paricalcitol ลดลงในลักษณะเชิงเส้นแบบลอการิทึม โดยมีครึ่งชีวิตเฉลี่ยประมาณ 15 ชั่วโมง นอกจากนี้ยังไม่พบการสะสมของ paricalcitol เมื่อมีการใช้ยาหลายขนาน การจับกับโปรตีนในพลาสมาของ paricalcitol ในหลอดทดลอง พบว่ามีความเข้มข้นมาก (> 99.9%) และไม่อิ่มตัวตลอดช่วงความเข้มข้นระหว่าง 1 ng / mL และ 100 ng / mL
การเปลี่ยนแปลงทางชีวภาพ
ในปัสสาวะและอุจจาระ มีการระบุสารที่ไม่รู้จักหลายชนิดและไม่พบ paricalcitol ในปัสสาวะ สารเมตาโบไลต์เหล่านี้ยังไม่ได้รับการระบุลักษณะหรือระบุ โดยรวมแล้ว เมแทบอไลต์เหล่านี้มีส่วนทำให้เกิดกัมมันตภาพรังสีในปัสสาวะ 51% และกัมมันตภาพรังสีในอุจจาระ 59%
การกำจัด
ในคนที่มีสุขภาพดี การศึกษาได้ดำเนินการโดยให้ 3H-paricalcitol ขนาด 0.16 mcg / kg ครั้งเดียว (n = 4) ทางหลอดเลือดดำ กัมมันตภาพรังสีที่พบในพลาสมาคือ Paricalcitol ถูกกำจัดโดยการขับถ่ายของตับและท่อน้ำดีเป็นหลัก โดย 74% ของ ปริมาณกัมมันตภาพรังสีถูกกู้คืนในอุจจาระและมีเพียง 16% เท่านั้นที่ฟื้นตัวในปัสสาวะ
ประชากรพิเศษ
เพศ เชื้อชาติ และอายุ: ในผู้ป่วยผู้ใหญ่ที่ศึกษา ไม่พบความแตกต่างทางเภสัชจลนศาสตร์ที่เกี่ยวข้องกับอายุหรือเพศ ไม่พบความแตกต่างทางเภสัชจลนศาสตร์เนื่องจากเชื้อชาติ
การด้อยค่าของตับ: ความเข้มข้นของ paricalcitol ฟรีในผู้ป่วยที่มีภาวะตับบกพร่องระดับเล็กน้อยถึงปานกลางมีความคล้ายคลึงกับที่รายงานในอาสาสมัครที่มีสุขภาพดี และไม่จำเป็นต้องปรับขนาดยาในประชากรผู้ป่วยรายนี้ ไม่มีประสบการณ์ในผู้ป่วยตับวายขั้นรุนแรง
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ข้อมูลเด่นจากการศึกษาความเป็นพิษในขนาดยาซ้ำในสัตว์ฟันแทะและสุนัขโดยทั่วไปมักระบุถึงกิจกรรมแคลเซียมของ paricalcitol ผลกระทบที่ไม่เกี่ยวข้องกับภาวะแคลเซียมในเลือดสูงอย่างชัดเจน ได้แก่ การลดจำนวนเม็ดเลือดขาวในสุนัข , การฝ่อของต่อมไทมัสในสุนัขและ การปรากฏตัวของค่าที่เปลี่ยนแปลงของเวลา thromboplastin บางส่วนที่เปิดใช้งาน (เพิ่มขึ้นในสุนัขและลดลงในหนู) ไม่มีการเปลี่ยนแปลงจำนวนเม็ดเลือดขาวในการศึกษาทางคลินิก
Paricalcitol ไม่ก่อให้เกิดผลเสียต่อภาวะเจริญพันธุ์ของหนู และพบว่าไม่มีกิจกรรมการก่อมะเร็งในหนูหรือกระต่าย การเตรียมวิตามินดีในปริมาณสูงที่ให้แก่สัตว์ที่ตั้งครรภ์ทำให้เกิดการก่อให้เกิดการก่อวิรูป
Paricalcitol แสดงให้เห็นว่ามีอิทธิพลต่อความสามารถในการมีชีวิตของทารกในครรภ์ และอาจส่งเสริมการเพิ่มขึ้นอย่างมีนัยสำคัญในการเสียชีวิตระหว่างตั้งครรภ์และหลังคลอดในหนูแรกเกิดเมื่อให้ยาในปริมาณที่เป็นพิษต่อมารดา
ระหว่างชุดการทดสอบความเป็นพิษทางพันธุกรรม ในหลอดทดลอง และ ในร่างกายได้รับการแสดงให้เห็นว่า paricalcitol ไม่มีกิจกรรมที่เป็นพิษต่อยีนที่อาจเกิดขึ้น
การศึกษาเกี่ยวกับสารก่อมะเร็งในหนูไม่ได้บ่งชี้ถึงความเสี่ยงใด ๆ เมื่อใช้ paricalcitol ในมนุษย์
ปริมาณที่ให้และ / หรือได้รับยา paricalcitol อย่างเป็นระบบจะสูงกว่าปริมาณที่ใช้ในการรักษา / การได้รับสัมผัสทั่วร่างกายเล็กน้อย
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
เอทานอล (20% โวลต์ / โวลต์)
โพรพิลีนไกลคอล
น้ำสำหรับฉีด
06.2 ความเข้ากันไม่ได้
ในกรณีที่ไม่มีการศึกษาความเข้ากันได้ ยานี้ต้องไม่ผสมกับผลิตภัณฑ์ยาอื่น ๆ
โพรพิลีนไกลคอลทำปฏิกิริยากับเฮปารินและทำให้ผลของของมันเป็นกลาง สารละลาย Zemplar สำหรับการฉีดประกอบด้วยโพรพิลีนไกลคอลเป็นสารเพิ่มปริมาณและต้องได้รับการดูแลผ่านช่องทางการเข้าถึงอื่นนอกเหนือจากการใช้เฮปาริน
06.3 ระยะเวลาที่ใช้ได้
2 ปี.
ใช้ทันทีหลังเปิดใช้
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
ยานี้ไม่ต้องการเงื่อนไขการจัดเก็บพิเศษใด ๆ
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
สารละลาย Zemplar 2 mcg / ml สำหรับฉีด:
ขวดแก้วชนิดที่ 1 แต่ละขวดมีสารละลายสำหรับฉีด 1 มล.
ขวดแก้วชนิดที่ 1 แต่ละขวดมีสารละลายสำหรับฉีด 1 มล.
การนำเสนอ Zemplar คือ:
หนึ่งซองบรรจุสารละลาย 1 มล. 5 หลอดสำหรับฉีด
หนึ่งแพ็คประกอบด้วย 5 ขวดสารละลาย 1 มล. สำหรับฉีด
สารละลาย Zemplar 5 mcg / ml สำหรับฉีด:
ขวดแก้วชนิดที่ 1 แต่ละขวดมีสารละลายสำหรับฉีด 1 มล. หรือ 2 มล.
ขวดแก้วชนิดที่ 1 แต่ละขวดมีสารละลายสำหรับฉีด 1 มล. หรือ 2 มล.
การนำเสนอ Zemplar คือ:
หนึ่งแพ็คบรรจุสารละลาย 1 มล. 5 หลอดสำหรับฉีด
แพ็คบรรจุ 5 หลอด 2 มล. ของสารละลายสำหรับฉีด
หนึ่งแพ็คประกอบด้วย 5 ขวดสารละลาย 1 มล. สำหรับฉีด
หนึ่งแพ็คประกอบด้วย 5 ขวดสารละลาย 2 มล. สำหรับฉีด
ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
06.6 คำแนะนำในการใช้งานและการจัดการ
ผลิตภัณฑ์ยาที่ฉีดเข้าเส้นเลือดต้องได้รับ "การตรวจสอบด้วยสายตาสำหรับการมีอยู่ของสารเกี่ยวกับเม็ดเลือดและอาจทำให้ขุ่นมัวได้ก่อนที่จะดำเนินการให้ยา สารละลายมีความชัดเจนและไม่มีสี
สำหรับการใช้งานเพียงครั้งเดียวเท่านั้น ยาที่ไม่ได้ใช้และของเสียที่ได้จากยานี้ต้องกำจัดตามระเบียบข้อบังคับของท้องถิ่น
07.0 ผู้ทรงอำนาจการตลาด
AbbVie Srl
S.R. 148 Pontina km 52 snc
04011 กัมโอเวอร์เด ดิ อาพริเลีย (LT)
08.0 หมายเลขอนุญาตการตลาด
Zemplar 2 mcg / ml สารละลายสำหรับฉีด "5 หลอด 1 มล. - AIC n. 036374128
Zemplar 2 mcg / ml solution สำหรับฉีด "5 ขวดแก้ว 1 ml - AIC n. 036374155
Zemplar 5 mcg / ml สารละลายสำหรับฉีด "5 หลอด 1 มล. - AIC n. 036374015
สารละลาย Zemplar 5 mcg / ml สำหรับฉีด "5 หลอด 2 มล. - AIC n. 036374027
Zemplar 5 mcg / ml solution สำหรับฉีด "5 ขวดแก้ว 1 ml - AIC n. 036374130
Zemplar 5 mcg / ml solution สำหรับฉีด "5 ขวดแก้ว 2 ml - AIC n. 036374142
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
วันที่ได้รับอนุญาตครั้งแรก: 22 มกราคม 2548
วันที่ต่ออายุครั้งล่าสุด: 22 พฤศจิกายน 2553
10.0 วันที่แก้ไขข้อความ
09/2016