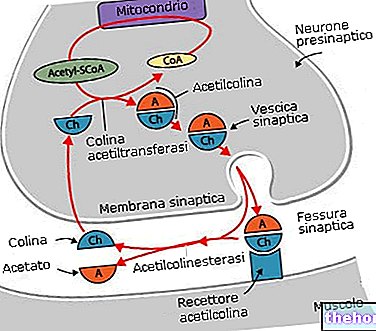
สารออกฤทธิ์: Fingolimod
GILENYA 0.5 มก. แคปซูลแข็ง
เหตุใดจึงใช้ Gilenya? มีไว้เพื่ออะไร?
กิเลนยาคืออะไร
สารออกฤทธิ์ใน Gilenya คือ fingolimod
Gilenya มีไว้เพื่ออะไร
Gilenya ใช้ในผู้ใหญ่เพื่อรักษาโรคปลอกประสาทเสื่อมแข็ง (MS) โดยเฉพาะอย่างยิ่งใน:
ผู้ป่วยที่ไม่ตอบสนองต่อการรักษาด้วย MS
หรือ
ผู้ป่วยที่มีการพัฒนาอย่างรวดเร็วของ MS ที่รุนแรง
Gilenya ไม่ได้รักษาโรค MS แต่ช่วยลดจำนวนการกำเริบของโรคและชะลอการลุกลามของความพิการทางร่างกายที่เกิดจาก MS
หลายเส้นโลหิตตีบคืออะไร
MS เป็นโรคเรื้อรังที่ส่งผลต่อระบบประสาทส่วนกลาง (CNS) ซึ่งรวมถึงสมองและไขสันหลัง ในโรค MS การอักเสบจะทำลายปลอกป้องกัน (เรียกว่าไมอีลิน) ที่เรียงแถวเส้นประสาทในระบบประสาทส่วนกลางและป้องกันไม่ให้เส้นประสาททำงานตามที่ควรจะเป็น กระบวนการนี้เรียกว่าการดีไมอีลิเนชัน
MS Relapsing-remitting MS มีลักษณะอาการกำเริบ (กำเริบ) ของอาการทางระบบประสาทที่สะท้อนถึงสถานะการอักเสบของระบบประสาทส่วนกลาง อาการจะแตกต่างกันไปในแต่ละผู้ป่วย แต่มักเกี่ยวข้องกับการเดินลำบาก ชา การมองเห็น หรือการทรงตัว อาการของโรคกำเริบอาจหายไปอย่างสมบูรณ์เมื่อการกำเริบของโรคสิ้นสุดลง แต่ข้อร้องเรียนบางอย่างอาจยังคงอยู่
Gilenya ทำงานอย่างไร
Gilenya ช่วยปกป้องระบบประสาทจากการโจมตีของระบบภูมิคุ้มกันโดยการลดความสามารถของเซลล์เม็ดเลือดขาว (lymphocytes) ในการหมุนเวียนอย่างอิสระภายในร่างกายและป้องกันไม่ให้ไปถึงสมองและไขสันหลัง ซึ่งจำกัดความเสียหายของเส้นประสาทที่เกิดจาก MS
ข้อห้าม เมื่อไม่ควรใช้ Gilenya
อย่ากินกิเลนยา
- หากคุณมีการตอบสนองทางภูมิคุ้มกันลดลง (เนื่องจากโรคภูมิคุ้มกันบกพร่อง โรคหรือยาที่กดภูมิคุ้มกัน)
- หากคุณมีการติดเชื้อรุนแรงต่อเนื่องหรือมีการติดเชื้อเรื้อรังอย่างต่อเนื่อง เช่น ตับอักเสบหรือวัณโรค
- หากคุณเป็นมะเร็งระยะลุกลาม (ยกเว้นในกรณีที่เป็นมะเร็งผิวหนังชนิดหนึ่งที่เรียกว่ามะเร็งผิวหนังชนิดเซลล์ต้นกำเนิด)
- หากคุณมีปัญหาเกี่ยวกับตับอย่างรุนแรง
- หากคุณแพ้ fingolimod หรือส่วนผสมอื่น ๆ ของยานี้
หากข้อใดข้อหนึ่งเหล่านี้ตรงกับคุณ โปรดแจ้งให้แพทย์ทราบก่อนใช้ยากิเลนยา
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนรับประทาน Gilenya
พูดคุยกับแพทย์ของคุณก่อนรับประทาน Gilenya:
- หากคุณมีการเต้นของหัวใจผิดปกติและผิดปกติ
- หากคุณมีอาการของอัตราการเต้นของหัวใจต่ำ (เช่น เวียนศีรษะ คลื่นไส้ หรือใจสั่น)
- หากคุณมีปัญหาเกี่ยวกับหัวใจ การอุดตันของหลอดเลือดในหัวใจ เคยมีอาการหัวใจวายหรือหัวใจหยุดเต้นในอดีต หรือมีอาการเจ็บหน้าอก
- หากคุณเคยเป็นโรคหลอดเลือดสมองมาก่อน
- หากคุณประสบภาวะหัวใจล้มเหลว
- หากคุณมีปัญหาการหายใจรุนแรงขณะนอนหลับ (ภาวะหยุดหายใจขณะหลับอย่างรุนแรง)
- หากคุณได้รับแจ้งว่าคุณมี EKG ผิดปกติ
- หากคุณกำลังใช้หรือเพิ่งกินยาที่ทำให้หัวใจเต้นผิดปกติ เช่น ควินิดีน ไดโซไพราไมด์ อะมิโอดาโรน หรือโซตาลอล
- หากคุณกำลังใช้หรือเพิ่งเคยทานยาที่ทำให้หัวใจเต้นช้าลง (เช่น ยา beta blockers, verapamil, diltiazem หรือ ivabradine, digoxin, anticholinesterase drugs หรือ pilocarpine)
- หากคุณเคยมีอาการหมดสติหรือหมดสติกะทันหัน (เป็นลมหมดสติ)
- ถ้าคุณตั้งใจจะฉีดวัคซีน
- หากคุณไม่เคยเป็นโรคอีสุกอีใส
- หากคุณมีหรือมีอาการผิดปกติทางสายตาหรือสัญญาณอื่น ๆ ของอาการบวมในบริเวณที่มองเห็นส่วนกลาง (macula) ที่ด้านหลังดวงตา (สภาพที่เรียกว่า macular edema ดูด้านล่าง) หากคุณมีหรือเคยมี "การอักเสบหรือ" การติดเชื้อที่ตา (uveitis) หรือถ้าคุณมีโรคเบาหวาน (ซึ่งอาจทำให้เกิดปัญหาสายตา)
- หากคุณมีปัญหาเกี่ยวกับตับ
- หากคุณมีความดันโลหิตสูงที่ยาควบคุมไม่ได้
- หากคุณมีปัญหาเกี่ยวกับปอดอย่างรุนแรงหรือมีอาการไอจากการสูบบุหรี่
หากข้อใดข้อหนึ่งเหล่านี้ตรงกับคุณ โปรดแจ้งให้แพทย์ทราบก่อนใช้ยากิเลนยา
อัตราการเต้นของหัวใจช้า (หัวใจเต้นช้า) และหัวใจเต้นผิดปกติ: ในช่วงเริ่มต้นของการรักษา Gilenya จะทำให้อัตราการเต้นของหัวใจช้าลง ดังนั้น คุณอาจพบอาการวิงเวียนศีรษะหรือเหนื่อยล้า การรับรู้ถึงการเต้นของหัวใจหรือความดันโลหิตลดลง ให้ติดต่อคุณ แพทย์ เนื่องจากคุณอาจต้องรับการรักษาทันที Gilenya อาจทำให้หัวใจเต้นผิดปกติได้ โดยเฉพาะหลังจากให้ยาครั้งแรก การเต้นของหัวใจผิดปกติมักจะกลับมาเป็นปกติภายในเวลาไม่ถึง 1 วัน อัตราการเต้นของหัวใจช้ามักจะกลับมา กลับมาเป็นปกติภายในหนึ่งเดือน
แพทย์ของคุณจะขอให้คุณอยู่ในคลินิกหรือโรงพยาบาลเป็นเวลาอย่างน้อย 6 ชั่วโมงหลังจากให้ยา Gilenya ครั้งแรก ในระหว่างนั้นจะมีการวัดชีพจรและความดันโลหิตของคุณเมื่อใดก็ได้: ด้วยวิธีนี้ สามารถใช้มาตรการที่เหมาะสมได้ ของผลข้างเคียงที่เกิดขึ้นในช่วงเริ่มต้นของการรักษา คุณต้องมีการตรวจคลื่นไฟฟ้าหัวใจก่อนให้ยา Gilenya ครั้งแรกและเมื่อสิ้นสุดการติดตาม 6 ชั่วโมง แพทย์ของคุณอาจตรวจคลื่นไฟฟ้าหัวใจของคุณอย่างต่อเนื่องในช่วงเวลานี้ หากหลังจาก 6 โมง นาฬิกา ชั่วโมง อัตราการเต้นของหัวใจของคุณต่ำมากหรือลดลงหรือหาก EKG ของคุณแสดงความผิดปกติคุณอาจต้องสังเกตเป็นเวลานาน (อย่างน้อยอีก 2 ชั่วโมงและอาจถึงเช้าวันถัดไป) จนกว่าปัญหาเหล่านี้จะได้รับการแก้ไข เช่นเดียวกันอาจเกิดขึ้นได้ถ้าเธอพา G อีกครั้ง ilenya หลังจากการหยุดชะงักของการรักษาขึ้นอยู่กับระยะเวลาของการหยุดชะงักและระยะเวลาที่คุณใช้ Gilenya ก่อนการหยุดชะงัก
หากคุณมีหรือมีความเสี่ยงที่จะหัวใจเต้นผิดปกติหรือผิดปกติ หาก EKG ของคุณผิดปกติ หรือหากคุณเป็นโรคหัวใจหรือหัวใจล้มเหลว Gilenya อาจไม่เหมาะกับคุณ
หากคุณเคยหมดสติกะทันหันหรืออัตราการเต้นของหัวใจลดลง Gilenya อาจไม่เหมาะกับคุณ แพทย์โรคหัวใจ (ผู้เชี่ยวชาญด้านหัวใจ) จะพบคุณ ซึ่งจะแนะนำวิธีเริ่มการรักษากับ Gilenya ให้คุณ รวมถึงการเฝ้าสังเกตจนถึงเช้าวันถัดไป
หากคุณกำลังใช้ยาที่อาจทำให้อัตราการเต้นของหัวใจลดลง Gilenya อาจไม่เหมาะกับคุณ แพทย์โรคหัวใจจะตรวจดูคุณ ซึ่งจะประเมินว่าคุณสามารถใช้ยาที่ไม่ลดอัตราการเต้นของหัวใจเป็นทางเลือกหรือไม่ และอนุญาตให้คุณเริ่มการรักษาด้วย Gilenya ได้ หากไม่สามารถเปลี่ยนแปลงการรักษาได้ แพทย์โรคหัวใจของคุณจะแนะนำวิธีเริ่มการรักษาด้วย Gilenya รวมถึงการเฝ้าสังเกตจนถึงเช้าวันรุ่งขึ้น
หากคุณไม่เคยเป็นโรคอีสุกอีใส: หากคุณไม่เคยเป็นโรคอีสุกอีใส แพทย์จะตรวจภูมิคุ้มกันของคุณต่อไวรัสที่เป็นสาเหตุของโรคนี้ (ไวรัส varicella zoster) หากคุณไม่ได้รับการป้องกันไวรัส คุณอาจต้องฉีดวัคซีนก่อนเริ่มการรักษาด้วย Gilenya หากเกิดเหตุการณ์นี้ขึ้น แพทย์ของคุณจะเลื่อนการเริ่มต้นการรักษา Gilenya ออกไปเป็นเวลาหนึ่งเดือนหลังจากเสร็จสิ้นหลักสูตรการฉีดวัคซีนเต็มรูปแบบ
การติดเชื้อ: Gilenya ลดจำนวนเซลล์เม็ดเลือดขาว (โดยเฉพาะเซลล์เม็ดเลือดขาว) เซลล์เม็ดเลือดขาวต่อสู้กับการติดเชื้อ ขณะรับประทาน Gilenya (และไม่เกิน 2 เดือนหลังจากหยุดการรักษา) คุณอาจติดเชื้อได้ง่ายขึ้น การติดเชื้อที่มีอยู่อาจแย่ลงได้ การติดเชื้ออาจร้ายแรงและเป็นอันตรายถึงชีวิต หากคุณคิดว่าติดเชื้อ มีไข้ มีอาการไข้หวัด หรือปวดศีรษะร่วมกับคอเคล็ด ไวต่อแสง คลื่นไส้และ/หรือสับสน (อาจเป็นอาการของเยื่อหุ้มสมองอักเสบ) ให้ติดต่อ คุณหมอทันที. .
จอประสาทตาบวม: ก่อนเริ่มการรักษาด้วย Gilenya หากคุณมีหรือมีอาการผิดปกติทางสายตาหรือมีอาการอื่นๆ ของอาการบวมที่บริเวณการมองเห็นส่วนกลาง (macula) ที่ด้านหลังตา หากคุณมีหรือเคยมี "การอักเสบหรือ" ที่ตาติดเชื้อ (uveitis) หรือหากคุณเป็นเบาหวาน แพทย์อาจขอให้คุณตรวจตา
แพทย์ของคุณอาจขอให้คุณตรวจตา 3-4 เดือนหลังจากเริ่มการรักษาด้วย Gilenya
จุดภาพชัดคือพื้นที่เล็กๆ ของเรตินาที่อยู่ด้านหลังดวงตาซึ่งช่วยให้คุณเห็นรูปร่าง สี และรายละเอียดได้ชัดเจนและคมชัด Gilenya อาจทำให้เกิดการบวมของจุดภาพชัดซึ่งเป็นภาวะที่เรียกว่า macular edema อาการบวมเกิดขึ้น โดยปกติใน 4 เดือนแรกของการรักษาด้วย Gilenya
อาการบวมน้ำที่จุดภาพมักเกิดขึ้นหากคุณเป็นโรคเบาหวานหรือมี "การอักเสบของดวงตา" ที่เรียกว่าม่านตาอักเสบ ในกรณีเหล่านี้ แพทย์จะต้องการตรวจคุณอย่างสม่ำเสมอเพื่อดูสัญญาณแรกของอาการบวมน้ำที่จุดภาพชัด
หากคุณมีอาการบวมน้ำที่จุดภาพชัด ให้ปรึกษาแพทย์ก่อนเริ่มการรักษาด้วย Gilenya อีกครั้ง
จอประสาทตาบวมอาจทำให้เกิดอาการทางสายตาบางอย่าง (optic neuritis) ที่เกิดขึ้นระหว่างการโจมตีของ MS ได้ ในระยะเริ่มแรกอาจไม่มีอาการใด ๆ อย่าลืมแจ้งให้แพทย์ทราบเกี่ยวกับการเปลี่ยนแปลงการมองเห็นใด ๆ แพทย์ของคุณอาจขอให้คุณอ้างอิง . ได้รับการตรวจตาโดยเฉพาะถ้า:
- พื้นที่รับชมส่วนกลางไม่อยู่ในโฟกัสหรือมีเงา
- จุดบอดพัฒนาในพื้นที่การมองเห็นส่วนกลาง
- มีปัญหาในการแยกแยะสีหรือรายละเอียดปลีกย่อย
การทดสอบการทำงานของตับ: หากคุณมีปัญหาเกี่ยวกับตับอย่างรุนแรง คุณไม่ควรรับประทาน Gilenya การรักษาด้วย Gilenya อาจส่งผลต่อการทำงานของตับ คุณอาจไม่สังเกตเห็นอาการใดๆ แต่ถ้าคุณสังเกตเห็นว่าผิวของคุณหรือตาขาวเป็นสีเหลือง ปัสสาวะสีเข้มผิดปกติ หรือคลื่นไส้และอาเจียนโดยไม่ทราบสาเหตุ ให้แจ้งแพทย์ของคุณทันที
หากคุณมีอาการเหล่านี้หลังจากเริ่มการรักษาด้วย Gilenya โปรดแจ้งให้แพทย์ทราบทันที
ในช่วง 12 เดือนแรกของการรักษา แพทย์ของคุณจะขอให้คุณตรวจเลือดเพื่อตรวจการทำงานของตับ หากผลการศึกษาพบว่ามีปัญหาเกี่ยวกับตับ อาจต้องหยุดการรักษาด้วย Gilenya
ความดันสูง
เนื่องจาก Gilenya ทำให้ความดันโลหิตเพิ่มขึ้นเล็กน้อย แพทย์ของคุณอาจได้รับการตรวจความดันโลหิตของคุณเป็นประจำ ปัญหาปอด Gilenya มีผลอ่อนแอต่อการทำงานของปอด ในผู้ป่วยที่มีปัญหาปอดรุนแรงหรือไอจากการสูบบุหรี่ ผลข้างเคียงอาจเกิดขึ้นได้ง่ายขึ้น
การนับเม็ดเลือด ผลที่ต้องการของการรักษาด้วย Gilenya คือการลดปริมาณเซลล์เม็ดเลือดขาวในเลือด ซึ่งมักจะกลับมาเป็นปกติภายใน 2 เดือนหลังจากหยุดการรักษา หากคุณต้องการตรวจเลือด โปรดแจ้งให้แพทย์ทราบว่าคุณกำลังใช้ Gilenya .
ก่อนเริ่มการรักษาด้วย Gilenya แพทย์ของคุณจะยืนยันว่าจำนวนเม็ดเลือดขาวของคุณเพียงพอหรือไม่ และอาจขอให้คุณนับซ้ำเป็นประจำ หากคุณมีเซลล์เม็ดเลือดขาวไม่เพียงพอ คุณอาจต้องหยุดรับประทาน Gilenya
โรคเอนเซ็ปฟาโลพาทีย้อนกลับหลัง (PRES)
มีรายงานกลุ่มอาการที่เรียกว่าโรคไข้สมองอักเสบจากด้านหลัง (PRES) ในผู้ป่วยโรคปลอกประสาทเสื่อมแข็งที่รักษาด้วย Gilenya น้อยมาก อาการต่างๆ อาจรวมถึงอาการปวดศีรษะรุนแรง สับสน อาการชัก และการมองเห็นเปลี่ยนแปลงไปอย่างฉับพลัน บอกแพทย์หากมีอาการเหล่านี้เกิดขึ้นระหว่างการรักษาด้วย Gilenya
ใช้ในผู้สูงอายุ
ประสบการณ์กับ Gilenya ในผู้ป่วยสูงอายุที่อายุเกิน 65 ปีมีจำกัด หากคุณมีคำถามเพิ่มเติม โปรดปรึกษาแพทย์
เด็กและวัยรุ่น
Gilenya ไม่ได้มีไว้สำหรับใช้ในเด็กและวัยรุ่นที่มีอายุต่ำกว่า 18 ปี เนื่องจากยังไม่มีการศึกษาในผู้ป่วยโรค MS ที่มีอายุต่ำกว่า 18 ปี
ปฏิกิริยา ยาหรืออาหารชนิดใดที่สามารถเปลี่ยนผลของกิเลนยาได้
แจ้งให้แพทย์หรือเภสัชกรทราบ หากคุณกำลังรับประทาน หรือเพิ่งรับประทานยาไปเมื่อเร็วๆ นี้ หรืออาจกำลังใช้ยาอื่นอยู่ บอกแพทย์หากคุณกำลังใช้ยาต่อไปนี้:
- ยาที่กดหรือปรับเปลี่ยนระบบภูมิคุ้มกัน รวมถึงยาอื่นๆ ที่ใช้รักษาโรค MS เช่น interferon beta, glatiramer acetate, natalizumab, mitoxantrone, teriflunomide, dimethyl fumarate หรือ alemtuzumab คุณไม่ควรใช้ Gilenya ร่วมกับยาเหล่านี้ เนื่องจากอาจทำให้ผลต่อระบบภูมิคุ้มกันรุนแรงขึ้น (ดูเพิ่มเติมที่ "Do not Take Gilenya")
- Corticosteroids เนื่องจากอาจมีผลต่อระบบภูมิคุ้มกัน
- วัคซีน. หากคุณต้องการฉีดวัคซีน ควรปรึกษาแพทย์ก่อน ในระหว่างและไม่เกิน 2 เดือนหลังการรักษาด้วย Gilenya คุณไม่ควรรับวัคซีนบางประเภท (วัคซีนลดทอนที่มีชีวิต) เนื่องจากอาจทำให้เกิดการติดเชื้อที่ควรป้องกัน วัคซีนอื่นๆ อาจใช้ไม่ได้ผลตามปกติหากได้รับในขณะนี้ . . .
- ยาที่ทำให้หัวใจเต้นช้าลง (เช่น beta-blockers เช่น atenolol) การใช้ Gilenya ร่วมกับยาเหล่านี้อาจทำให้ผลต่ออัตราการเต้นของหัวใจรุนแรงขึ้นในวันแรกของการรักษา Gilenya
- ยาสำหรับการเต้นของหัวใจผิดปกติ เช่น quinidine, disopyramide, amiodarone หรือ sotalol แพทย์ของคุณอาจตัดสินใจไม่สั่งจ่ายยา Gilenya หากคุณใช้ยาประเภทนี้ เนื่องจากยาเหล่านี้อาจส่งผลรุนแรงต่อการเต้นของหัวใจที่ไม่สม่ำเสมอ
- ยาอื่นๆ:
- สารยับยั้งโปรตีเอส ยาต้านการติดเชื้อ เช่น ketoconazole, azole antifungals, clarithromycin หรือ telithromycin
- carbamazepine, rifampicin, phenobarbital, phenytoin, efavirenz หรือสาโทเซนต์จอห์น (เสี่ยงต่อประสิทธิภาพที่ลดลง)
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
การตั้งครรภ์และให้นมบุตร
ก่อนเริ่มการรักษาด้วย Gilenya แพทย์ของคุณอาจขอให้คุณทำการทดสอบการตั้งครรภ์เพื่อให้แน่ใจว่าคุณไม่ได้ตั้งครรภ์ ขณะรับประทาน Gilenya หรือ 2 เดือนหลังจากหยุดการรักษา คุณควรหลีกเลี่ยงการตั้งครรภ์เนื่องจากอาจมีความเสี่ยงที่จะเกิดอันตรายต่อทารก พูดคุยกับแพทย์ของคุณเกี่ยวกับวิธีการคุมกำเนิดที่เชื่อถือได้เพื่อใช้ในระหว่างการรักษา กับ Gilenya และเป็นเวลา 2 เดือนหลังจากหยุดการรักษา .
หากคุณตั้งครรภ์ขณะรับประทาน Gilenya ให้หยุดการรักษาและแจ้งให้แพทย์ทราบทันที แพทย์ของคุณจะตัดสินใจร่วมกับคุณว่าอะไรดีที่สุดสำหรับคุณและลูกน้อยของคุณ
อย่าให้นมขณะรับประทาน Gilenya Gilenya ถูกขับออกมาในน้ำนมแม่โดยมีความเสี่ยงที่จะเกิดผลข้างเคียงที่ร้ายแรงสำหรับทารกแรกเกิด
ปรึกษาแพทย์หรือเภสัชกรเพื่อขอคำแนะนำก่อนรับประทานยาใดๆ
การขับรถและการใช้เครื่องจักร
แพทย์ของคุณจะบอกคุณว่าความเจ็บป่วยของคุณอนุญาตให้คุณขับรถและใช้เครื่องจักรได้อย่างปลอดภัยหรือไม่ Gilenya ไม่คาดว่าจะส่งผลต่อความสามารถในการขับขี่และการใช้เครื่องจักร
อย่างไรก็ตาม ในช่วงเริ่มต้นของการรักษา คุณจะต้องอยู่ในสำนักงานแพทย์หรือโรงพยาบาลเป็นเวลา 6 ชั่วโมงหลังจากรับประทาน Gilenya ครั้งแรก ความสามารถในการขับและใช้งานเครื่องจักรอาจลดลงในช่วงเวลานี้และในอนาคตข้างหน้า
ปริมาณและวิธีการใช้ วิธีใช้ Gilenya: Dosage
การรักษาด้วย Gilenya จะได้รับการดูแลโดยแพทย์ที่มีประสบการณ์ในการรักษาโรคปลอกประสาทเสื่อมแข็ง
ใช้ยานี้ตามที่แพทย์ของคุณบอกเสมอ
หากมีข้อสงสัย ควรปรึกษาแพทย์ ปริมาณคือหนึ่งแคปซูลวันละครั้ง ใช้ Gilenya วันละครั้งพร้อมกับน้ำหนึ่งแก้ว Gilenya สามารถรับประทานได้ทั้งที่มีหรือไม่มีอาหาร
การรับประทาน Gilenya ในเวลาเดียวกันในแต่ละวันจะช่วยให้คุณจำได้ว่าควรทานยาเมื่อใด
ไม่เกินปริมาณที่แนะนำ
แพทย์ของคุณสามารถเปลี่ยนคุณโดยตรงจากการรักษาด้วย interferon beta, glatiramer acetate หรือ dimethyl fumarate เป็น Gilenya หากไม่มีอาการผิดปกติที่เกิดจากการรักษาก่อนหน้านี้ แพทย์ของคุณอาจให้คุณตรวจเลือดเพื่อแยกแยะความผิดปกติเหล่านี้ หลังจากหยุดใช้ยา natalizumab อาจต้องรอ 2-3 เดือนก่อนเริ่มการรักษาด้วย Gilenya สำหรับการเปลี่ยนจากเทอริฟลูโนไมด์ แพทย์ของคุณอาจแนะนำให้คุณรอเป็นระยะเวลาหนึ่งหรือดำเนินการตามขั้นตอนการกำจัดแบบเร่งด่วน หากคุณได้รับการรักษาด้วย alemtuzumab การประเมินอย่างรอบคอบและปรึกษากับแพทย์ของคุณเป็นสิ่งจำเป็นเพื่อตัดสินใจว่า Gilenya เหมาะกับคุณหรือไม่
หากคุณไม่แน่ใจว่าจะใช้ยา Gilenya นานแค่ไหน ให้ปรึกษาแพทย์หรือเภสัชกรของคุณ
ยาเกินขนาดจะทำอย่างไรถ้าคุณทาน Gilenya มากเกินไป
ถ้าคุณกิน Gilenya มากกว่าที่ควร
หากคุณรับประทานแคปซูล Gilenya มากเกินไป แจ้งให้แพทย์ทราบทันที
หากคุณลืมทาน Gilenya
หากคุณเคยใช้ยา Gilenya มาน้อยกว่า 1 เดือนและลืมรับประทาน 1 โด๊สสำหรับหนึ่งวันเต็ม ให้ปรึกษาแพทย์ก่อนรับประทานยาครั้งต่อไป แพทย์ของคุณอาจตัดสินใจสังเกตคุณเมื่อคุณทานยาครั้งต่อไป
หากคุณเคยใช้ Gilenya มาอย่างน้อย 1 เดือนและลืมกินยาเกิน 2 สัปดาห์แล้ว ให้ปรึกษาแพทย์ก่อนใช้ยาครั้งต่อไป แพทย์ของคุณอาจตัดสินใจสังเกตคุณเมื่อคุณทานยาครั้งต่อไป อย่างไรก็ตาม หากคุณลืมกินยาเป็นเวลา 2 สัปดาห์หรือน้อยกว่านั้น คุณสามารถทานยาครั้งต่อไปได้ตามแผนที่วางไว้
อย่าใช้ยาสองครั้งเพื่อชดเชยปริมาณที่ลืม
หากคุณหยุดทาน Gilenya
อย่าหยุดรับประทาน Gilenya หรือเปลี่ยนขนาดยาโดยไม่ได้ปรึกษาแพทย์ก่อน
Gilenya จะยังคงอยู่ในร่างกายนานถึง 2 เดือนหลังจากหยุดการรักษา จำนวนเซลล์เม็ดเลือดขาว (ลิมโฟไซต์) อาจยังคงต่ำในช่วงเวลานี้ และผลข้างเคียงที่อธิบายไว้ในเอกสารฉบับนี้อาจยังคงเกิดขึ้น หลังจากหยุดการรักษา Gilenya อาจต้องรอ 6-8 สัปดาห์ก่อนเริ่มการรักษาใหม่สำหรับโรคปลอกประสาทเสื่อมแข็ง
หากคุณจำเป็นต้องรีสตาร์ท Gilenya หลังจากหยุดการรักษานานกว่า 2 สัปดาห์ ผลกระทบต่ออัตราการเต้นของหัวใจที่ปกติเกิดขึ้นเมื่อเริ่มการรักษาอาจเกิดขึ้นอีกครั้ง หมอ.
หากคุณมีคำถามเพิ่มเติมเกี่ยวกับการใช้ยานี้ โปรดติดต่อแพทย์หรือเภสัชกร
ผลข้างเคียงของ Gilenya คืออะไร?
เช่นเดียวกับยาอื่น ๆ ยานี้อาจทำให้เกิดผลข้างเคียงได้ แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
ผลข้างเคียงบางอย่างอาจเป็นหรือร้ายแรงได้
สามัญ (อาจส่งผลกระทบมากถึง 1 ใน 10 คน):
- ไอมีเสมหะ เจ็บหน้าอก มีไข้ (สัญญาณของความผิดปกติของปอด)
- การติดเชื้อไวรัสเริม (St. Anthony's fire หรือ herpes zoster) โดยมีอาการต่างๆ เช่น พุพอง แสบร้อน คัน หรือปวดตามผิวหนัง มักอยู่ที่ร่างกายส่วนบนหรือบนใบหน้า อาการอื่นๆ อาจเป็นไข้และอ่อนแรงในระยะแรก . ติดเชื้อ ตามมาด้วยอาการชา คัน หรือจุดแดงปวดอย่างรุนแรง
- หัวใจเต้นช้า (bradycardia), จังหวะการเต้นของหัวใจผิดปกติ
ผิดปกติ (อาจส่งผลกระทบมากถึง 1 ใน 100 คน):
- โรคปอดบวมที่มีอาการ เช่น มีไข้ ไอ หายใจลำบาก
- จอประสาทตาบวม (บวมบริเวณกลางการมองเห็นของเรตินาที่ด้านหลังดวงตา) โดยมีอาการต่างๆ เช่น เงาหรือจุดบอดตรงกลางการมองเห็น ตาพร่ามัว ปัญหาในการแยกแยะสีหรือรายละเอียด
หายาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 คน):
- กลุ่มอาการที่เรียกว่าโรคไข้สมองอักเสบจากด้านหลัง อาการต่างๆ อาจรวมถึงอาการปวดศีรษะรุนแรง สับสน อาการชัก และ/หรือการมองเห็นผิดปกติ
กรณีแยก:
- การติดเชื้อ Cryptococcal (การติดเชื้อราชนิดหนึ่ง) รวมถึงเยื่อหุ้มสมองอักเสบจากเชื้อ cryptococcal ที่มีอาการต่างๆ เช่น ปวดศีรษะร่วมกับคอตึง ไวต่อแสง คลื่นไส้และ/หรือสับสน
หากคุณได้รับผลข้างเคียงเหล่านี้ แจ้งให้แพทย์ทราบทันที
ผลข้างเคียงอื่นๆ
พบบ่อยมาก (อาจส่งผลกระทบมากกว่า 1 ใน 10 คน):
- การติดเชื้อไวรัสไข้หวัดใหญ่ที่มีอาการต่างๆ เช่น เหนื่อยล้า หนาวสั่น เจ็บคอ ปวดข้อหรือกล้ามเนื้อ มีไข้
- รู้สึกกดดันหรือปวดที่แก้มและหน้าผาก (ไซนัสอักเสบ)
- ปวดศีรษะ
- ท้องเสีย
- ปวดหลัง
- การตรวจเลือดแสดงเอนไซม์ตับในระดับที่สูงขึ้น
- ไอ
สามัญ (อาจส่งผลกระทบมากถึง 1 ใน 10 คน):
- กลากเป็น "การติดเชื้อราของผิวหนัง (pityriasis versicolor)
- เวียนหัว
- ปวดหัวอย่างรุนแรง มักมาพร้อมกับอาการคลื่นไส้ อาเจียน และไวต่อแสง (ไมเกรน)
- ระดับเม็ดเลือดขาวต่ำ (เซลล์เม็ดเลือดขาว, เม็ดเลือดขาว)
- ความอ่อนแอ
- ผื่นผิวหนังที่มีอาการคัน แดง และแสบร้อน (กลาก)
- อาการคัน
- เพิ่มระดับไขมัน (ไตรกลีเซอไรด์) ในเลือด
- ผมร่วง
- หายใจดังเสียงฮืด ๆ
- ภาวะซึมเศร้า
- ตาพร่ามัว (ดูหัวข้อ "บวมน้ำ" ผลข้างเคียงบางอย่างอาจเป็นหรือร้ายแรง ")
- ความดันโลหิตสูง (Gilenya อาจทำให้ความดันโลหิตเพิ่มขึ้นเล็กน้อย)
ผิดปกติ (อาจส่งผลกระทบมากถึง 1 ใน 100 คน):
- ระดับต่ำของเม็ดเลือดขาวบางชนิด (นิวโทรฟิล)
- อารมณ์เสีย
หายาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 คน):
- ความผิดปกติของหลอดเลือด
- ความผิดปกติของระบบประสาท
- มะเร็งของระบบน้ำเหลือง (มะเร็งต่อมน้ำเหลือง)
ไม่ทราบ (ความถี่ไม่สามารถประมาณจากข้อมูลที่มีอยู่):
- อาการแพ้และผื่นที่ผิวหนัง
หากมีผลข้างเคียงเหล่านี้เกิดขึ้นอย่างรุนแรง โปรดแจ้งให้แพทย์ทราบ
การรายงานผลข้างเคียง
หากคุณได้รับผลข้างเคียง ให้ปรึกษาแพทย์หรือเภสัชกร ซึ่งรวมถึงผลข้างเคียงที่อาจเกิดขึ้นซึ่งไม่ได้ระบุไว้ในเอกสารฉบับนี้ คุณยังสามารถรายงานผลข้างเคียงได้โดยตรงผ่านระบบการรายงานระดับประเทศที่ระบุไว้ในภาคผนวก 5 โดยการรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
เก็บยานี้ให้พ้นสายตาและมือเด็ก
ห้ามใช้ยานี้หลังจากวันหมดอายุซึ่งระบุไว้บนกล่องและตุ่มหลัง "EXP" / "EXP" วันหมดอายุหมายถึงวันสุดท้ายของเดือนนั้น
อย่าเก็บที่อุณหภูมิสูงกว่า 25 องศาเซลเซียส
เก็บในบรรจุภัณฑ์เดิมเพื่อป้องกันตัวยาจากความชื้น
อย่าใช้บรรจุภัณฑ์ที่เสียหายหรือมีสัญญาณของการปลอมแปลง
ห้ามทิ้งยาลงในน้ำเสียหรือของเสียในครัวเรือน ถามเภสัชกรว่าจะทิ้งยาที่ไม่ได้ใช้แล้วอย่างไร ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
สิ่งที่ Gilenya มี
- สารออกฤทธิ์คือ fingolimod แต่ละแคปซูลประกอบด้วย fingolimod 0.5 มก. (ในรูปของไฮโดรคลอไรด์)
- ส่วนประกอบอื่นๆ ได้แก่ เนื้อหาในแคปซูล: แมกนีเซียม สเตียเรต แมนนิทอล เปลือกแคปซูล: เหล็กออกไซด์สีเหลือง (E172) ไททาเนียมไดออกไซด์ (E171) เจลาติน หมึก: แล็กเกอร์ (E904) แอลกอฮอล์แห้ง ไอโซโพรพิลแอลกอฮอล์ บิวทิลแอลกอฮอล์ โพรพิลีนไกลคอล น้ำบริสุทธิ์ , สารละลายแอมโมเนียเข้มข้น, โพแทสเซียมไฮดรอกไซด์, เหล็กออกไซด์สีดำ (E172), เหล็กออกไซด์สีเหลือง (E172), ไททาเนียมไดออกไซด์ (E171), ไดเมทิโคน
สิ่งที่ Gilenya ดูเหมือนและเนื้อหาของแพ็ค
Gilenya 0.5 มก. แคปซูลแข็งมีตัวทึบแสงสีขาวขุ่นและฝาปิดทึบแสงสีเหลืองเข้ม ตัวหนังสือสีดำ "FTY0,5mg" สลักบนหัว และแถบสีเหลืองสองแถบที่สลักอยู่บนร่างกาย
Gilenya มีจำหน่ายเป็นแพ็คที่มีแคปซูล 7, 28 หรือ 98 แคปซูลหรือในแพ็คหลายที่มี 84 แคปซูล (3 แพ็ค 28 แคปซูล) ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่นำเสนออาจไม่ใช่ข้อมูลล่าสุด
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
GILENYA 0.5 MG ฮาร์ดแคปซูล
▼ ผลิตภัณฑ์ยาอาจมีการตรวจสอบเพิ่มเติม ซึ่งจะช่วยให้ระบุข้อมูลความปลอดภัยใหม่ได้อย่างรวดเร็ว ผู้เชี่ยวชาญด้านการดูแลสุขภาพจะต้องรายงานอาการไม่พึงประสงค์ที่น่าสงสัย ดูหัวข้อ 4.8 สำหรับข้อมูลเกี่ยวกับวิธีการรายงานอาการไม่พึงประสงค์
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
แคปซูลแข็งแต่ละเม็ดประกอบด้วย fingolimod 0.5 มก. (ในรูปของไฮโดรคลอไรด์)
สำหรับรายการสารปรุงแต่งทั้งหมด โปรดดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
ฮาร์ดแคปซูล
แคปซูลขนาด 16 มม. พร้อมฝาทึบแสงสีเหลืองเข้มและตัวทึบแสงสีขาว แกะสลักสีดำ "FTY0.5 มก." บนศีรษะและแถบสีเหลืองสองวงที่แกะสลักบนร่างกาย
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
Gilenya ได้รับการระบุด้วยตัวของมันเองว่าเป็นยาปรับเปลี่ยนโรคในกลุ่มผู้ป่วยที่เป็นผู้ใหญ่ต่อไปนี้:
- ผู้ป่วยที่มีกิจกรรมโรคสูงแม้จะได้รับการรักษาด้วยการบำบัดอย่างน้อยหนึ่งครั้ง การปรับเปลี่ยนโรค (ดูหัวข้อ 4.4 และ 5.1 สำหรับข้อยกเว้นและข้อมูลเกี่ยวกับ ชะล้าง).
ผู้ป่วยเหล่านี้สามารถกำหนดได้ว่าเป็นผู้ที่ไม่ตอบสนองต่อการรักษาที่สมบูรณ์และเพียงพอ (โดยปกติคืออย่างน้อยหนึ่งปีของการรักษา) ด้วยการบำบัดอย่างน้อยหนึ่งครั้ง การปรับเปลี่ยนโรค. ผู้ป่วยต้องมีอาการกำเริบอย่างน้อย 1 ครั้งในปีที่แล้วในขณะที่ทำการรักษาและมีอย่างน้อย 9 T2 hyperintense lesions ใน MRI ของสมองหรืออย่างน้อย 1 gadolinium-enhancing lesion ไม่ตอบสนอง นอกจากนี้ยังสามารถกำหนดเป็นผู้ป่วยที่มีอัตราการกำเริบของโรคไม่เปลี่ยนแปลงหรือเพิ่มขึ้นเมื่อเทียบกับปีที่แล้วหรือผู้ที่มีอาการกำเริบรุนแรง
หรือ
- ผู้ป่วยที่มีอาการกำเริบอย่างรุนแรง-ส่งกลับหลายเส้นโลหิตตีบ กำหนดโดยอาการกำเริบที่ทำให้ทุพพลภาพสองคนขึ้นไปในหนึ่งปี และมีรอยโรคที่สร้างแกโดลิเนียมใน MRI ของสมองอย่างน้อย 1 รอยหรือมีภาระ T2 เพิ่มขึ้นอย่างมีนัยสำคัญเมื่อเทียบกับ MRI ก่อนหน้าเมื่อเร็วๆ นี้ ดำเนินการ.
04.2 วิทยาและวิธีการบริหาร
การรักษาควรเริ่มต้นและดูแลโดยแพทย์ที่มีประสบการณ์ในโรคปลอกประสาทเสื่อมแข็ง
ปริมาณ
ปริมาณที่แนะนำของ Gilenya คือหนึ่งแคปซูล 0.5 มก. รับประทานวันละครั้ง Gilenya สามารถรับประทานได้ทั้งระหว่างและนอกมื้ออาหาร
ขอแนะนำให้ทำการตรวจสอบเช่นเดียวกับเมื่อเริ่มการรักษาหลังจากให้ยาครั้งแรกหากหยุดการรักษาสำหรับ:
• 1 วันขึ้นไปในช่วงสองสัปดาห์แรกของการรักษา
• มากกว่า 7 วันในสัปดาห์ที่สามและสี่ของการรักษา
• มากกว่า 2 สัปดาห์หลังการรักษา 1 เดือน
หากการหยุดชะงักของการรักษามีระยะเวลาสั้นกว่าที่อธิบายไว้ข้างต้น การรักษาควรดำเนินต่อไปโดยให้ยาครั้งต่อไปตามที่วางแผนไว้ (ดูหัวข้อ 4.4)
ประชากรพิเศษ
พลเมืองอาวุโส
Gilenya ควรใช้ด้วยความระมัดระวังในผู้ป่วยอายุ 65 ปีขึ้นไป เนื่องจากมีข้อมูลความปลอดภัยและประสิทธิภาพไม่เพียงพอ (ดูหัวข้อ 5.2)
การทำงานของไตบกพร่อง
ในการศึกษาการพิจาณาหลักที่ดำเนินการในหลายเส้นโลหิตตีบ Gilenya ไม่ได้รับการศึกษาในผู้ป่วยที่มีความบกพร่องทางไต จากการศึกษาทางเภสัชวิทยาทางคลินิก ไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยที่มีภาวะไตวายเล็กน้อยถึงรุนแรง
การทำงานของตับบกพร่อง
ไม่ควรใช้ Gilenya ในผู้ป่วยที่มีความบกพร่องทางตับอย่างรุนแรง (Child-Pugh class C) (ดูหัวข้อ 4.3) แม้ว่าจะไม่มีการปรับขนาดยาในผู้ป่วยที่มีความบกพร่องทางตับในระดับเล็กน้อยหรือปานกลาง ขอแนะนำให้ใช้ความระมัดระวังเมื่อเริ่มการรักษาในผู้ป่วยเหล่านี้ (ดูหัวข้อ 4.4 และ 5.2)
ผู้ป่วยเบาหวาน
Gilenya ไม่ได้รับการศึกษาในผู้ป่วยโรคปลอกประสาทเสื่อมแข็งและเบาหวาน Gilenya ควรใช้ด้วยความระมัดระวังในผู้ป่วยเหล่านี้เนื่องจากมีความเสี่ยงที่จะเกิด macular edema เพิ่มขึ้น (ดูหัวข้อ 4.4 และ 4.8) ผู้ป่วยเหล่านี้ควรได้รับการตรวจทางจักษุวิทยาเป็นประจำเพื่อดูว่ามีอาการบวมน้ำหรือไม่
ประชากรเด็ก
ความปลอดภัยและประสิทธิภาพของ Gilenya ในเด็กอายุ 0-18 ปียังไม่ได้รับการจัดตั้งขึ้น ข้อมูลที่มีอยู่ในปัจจุบันได้อธิบายไว้ในหัวข้อ 5.2 แต่ไม่สามารถให้คำแนะนำเกี่ยวกับ posology ได้
04.3 ข้อห้าม
- วินิจฉัยโรคภูมิคุ้มกันบกพร่อง
- ผู้ป่วยที่มีความเสี่ยงในการติดเชื้อฉวยโอกาสเพิ่มขึ้น รวมถึงผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่อง (รวมถึงผู้ที่รับการรักษาด้วยยากดภูมิคุ้มกันร่วม หรือผู้ที่ภูมิคุ้มกันบกพร่องจากการรักษาครั้งก่อน)
- การติดเชื้อรุนแรง, การติดเชื้อเรื้อรัง (ตับอักเสบ, วัณโรค)
- ตรวจพบเนื้องอกมะเร็งที่ออกฤทธิ์ ยกเว้นผู้ป่วยที่เป็นมะเร็งผิวหนังจากเซลล์ต้นกำเนิด
- การด้อยค่าของตับอย่างรุนแรง (Child-Pugh class C)
- ภูมิไวเกินต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อ 6.1
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
Bradyarrhythmia
การเริ่มต้นของการรักษา Gilenya ส่งผลให้อัตราการเต้นของหัวใจลดลงชั่วคราวและอาจเกี่ยวข้องกับความล่าช้าในการนำ atrioventricular ซึ่งรวมถึงตอนที่แยกได้ของการเกิด atrioventricular block ที่สมบูรณ์ ชั่วคราว และเกิดขึ้นเองตามธรรมชาติ (ดูหัวข้อ 4.8 และ 5.1)
หลังจากการให้ยาครั้งแรก อัตราการเต้นของหัวใจจะลดลงภายในหนึ่งชั่วโมงและสูงสุดภายใน 6 ชั่วโมงแรก ในวันต่อๆ ไป ผลกระทบหลังการให้ยานี้ยังคงมีอยู่แม้ว่าโดยทั่วไปจะมีความรุนแรงน้อยกว่าและมักจะลดลงในช่วงสัปดาห์ต่อๆ ไป . . เมื่อให้การรักษาอย่างต่อเนื่อง อัตราการเต้นของหัวใจเฉลี่ยจะกลับสู่การตรวจวัดพื้นฐานภายในหนึ่งเดือน อย่างไรก็ตาม ในผู้ป่วยโดยเฉพาะ อัตราการเต้นของหัวใจอาจไม่กลับสู่การตรวจวัดพื้นฐานภายในสิ้นเดือนแรก ความผิดปกติของการนำไฟฟ้ามักจะเกิดขึ้นชั่วคราวและไม่มีอาการ โดยทั่วไปไม่จำเป็นต้อง และแก้ไขได้ภายใน 24 ชั่วโมงแรกของการรักษา หากจำเป็น การลดอัตราการเต้นของหัวใจที่เกิดจาก fingolimod สามารถย้อนกลับได้โดยการให้ยา atropine หรือ isoprenaline ทางหลอดเลือด
ผู้ป่วยทุกรายควรได้รับการตรวจวัดคลื่นไฟฟ้าหัวใจและความดันโลหิตก่อนให้ยา Gilenya ครั้งแรกและหลังจากผ่านไป 6 ชั่วโมง ผู้ป่วยทุกรายควรได้รับการตรวจสอบเป็นเวลา 6 ชั่วโมงเพื่อดูอาการและอาการแสดงของหัวใจเต้นช้าด้วยการวัดอัตราการเต้นของหัวใจรายชั่วโมงและความดันโลหิต แนะนำให้ติดตาม ECG แบบต่อเนื่อง (เรียลไทม์) ในช่วง 6 ชั่วโมงนี้ .
หากมีอาการ bradyarrhythmia เกิดขึ้นหลังการให้ยา ควรเริ่มขั้นตอนการจัดการผู้ป่วยทางคลินิกที่เหมาะสมและติดตามดูต่อไปจนกว่าอาการจะหาย หากผู้ป่วยต้องการการแทรกแซงทางเภสัชวิทยาระหว่างการตรวจติดตามหลังการให้ยาครั้งแรก ควรติดตามจนถึงเช้าวันรุ่งขึ้นในสถานพยาบาลในโรงพยาบาล และควรทำซ้ำหลังจากรับประทานยา Gilenya ครั้งที่สอง
หากเมื่อสิ้นสุด 6 ชั่วโมง ค่าอัตราการเต้นของหัวใจจะต่ำที่สุดหลังจากให้ยาครั้งแรก (แนะนำว่าอาจยังไม่ปรากฏผลทางเภสัชพลศาสตร์สูงสุดต่อหัวใจ) ควรติดตามต่อไปอย่างน้อย 2 ชั่วโมงและจนกว่าหัวใจ อัตราเพิ่มขึ้นอีกครั้ง จำเป็นต้องมีการตรวจสอบเพิ่มเติม (อย่างน้อยจนถึงเช้าวันถัดไปและในกรณีใด ๆ จนกว่าอาการจะได้รับการแก้ไข) ถ้าหลังจาก 6 ชั่วโมงนับจากการให้ยาครั้งแรกอัตราการเต้นของหัวใจจะเต้นต่อนาที หรือถ้า คลื่นไฟฟ้าหัวใจแสดงการโจมตีใหม่ระดับที่สองหรือสูงกว่าบล็อก atrioventricular หรือถ้าช่วง QTc คือ≥500 msec การโจมตีของบล็อก atrioventricular ระดับที่สามเมื่อใดก็ได้จะต้องนำไปสู่การขยายการตรวจสอบ (อย่างน้อยจนถึงเช้าวันรุ่งขึ้น)
เนื่องจากความเสี่ยงของจังหวะการเต้นของหัวใจอย่างรุนแรง ไม่ควรใช้ Gilenya ในผู้ป่วยที่มีระดับที่สอง Mobitz type II หรือบล็อก atrioventricular สูงกว่า ในผู้ป่วยที่มีอาการไซนัสป่วยหรือ sino-atrial block ประวัติของอาการหัวใจเต้นช้าหรือเป็นลมหมดสติ หรือในผู้ป่วย ด้วยการยืด QT อย่างมีนัยสำคัญ (QTc> 470 msec (ผู้หญิง) หรือ> 450 msec (ผู้ชาย)) เนื่องจากหัวใจเต้นช้าที่มีนัยสำคัญอาจทนได้ไม่ดีในผู้ป่วยโรคหัวใจขาดเลือดที่รู้จักกันดี (รวมถึงโรคหลอดเลือดหัวใจตีบ), โรคหลอดเลือดสมอง, ประวัติของกล้ามเนื้อหัวใจตาย, หัวใจล้มเหลว, ประวัติของภาวะหัวใจหยุดเต้น, ความดันโลหิตสูงที่ไม่สามารถควบคุมได้หรือภาวะหยุดหายใจขณะหลับอย่างรุนแรง Gilenya ไม่ควรใช้ใน ผู้ป่วยเหล่านี้ การรักษาด้วย Gilenya ควรได้รับการพิจารณาเฉพาะในผู้ป่วยเหล่านี้หากผลประโยชน์ที่คาดหวังมีมากกว่าความเสี่ยงที่อาจเกิดขึ้น หากตัดสินใจเริ่มการรักษาด้วย Gilenya ควรปรึกษาแพทย์โรคหัวใจก่อนเริ่มการรักษาเพื่อกำหนดการติดตามผลที่เหมาะสมที่สุด แนะนำให้ติดตามอย่างน้อยจนถึงเช้าวันถัดไปเพื่อเริ่มการรักษา (ดูหัวข้อ 4.5)
Gilenya ไม่ได้รับการศึกษาในผู้ป่วยที่มีภาวะหัวใจเต้นผิดจังหวะที่ต้องได้รับการรักษาด้วยคลาส Ia (เช่น quinidine, disopyramide) หรือคลาส III (เช่น amiodarone, sotalol) antiarrhythmics ยาต้านการเต้นของหัวใจคลาส Ia และคลาส III มีความเกี่ยวข้องกับกรณีของ torsades de pointes ในผู้ป่วยหัวใจเต้นช้า เนื่องจากการเริ่มต้นการรักษาด้วย Gilenya ส่งผลให้อัตราการเต้นของหัวใจลดลง จึงไม่ควรใช้ Gilenya ควบคู่ไปกับยาเหล่านี้
ประสบการณ์กับ Gilenya ในผู้ป่วยที่รักษาร่วมกับ beta-blockers, calcium channel blockers ที่ทำให้อัตราการเต้นของหัวใจลดลง (เช่น verapamil, diltiazem หรือ ivabradine) หรือยาอื่นๆ ที่อาจลดอัตราการเต้นของหัวใจ (เช่น digoxin ยา anticholinesterase หรือ pilocarpine ) มีจำนวนจำกัดเนื่องจากการเริ่มต้นของการรักษาด้วย Gilenya นั้นสัมพันธ์กับอัตราการเต้นของหัวใจที่ลดลง (ดูเพิ่มเติมในหัวข้อ 4.8 Bradyarrhythmia) การใช้ยาเหล่านี้ร่วมกันในช่วงเริ่มต้นของการรักษา Gilenya อาจเกี่ยวข้องกับภาวะหัวใจเต้นช้าและภาวะหัวใจล้มเหลวอย่างรุนแรง เนื่องจากอาจมีผลต่ออัตราการเต้นของหัวใจ ไม่ควรเริ่มการรักษาด้วย Gilenya ในผู้ป่วยที่ได้รับยาเหล่านี้ (ดูหัวข้อ 4.5) การรักษาด้วย Gilenya ควรพิจารณาเฉพาะในผู้ป่วยเหล่านี้หากผลประโยชน์ที่คาดหวังมีมากกว่าความเสี่ยง ปรึกษาก่อนเริ่มการรักษาเพื่อพิจารณาเปลี่ยนไปใช้ยาอื่นที่ไม่ทำให้อัตราการเต้นของหัวใจลดลง ควรปรึกษาแพทย์โรคหัวใจเพื่อกำหนดการตรวจติดตามให้เพียงพอตั้งแต่เริ่มต้น ของการรักษา แนะนำให้ติดตามอย่างน้อยก็จนถึงเช้าวันถัดไป (ดูหัวข้อ 4.5 ด้วย)
ขึ้นอยู่กับระยะเวลาของการหยุดชะงักและระยะเวลาของการรักษา (เวลาระหว่างการเริ่มต้นการรักษาและการหยุดการรักษา) ผลต่ออัตราการเต้นของหัวใจและการนำ atrioventricular อาจกลับมาเมื่อเริ่มการรักษาด้วย Gilenya ขอแนะนำให้ทำการตรวจสอบเช่นเดียวกับเมื่อเริ่มการรักษาหลังจากให้ยาครั้งแรกหากหยุดการรักษาสำหรับ:
• 1 วันขึ้นไปในช่วงสองสัปดาห์แรกของการรักษา
• มากกว่า 7 วันในสัปดาห์ที่สามและสี่ของการรักษา
• มากกว่า 2 สัปดาห์หลังการรักษา 1 เดือน
หากการหยุดชะงักของการรักษามีระยะเวลาสั้นกว่าที่อธิบายไว้ข้างต้น การรักษาควรดำเนินต่อไปโดยให้ยาครั้งต่อไปตามที่วางแผนไว้
ช่วง QT
ในการศึกษาช่วง QT อย่างละเอียดที่ดำเนินการด้วยขนาดยา fingolimod 1.25 มก. หรือ 2.5 มก. ที่สภาวะคงตัว (เมื่อยังคงมีผล chronotropic เชิงลบของ fingolimod) การรักษาด้วย fingolimod ทำให้เกิดการยืดขนาดยา แก้ไขช่วง QT (QTc) ด้วย ขีดจำกัดบนของช่วงความเชื่อมั่น 90% ≤ 13.0 ms ไม่พบความสัมพันธ์ระหว่างปริมาณยากับการตอบสนองต่อการสัมผัสหรือการตอบสนองต่อการสัมผัสระหว่างการยืดเวลาของ fingolimod และ QTc ทั้งในรูปแบบค่าสัมบูรณ์หรือการเปลี่ยนแปลงจากการตรวจวัดพื้นฐาน
ความสำคัญทางคลินิกของการค้นพบนี้ไม่เป็นที่รู้จัก ไม่พบการยืดช่วง QT อย่างมีนัยสำคัญทางคลินิกในการศึกษาในผู้ป่วยโรคปลอกประสาทเสื่อมแข็ง แต่ผู้ป่วยที่มีความเสี่ยงต่อการเกิดการขยายช่วง QT ไม่รวมอยู่ในการทดลองทางคลินิก
ควรหลีกเลี่ยงผลิตภัณฑ์ยาที่สามารถยืดช่วง QTc ในผู้ป่วยที่มีปัจจัยเสี่ยงที่สำคัญ เช่น ภาวะโพแทสเซียมในเลือดต่ำ หรือการยืดช่วง QT ที่มีมา แต่กำเนิด
การติดเชื้อ
ผลทางเภสัชพลศาสตร์ที่เกี่ยวข้องของ Gilenya คือการลดจำนวนเซลล์เม็ดเลือดขาวส่วนปลายโดยขึ้นกับขนาดยาเป็น 20-30% ของค่าพื้นฐาน นี่เป็นเพราะการรวมตัวของลิมโฟไซต์ในเนื้อเยื่อน้ำเหลืองแบบย้อนกลับได้ (ดูหัวข้อ 5.1)
ควรมีการตรวจนับเม็ดเลือดโดยสมบูรณ์ (เช่น ถ่ายภายใน 6 เดือนก่อนหรือหลังหยุดการรักษาก่อนหน้านี้) ก่อนเริ่มการรักษาด้วย Gilenya ในระหว่างการรักษา ขอแนะนำให้ประเมินการนับเม็ดเลือดเป็นระยะหลังจาก 3 เดือนและอย่างน้อยทุกปีหลังจากนั้น และในกรณีที่เริ่มมีอาการของการติดเชื้อ ควรนับจำนวนเม็ดเลือดขาวที่ต่ำกว่า 0.2x109 / l หากได้รับการยืนยัน การรักษาจนถึง กลับสู่ภาวะปกติ เนื่องจาก fingolimod ถูกยกเลิกในการทดลองทางคลินิกในผู้ป่วยที่มีจำนวนเม็ดเลือดขาวต่ำกว่า 0.2x109 / l
การเริ่มต้นของการรักษาด้วย Gilenya ควรถูกเลื่อนออกไปในผู้ป่วยที่มีการติดเชื้อรุนแรงอย่างต่อเนื่องจนกว่าจะหายดี
ผู้ป่วยควรได้รับการประเมินสถานะภูมิคุ้มกันโรคอีสุกอีใสก่อนเริ่มการรักษาด้วย Gilenya ในกรณีที่ไม่มีประวัติที่ได้รับการยืนยันจากแพทย์ว่าเป็นโรคอีสุกอีใสหรือหลักฐานของหลักสูตรการฉีดวัคซีน varicella อย่างสมบูรณ์ ขอแนะนำให้ผู้ป่วยได้รับการทดสอบหาแอนติบอดีต่อไวรัส varicella-zoster (VZV) ก่อนเริ่มการรักษาด้วย Gilenya สำหรับผู้ป่วยที่มีระดับแอนติบอดีเชิงลบ แนะนำให้ฉีดวัคซีนป้องกัน varicella อย่างครบถ้วนก่อนเริ่มการรักษาด้วย Gilenya (ดูหัวข้อ 4.8) การเริ่มต้นการรักษาด้วย Gilenya ควรเลื่อนออกไป 1 เดือนเพื่อให้การฉีดวัคซีนมีประสิทธิภาพเต็มที่
ผลของ Gilenya ต่อระบบภูมิคุ้มกันอาจเพิ่มความเสี่ยงของการติดเชื้อ (ดูหัวข้อ 4.8) ควรใช้กลยุทธ์การวินิจฉัยและการรักษาที่มีประสิทธิภาพในผู้ป่วยที่ได้รับการรักษาด้วย Gilenya ที่มีอาการของการติดเชื้อ ผู้ป่วยควรได้รับคำแนะนำให้รายงานอาการติดเชื้อกับแพทย์ระหว่างการรักษาด้วย Gilenya
หากผู้ป่วยมีการติดเชื้อรุนแรง ควรพิจารณาหยุดการรักษาด้วย Gilenya และควรประเมินความสมดุลระหว่างผลประโยชน์และความเสี่ยงก่อนเริ่มการรักษาต่อ
การกำจัด fingolimod หลังจากหยุดการรักษาอาจใช้เวลานานถึงสองเดือน ดังนั้นการควบคุมการติดเชื้อจึงควรคงอยู่ในช่วงเวลานี้ ผู้ป่วยควรได้รับคำแนะนำให้รายงานอาการติดเชื้อภายในสองเดือนหลังจากหยุดยา fingolimod
จอประสาทตาบวมน้ำ
พบอาการบวมน้ำที่จุดภาพชัดที่มีหรือไม่มีการรบกวนทางสายตาในผู้ป่วย 0.5% ที่ได้รับการรักษาด้วย fingolimod 0.5 มก. ส่วนใหญ่ในช่วง 3-4 เดือนแรกของการรักษา (ดูหัวข้อ 4.8) ดังนั้นจึงแนะนำให้ทำการประเมินทางจักษุวิทยาหลังจากเริ่มการรักษาประมาณ 3-4 เดือน หากผู้ป่วยรายงานการรบกวนทางสายตาเมื่อใดก็ได้ในระหว่างการรักษา ควรทำการตรวจจอตา รวมทั้งจุดภาพชัดด้วย
ผู้ป่วยที่มีประวัติเกี่ยวกับม่านตาอักเสบและผู้ป่วยโรคเบาหวานมีความเสี่ยงที่จะเกิดจุดภาพชัดบวมน้ำมากขึ้น (ดูหัวข้อ 4.8) Gilenya ไม่ได้รับการศึกษาในผู้ป่วยโรคปลอกประสาทเสื่อมแข็งและเบาหวานร่วม ขอแนะนำว่าผู้ป่วยโรคปลอกประสาทเสื่อมแข็งและเบาหวานร่วม หรือมีประวัติเป็นโรคม่านตาอักเสบ ให้เข้ารับการประเมินทางจักษุวิทยาก่อนเริ่มการรักษาและตรวจติดตามผลระหว่างการรักษา
ยังไม่มีการศึกษาความต่อเนื่องของการรักษา Gilenya ในผู้ป่วยที่มีอาการบวมน้ำที่จุดภาพชัด ขอแนะนำให้หยุดการรักษา Gilenya หากเกิดอาการบวมน้ำที่จุดภาพชัดในผู้ป่วย ในการตัดสินใจว่าควรให้การรักษาด้วย Gilenya กลับมาใช้ใหม่หรือไม่หลังการรักษา ควรพิจารณาถึงประโยชน์และความเสี่ยงที่อาจเกิดขึ้นกับผู้ป่วยแต่ละราย
การทำงานของตับ
การเพิ่มขึ้นของเอนไซม์ตับ โดยเฉพาะ alanine aminotransferase (ALT) แต่ยังมี gamma glutamyltranspeptidase (GGT) และ aspartate transaminase (AST) ในผู้ป่วยโรคปลอกประสาทเสื่อมแข็งที่รักษาด้วย Gilenya ในการทดลองทางคลินิก ALT สูงขึ้น≥3เท่าของขีด จำกัด บนของช่วงปกติ (ULN) เกิดขึ้นใน 8.0% ของผู้ป่วยที่ได้รับ fingolimod 0.5 มก. เทียบกับ 1.9% ของผู้ป่วยที่ได้รับยาหลอก . เพิ่มขึ้น 5 เท่าของขีด จำกัด บนของช่วงปกติ เกิดขึ้นในผู้ป่วย 1.8% ที่ได้รับ fingolimod และ 0.9% ของผู้ป่วยที่ได้รับยาหลอก ในการทดลองทางคลินิก การรักษาด้วย fingolimod ถูกยกเลิกหากการเพิ่มขึ้น> 5 เท่าของขีดจำกัดบนของช่วงปกติ ในผู้ป่วยบางรายที่ได้รับการรักษาซ้ำหลังจากหยุดยา ระดับเอนไซม์ตับ transaminase เกิดขึ้นอีกครั้ง เพื่อยืนยันความสัมพันธ์ระหว่างการเพิ่มขึ้นนี้กับยา ในการศึกษาทางคลินิก ระดับเอนไซม์ตับ transaminases เกิดขึ้นตลอดเวลาระหว่างการรักษา แม้ว่าส่วนใหญ่เกิดขึ้นในช่วง 12 เดือนแรก ระดับ transaminase ในเลือดกลับมาเป็นปกติประมาณ 2 เดือนหลังจากหยุด fingolimod
Gilenya ยังไม่ได้รับการศึกษาในผู้ป่วยที่มีความบกพร่องทางตับอย่างรุนแรง (Child-Pugh class C) มาก่อน ดังนั้นจึงไม่ควรใช้ในผู้ป่วยเหล่านี้ (ดูหัวข้อ 4.3)
เนื่องจากคุณสมบัติทางภูมิคุ้มกันของ fingolimod การรักษาควรล่าช้าในผู้ป่วยที่เป็นโรคตับอักเสบจากเชื้อไวรัส จนกว่าระยะที่ออกฤทธิ์จะคลี่คลายลง
ควรมีการวิเคราะห์ล่าสุด (เช่น ภายใน 6 เดือนก่อนหน้า) ของระดับ transaminase และ bilirubin ก่อนเริ่มการรักษาด้วย Gilenya ในกรณีที่ไม่มีอาการทางคลินิก ควรตรวจสอบระดับ transaminase ของตับหลังจาก 1, 3, 6, 9 และ 12 เดือน ของการรักษาและเป็นระยะหลังจากนั้น หากระดับ transaminase ตับมีค่ามากกว่า 5 เท่าของค่าปกติ (ULN) ควรมีการตรวจสอบบ่อยขึ้นรวมถึงการตรวจระดับบิลิรูบินในซีรัมและอัลคาไลน์ฟอสฟาเตส ( ALP)หากหลังจากตรวจสอบซ้ำแล้วซ้ำอีกค่า transaminase ตับยังคงอยู่มากกว่า 5 เท่าของค่าปกติ (ULN) การรักษาด้วย Gilenya ควรถูกขัดจังหวะและเริ่มต้นใหม่เฉพาะเมื่อค่า transaminase ตับกลับมาเป็นปกติ
ในผู้ป่วยที่มีอาการตับทำงานผิดปกติ เช่น คลื่นไส้ อาเจียน ปวดท้อง อ่อนเพลีย เบื่ออาหาร ตัวเหลือง และ/หรือปัสสาวะสีเข้ม โดยไม่ทราบสาเหตุ ควรมีการประเมินระดับเอนไซม์ในตับ หากได้รับการยืนยันว่าได้รับบาดเจ็บที่ตับอย่างมีนัยสำคัญ (เช่น ระดับ transaminase ตับเกินขีด จำกัด สูงสุดของช่วงปกติมากกว่า 5 เท่าและ / หรือระดับบิลิรูบินในซีรัมเพิ่มขึ้น) ควรหยุดการรักษาด้วย Gilenya การเริ่มต้นใหม่ของการรักษาจะขึ้นอยู่กับว่ามีการระบุสาเหตุอื่นของการบาดเจ็บที่ตับหรือไม่ และผลประโยชน์ของผู้ป่วยในการกลับมารักษาต่อกับความเสี่ยงของความผิดปกติของตับที่เกิดขึ้นซ้ำ
แม้ว่าจะไม่มีข้อมูลที่ระบุว่าผู้ป่วยโรคตับที่มีอยู่ก่อนมีความเสี่ยงเพิ่มขึ้นในการพัฒนาการทดสอบการทำงานของตับในระดับสูง แต่ควรใช้ความระมัดระวังในการบริหาร Gilenya ให้กับผู้ป่วยที่มีประวัติโรคตับที่มีนัยสำคัญ
รบกวนการตรวจซีรัมวิทยา
เนื่องจาก fingolimod ช่วยลดจำนวนเม็ดเลือดขาวในเลือดโดยการแจกจ่ายไปยังอวัยวะน้ำเหลืองทุติยภูมิ จึงไม่สามารถใช้ประเมินสถานะลิมโฟไซต์ของผู้ป่วยที่รักษาด้วย Gilenya ได้ การทดสอบในห้องปฏิบัติการที่เกี่ยวข้องกับการใช้เซลล์โมโนนิวเคลียร์แบบหมุนเวียนนั้นต้องการปริมาณเลือดที่สูงขึ้นเนื่องจากการลดจำนวนเซลล์เม็ดเลือดขาวที่ไหลเวียน
ผลต่อความดันโลหิต
ผู้ป่วยที่เป็นโรคความดันโลหิตสูงที่ไม่ได้ควบคุมด้วยยาได้รับการยกเว้นจากการทดลองทางคลินิกก่อนการตลาดของ Gilenya; ดังนั้นจึงควรให้ความสนใจเป็นพิเศษหากผู้ป่วยโรคความดันโลหิตสูงที่ไม่สามารถควบคุมได้ได้รับการรักษาด้วย Gilenya
ในการศึกษาทางคลินิกในผู้ป่วยโรคปลอกประสาทเสื่อมแข็ง การรักษาด้วย fingolimod 0.5 มก. มีความสัมพันธ์กับความดันโลหิตตัวล่างเฉลี่ยประมาณ 3 mmHg และความดันโลหิตตัวล่างประมาณ 1 mmHg: การเพิ่มขึ้นเหล่านี้เกิดขึ้นประมาณ 1 เดือนต่อมา การเริ่มต้นการรักษาและยังคงอยู่กับ การรักษาต่อ ในการศึกษาที่ควบคุมด้วยยาหลอกเป็นเวลา 2 ปี ความดันโลหิตสูงถูกรายงานว่าเป็นเหตุการณ์ไม่พึงประสงค์ใน 6.5% ของผู้ป่วยที่ได้รับยา Gilenya 0.5 มก. และ 3.3% ของผู้ป่วยที่ได้รับยาหลอก ดังนั้นความดันโลหิตของคุณควรได้รับการตรวจสอบอย่างสม่ำเสมอในระหว่างการรักษาด้วย Gilenya
ผลต่อระบบทางเดินหายใจ
การลดลงของปริมาณการหายใจที่ถูกบังคับ (FEV1) และความสามารถในการแพร่ของคาร์บอนมอนอกไซด์ (Dlco) ขึ้นอยู่กับขนาดยาเล็กน้อยถูกสังเกตระหว่างการรักษาด้วย Gilenya การลดลงที่เกิดขึ้นในเดือนแรกและยังคงทรงตัวตลอดการรักษา Gilenya ควรใช้ด้วยความระมัดระวังในผู้ป่วยที่มีความผิดปกติของระบบทางเดินหายใจอย่างรุนแรง พังผืดในปอด และโรคปอดอุดกั้นเรื้อรัง (ดูหัวข้อ 4.8)
โรคเอนเซ็ปฟาโลพาทีแบบย้อนกลับหลัง
มีรายงานกรณีที่ไม่ค่อยพบของโรคสมองจากสมองที่กลับคืนมา (PRES) ในการทดลองทางคลินิกและประสบการณ์หลังการขายยาด้วยขนาดยา 0.5 มก. (ดูหัวข้อ 4.8) อาการที่รายงาน ได้แก่ อาการปวดศีรษะรุนแรง คลื่นไส้ อาเจียน สถานะทางจิตที่เปลี่ยนแปลงไป การรบกวนและอาการชัก อาการของ PRES มักจะย้อนกลับได้ แต่สามารถพัฒนาไปสู่โรคหลอดเลือดสมองตีบหรือเลือดออกในสมองได้ การวินิจฉัยและการรักษาล่าช้าอาจนำไปสู่ผลที่ตามมาทางระบบประสาทอย่างถาวร หากสงสัยว่ามี PRES ควรยุติการรักษาด้วย Gilenya
การรักษาก่อนหน้าด้วยการบำบัดด้วยภูมิคุ้มกันหรือการบำบัดด้วยภูมิคุ้มกัน
ไม่มีการศึกษาเพื่อประเมินประสิทธิภาพและความปลอดภัยของ Gilenya เมื่อผู้ป่วยเปลี่ยนจาก teriflunomide, dimethyl fumarate หรือ alemtuzumab เป็น Gilenya เมื่อผู้ป่วยเปลี่ยนจากการรักษาแบบอื่น การปรับเปลี่ยนโรค ใน Gilenya ต้องคำนึงถึงครึ่งชีวิตและกลไกการทำงานของการรักษาอื่น ๆ เพื่อหลีกเลี่ยงผลกระทบเพิ่มเติมต่อระบบภูมิคุ้มกันและในขณะเดียวกันก็ลดความเสี่ยงของการเปิดใช้งานของโรคอีกครั้ง ขอแนะนำให้ประเมิน การนับเม็ดเลือดโดยสมบูรณ์ก่อนเริ่มการรักษาด้วย Gilenya เพื่อให้แน่ใจว่าผลกระทบต่อระบบภูมิคุ้มกันที่เกิดจากการรักษาครั้งก่อน (เช่น cytopenia) ได้รับการแก้ไขแล้ว
โดยทั่วไปแล้วการรักษา Gilenya สามารถเริ่มได้ทันทีหลังจากหยุดการรักษาด้วย interferon หรือ glatiramer acetate
ในกรณีของไดเมทิลฟูมาเรต ระยะเวลาของ ชะล้าง จะต้องเพียงพอที่จะคืนค่าจำนวนเลือดให้เพียงพอก่อนเริ่มการรักษาด้วย Gilenya
เนื่องจากครึ่งชีวิตที่ยาวนานของ natalizumab การกำจัดโดยทั่วไปจะใช้เวลาถึง 2-3 เดือนหลังจากหยุดการรักษา Teriflumonide จะถูกกำจัดออกจากพลาสมาอย่างช้าๆ หากไม่มีขั้นตอนการกำจัดแบบเร่งด่วน การกำจัด teriflunomide จากพลาสมาอาจใช้เวลาหลายเดือนถึง 2 ปี ขอแนะนำให้ดำเนินการตามขั้นตอนการกำจัดแบบเร่งด่วนตามที่อธิบายไว้ในบทสรุปของคุณลักษณะของผลิตภัณฑ์สำหรับ teriflunomide หรืออีกทางหนึ่งคือระยะเวลาการชะล้างไม่ควรน้อยกว่า 3.5 เดือน ควรใช้ความระมัดระวังเมื่อเปลี่ยนผู้ป่วยจากการรักษาด้วย natalizumab หรือ teriflunomide ไปเป็น Gilenya เกี่ยวกับผลกระทบที่อาจเกิดขึ้นพร้อมกันในระบบภูมิคุ้มกัน
Alemtuzumab มีผลกดภูมิคุ้มกันที่รุนแรงและยาวนาน เนื่องจากไม่ทราบระยะเวลาที่แท้จริงของผลกระทบเหล่านี้ จึงไม่แนะนำให้เริ่มการรักษาด้วย Gilenya ตาม alemtuzumab เว้นแต่ว่าประโยชน์ของการรักษาสำหรับผู้ป่วยแต่ละรายมีมากกว่าความเสี่ยงอย่างชัดเจน
การตัดสินใจร่วมให้การรักษาด้วยยาคอร์ติโคสเตียรอยด์เป็นเวลานานจะต้องทำหลังจากพิจารณาอย่างรอบคอบแล้ว
การบริหารร่วมกับตัวกระตุ้น CYP450 ที่มีศักยภาพ
ควรใช้ Fingolimod ด้วยความระมัดระวังร่วมกับตัวกระตุ้น CYP450 ที่มีศักยภาพ ขอแนะนำว่าอย่าใช้สาโทเซนต์จอห์นควบคู่กันไป (ดูหัวข้อ 4.5)
การยุติการรักษา
ขึ้นอยู่กับครึ่งชีวิตของยา หากมีการตัดสินใจยุติการรักษาด้วย Gilenya ควรเว้นช่วงเวลา 6 สัปดาห์โดยไม่มีการรักษาเพื่อให้ fingolimod ถูกล้างออกจากเลือด (ดูหัวข้อ 5.2) การนับจำนวนเม็ดเลือดขาวแบบค่อยเป็นค่อยไป กลับสู่ค่าปกติภายใน 1-2 เดือนหลังจากหยุดการรักษา (ดูหัวข้อ 5.1) การเริ่มการรักษาอื่นๆ ในช่วงเวลานี้ส่งผลให้เกิดการสัมผัส fingolimod ร่วมกัน การใช้ยากดภูมิคุ้มกันทันทีหลังจากหยุดใช้ยา Gilenya อาจส่งผลเพิ่มเติมต่อระบบภูมิคุ้มกัน ดังนั้นจึงขอแนะนำให้ใช้ความระมัดระวัง
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
ยาต้านมะเร็ง การบำบัดด้วยภูมิคุ้มกันหรือยากดภูมิคุ้มกัน
ไม่ควรให้การรักษาด้วยยาต้านมะเร็ง ภูมิคุ้มกัน หรือยากดภูมิคุ้มกันควบคู่กัน เนื่องจากมีความเสี่ยงที่จะเกิดผลเสริมต่อระบบภูมิคุ้มกัน (ดูหัวข้อ 4.3 และ 4.4)
ควรใช้ความระมัดระวังเมื่อผู้ป่วยเริ่มการรักษาด้วย Gilenya หลังจากหยุดการรักษาด้วยการรักษาที่ออกฤทธิ์นานซึ่งมีผลต่อระบบภูมิคุ้มกัน เช่น natalizumab หรือ mitoxantrone (ดูหัวข้อ 4.4) ในการทดลองทางคลินิกในเส้นโลหิตตีบ ของคอร์ติโคสเตียรอยด์ไม่สัมพันธ์กับอัตราการติดเชื้อที่เพิ่มขึ้น
การฉีดวัคซีน
การฉีดวัคซีนอาจมีประสิทธิภาพน้อยลงในระหว่างการรักษาและนานถึงสองเดือนหลังจากหยุดการรักษาด้วย Gilenya การใช้วัคซีนที่มีชีวิตอ่อนฤทธิ์อาจเสี่ยงต่อการติดเชื้อและด้วยเหตุนี้จึงควรหลีกเลี่ยง (ดูหัวข้อ 4.4 และ 4.8)
สารที่กระตุ้นให้หัวใจเต้นช้า
Fingolimod ได้รับการศึกษาร่วมกับ atenolol และ diltiazem เมื่อใช้ fingolimod ร่วมกับ atenolol ในการศึกษาปฏิสัมพันธ์ในอาสาสมัครที่มีสุขภาพดี อัตราการเต้นของหัวใจลดลงอีก 15% เมื่อเริ่มการรักษา ไม่พบผลกระทบนี้กับ diltiazem เนื่องจากอาจมีผลข้างเคียง อัตราการเต้นของหัวใจ การรักษาด้วย Gilenya ควร ห้ามใช้ในผู้ป่วยที่ใช้ยา beta-blockers หรือยาอื่นๆ ที่อาจลดอัตราการเต้นของหัวใจ เช่น ยาต้านการเต้นผิดจังหวะ class Ia และ III, calcium channel blockers (เช่น ivabradine, verapamil หรือ diltiazem), digoxin, anticholinesterases หรือ pilocarpine (ดูหัวข้อ 4.4 และ 4.8 ) หากผู้ป่วยเหล่านี้พิจารณาการรักษาด้วย Gilenya ควรปรึกษาแพทย์โรคหัวใจเพื่อพิจารณาเปลี่ยนไปใช้ผลิตภัณฑ์ยาอื่น ๆ ที่ไม่ส่งผลให้อัตราการเต้นของหัวใจลดลงหรือเพื่อกำหนดการตรวจสอบที่เพียงพอในช่วงเริ่มต้นของการรักษา หากไม่สามารถหยุดการรักษาด้วยยาที่ลดอัตราการเต้นของหัวใจได้ แนะนำให้ติดตามอย่างน้อยจนถึงเช้าวันถัดไป
การเปลี่ยนแปลงทางเภสัชจลนศาสตร์ของ fingolimod ที่เกิดจากสารอื่น
Fingolimod ถูกเผาผลาญเป็นหลักโดย CYP4F2 เอนไซม์อื่นๆ เช่น CYP3A4 อาจเกี่ยวข้องกับการเผาผลาญของมัน โดยเฉพาะอย่างยิ่งในกรณีที่มีการเหนี่ยวนำ CYP3A4 ที่มีศักยภาพ สารยับยั้งโปรตีนตัวพาที่มีศักยภาพไม่คาดว่าจะส่งผลต่อพฤติกรรมของ fingolimod การใช้ยา fingolimod ร่วมกับ ketoconazole ร่วมกันส่งผลให้ได้รับ fingolimod และ fingolimod phosphate เพิ่มขึ้น 1.7 เท่าผ่านการยับยั้ง CYP4F2 ควรใช้ความระมัดระวังในการบริหาร fingolimod กับสารที่อาจยับยั้ง CYP3A4 ( protease inhibitors, azole antifungals บางชนิด macrolides เช่น clarithromycin หรือ telithromycin)
การใช้ carbamazepine 600 มก. วันละสองครั้งในสภาวะคงที่และ fingolimod 2 มก. เพียงครั้งเดียวลด AUC ของ fingolimod และเมแทบอไลต์ของมันลงประมาณ 40% ตัวกระตุ้นที่มีศักยภาพอื่น ๆ ของเอนไซม์ CYP3A4 เช่น rifampicin, phenobarbital, phenytoin efavirenz และสาโทเซนต์จอห์นสามารถกระตุ้นให้ AUC ของ fingolimod และ metabolite ลดลงอย่างน้อยขนาดนี้ เนื่องจากอาจทำให้ประสิทธิภาพลดลง ควรใช้ความระมัดระวังเมื่อให้ยาควบคู่กัน อย่างไรก็ตาม ไม่แนะนำให้ใช้ร่วมกับสาโทเซนต์จอห์น (ดูหัวข้อ 4.4)
การเปลี่ยนแปลงทางเภสัชวิทยาของสารอื่นๆ ที่เกิดจาก fingolimod
Fingolimod ไม่น่าจะทำปฏิกิริยากับสารที่ถูกเผาผลาญโดยเอนไซม์ CYP450 หรือสารตั้งต้นของโปรตีนพาหะหลัก
การใช้ยา fingolimod ร่วมกับ cyclosporine ร่วมกันไม่ได้ส่งผลให้เกิดการเปลี่ยนแปลงใด ๆ ในการสัมผัสกับ cyclosporine หรือ fingolimod ดังนั้น fingolimod จึงไม่คาดว่าจะเปลี่ยนแปลงเภสัชจลนศาสตร์ของผลิตภัณฑ์ยาที่เป็นสารตั้งต้นของ CYP3A4
การใช้ยา fingolimod ร่วมกับยาคุมกำเนิด (ethinyl estradiol และ levonorgestrel) ร่วมกัน ไม่ส่งผลให้การรับยาคุมกำเนิดเปลี่ยนแปลงไปแต่อย่างใด
04.6 การตั้งครรภ์และให้นมบุตร
ผู้หญิงที่มีศักยภาพในการคลอดบุตร / การคุมกำเนิดในสตรี
ก่อนเริ่มการรักษาด้วย Gilenya สตรีมีครรภ์ควรได้รับแจ้งถึงความเสี่ยงร้ายแรงที่อาจเกิดขึ้นต่อทารกในครรภ์และความจำเป็นในการใช้มาตรการคุมกำเนิดที่มีประสิทธิภาพระหว่างการรักษาด้วย Gilenya เนื่องจากใช้เวลาประมาณสองเดือนหลังจากหยุดการรักษาเพื่อล้าง fingolimod ออกจากร่างกาย (ดูหัวข้อ 4.4) ความเสี่ยงที่อาจเกิดขึ้นกับทารกในครรภ์จึงอาจมีอยู่ ดังนั้นมาตรการคุมกำเนิดจึงต้องดำเนินต่อไปในช่วงเวลานั้น
การตั้งครรภ์
ต้องมีการทดสอบการตั้งครรภ์เป็นลบก่อนเริ่มการรักษาในสตรีมีครรภ์ ผู้หญิงไม่ควรตั้งครรภ์ระหว่างการรักษาและแนะนำให้คุมกำเนิดอย่างมีประสิทธิภาพ หากสตรีตั้งครรภ์ขณะรับประทาน Gilenya ขอแนะนำให้หยุดการรักษา
การศึกษาในสัตว์ทดลองแสดงให้เห็นถึงความเป็นพิษต่อระบบสืบพันธุ์รวมถึงการสูญเสียของทารกในครรภ์และข้อบกพร่องของอวัยวะโดยเฉพาะอย่างยิ่งหลอดเลือดแดงถาวรและข้อบกพร่องของผนังกั้นห้องล่าง (ดูหัวข้อ 5.3) นอกจากนี้ ตัวรับซึ่ง fingolimod ทำหน้าที่ (sphingosine 1-phosphate ) มีส่วนเกี่ยวข้องกับการก่อตัวของหลอดเลือดในระหว่างการสร้างตัวอ่อน มีข้อมูลที่จำกัดมากจากการใช้ fingolimod ในหญิงตั้งครรภ์
ไม่มีข้อมูลเกี่ยวกับผลกระทบของ fingolimod ต่อแรงงานและการคลอดบุตร
เวลาให้อาหาร
Fingolimod ถูกขับออกมาในน้ำนมของสัตว์ที่ให้นมบุตรที่ความเข้มข้นสูงกว่าที่พบในพลาสมาของมารดา 2-3 เท่า (ดูหัวข้อ 5.3) เนื่องจากอาจเกิดปฏิกิริยาข้างเคียงที่ร้ายแรงต่อ fingolimod ในทารกที่กินนมแม่ ผู้หญิงที่รักษาด้วย Gilenya ไม่ควร ให้นมลูก
ภาวะเจริญพันธุ์
ข้อมูลจากการศึกษาพรีคลินิกไม่ได้บ่งชี้ว่า fingolimod มีความสัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของภาวะเจริญพันธุ์บกพร่อง (ดูหัวข้อ 5.3)
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
Gilenya ไม่มีหรือมีอิทธิพลเล็กน้อยต่อความสามารถในการขับขี่หรือใช้เครื่องจักร
อย่างไรก็ตาม บางครั้งอาการวิงเวียนศีรษะหรืออาการง่วงซึมอาจเกิดขึ้นได้เมื่อเริ่มการรักษาด้วย Gilenya ขอแนะนำให้สังเกตผู้ป่วยเป็นเวลา 6 ชั่วโมงเมื่อเริ่มการรักษาด้วย Gilenya (ดูหัวข้อ 4.4 Bradyarrhythmia)
04.8 ผลกระทบที่ไม่พึงประสงค์
สรุปข้อมูลความปลอดภัย
ประชากรด้านความปลอดภัยของ Gilenya มาจากการทดลองทางคลินิกที่ควบคุมด้วยยาหลอกระยะที่ 3 และการทดลองทางคลินิกระยะที่ 3 ที่ควบคุมโดย Active หนึ่งครั้งซึ่งดำเนินการในผู้ป่วยที่มีโรคปลอกประสาทเสื่อมแข็งแบบกำเริบ-ส่งกลับ รวมผู้ป่วยทั้งหมด 2,431 รายที่ได้รับการรักษาด้วย Gilenya (0.5 หรือ 1.25 มก.) ในการศึกษาทางคลินิกที่ควบคุมด้วยยาหลอก D2301 (FREDOMS) ระยะเวลา 2 ปี ผู้ป่วย 854 ราย (ยาหลอก: 418 ราย) ได้รับการรักษาด้วย fingolimod ในการศึกษา D2309 (FREDOMS II) ที่ควบคุมด้วยยาหลอก 2 ปี) ผู้ป่วย 728 รายที่เป็นโรคปลอกประสาทเสื่อมแข็ง (ยาหลอก: 355 ราย) ได้รับการรักษาด้วย fingolimod ผลรวมจากการศึกษาทั้งสองนี้ระบุว่าอาการไม่พึงประสงค์ที่ร้ายแรงที่สุดที่เกิดขึ้นกับ Gilenya 0.5 มก. ได้แก่ การติดเชื้อ อาการจุดภาพชัด และการอุดตันของหัวใจห้องล่างแบบชั่วคราวในช่วงเริ่มต้นของการรักษา อาการไม่พึงประสงค์ที่พบบ่อยที่สุด (อุบัติการณ์ ≥ 10%) ที่เกิดขึ้นกับ Gilenya 0.5 มก. ได้แก่ ไข้หวัดใหญ่ ไซนัสอักเสบ ปวดศีรษะ ท้องร่วง ปวดหลัง เอนไซม์ตับสูง และไอ อาการไม่พึงประสงค์ที่พบบ่อยที่สุดกับ Gilenya 0.5 มก. ที่นำไปสู่การ "หยุดการรักษา" เพิ่มระดับ ALT ในเลือด (2.2%) ในการศึกษา 1 ปี D2302 (TRANSFORMS) ที่เกี่ยวข้องกับผู้ป่วย 849 รายที่ได้รับ fingolimod และใช้ interferon beta-1αเป็นตัวควบคุม อาการไม่พึงประสงค์ที่เกิดขึ้นโดยทั่วไปมักคล้ายกับในการศึกษาที่ควบคุมด้วยยาหลอก โดยคำนึงถึงระยะเวลาการศึกษาที่แตกต่างกัน
อาการไม่พึงประสงค์ที่รายงานสำหรับ Gilenya 0.5 มก. ในการศึกษา D2301 (FREEDOMS) และ D2309 (FREDOMS II) แสดงไว้ด้านล่าง หมวดหมู่ความถี่ถูกกำหนดโดยใช้แบบแผนต่อไปนี้: ธรรมดามาก (≥1 / 10); ทั่วไป (≥1 / 100,
ตารางสรุปอาการไม่พึงประสงค์
* ไม่ได้รายงานในการศึกษา FREEDOMS, FREEDOMS II และ TRANSFOMS การจัดหมวดหมู่ความถี่ของเหตุการณ์ขึ้นอยู่กับ "การสัมผัส fingolimod ของผู้ป่วยประมาณ 10,000 รายในการทดลองทางคลินิกทั้งหมด"
คำอธิบายของอาการไม่พึงประสงค์บางอย่าง
การติดเชื้อ
ในการทดลองทางคลินิกในผู้ป่วยโรคปลอกประสาทเสื่อมแข็ง อัตราการติดเชื้อโดยรวม (65.1%) ที่รายงานด้วยขนาดยา 0.5 มก. มีความคล้ายคลึงกับที่พบในยาหลอก อย่างไรก็ตาม การติดเชื้อทางเดินหายใจส่วนล่าง ซึ่งส่วนใหญ่เป็นโรคหลอดลมอักเสบ และการติดเชื้อเริมและโรคปอดบวมในระดับที่น้อยกว่านั้นพบได้บ่อยในผู้ป่วยที่รักษาด้วย Gilenya
มีรายงานบางกรณีของการติดเชื้อเริมที่แพร่ระบาด รวมทั้งกรณีที่เสียชีวิตได้ แม้จะใช้ยาขนาด 0.5 มก.
จอประสาทตาบวมน้ำ
ในการศึกษาทางคลินิกในผู้ป่วยที่มีอาการบวมน้ำจุดภาพชัดหลายเส้นโลหิตตีบเกิดขึ้นใน 0.5% ของผู้ป่วยที่ได้รับยาที่แนะนำคือ 0.5 มก. และ 1.1% ของผู้ป่วยที่ได้รับยาในปริมาณที่สูงขึ้น (1, 25 มก.) ส่วนใหญ่เกิดขึ้นภายใน 3-4 เดือนแรกของการรักษา ผู้ป่วยบางรายรายงานว่าตาพร่ามัวและการมองเห็นลดลง คนอื่น ๆ ไม่มีอาการและได้รับการวินิจฉัยในระหว่างการเข้ารับการตรวจทางจักษุวิทยาเป็นประจำอาการบวมน้ำที่จุดภาพมักดีขึ้นหรือหายเองตามธรรมชาติหลังจากหยุดการรักษาด้วย Gilenya ยังไม่มีการศึกษาความเสี่ยงของการกลับเป็นซ้ำหลังจากสัมผัสกับการรักษาซ้ำ
อุบัติการณ์ของ macular edema เพิ่มขึ้นในผู้ป่วยหลายเส้นโลหิตตีบที่มีประวัติของ uveitis (17% ที่มีประวัติของ uveitis เทียบกับ 0.6% โดยไม่มีประวัติของ uveitis) Gilenya ไม่ได้รับการศึกษาในผู้ป่วยที่เป็นโรคปลอกประสาทเสื่อมแข็งและเบาหวาน โรคที่เกี่ยวข้องกับความเสี่ยงที่จะเกิด macular edema (ดูหัวข้อ 4.4) ในการศึกษาทางคลินิกในผู้ป่วยที่ปลูกถ่ายไตรวมถึงผู้ป่วยโรคเบาหวาน การรักษาด้วย fingolimod 2.5 มก. และ 5 มก. ส่งผลให้มีอุบัติการณ์ของ macular edema เพิ่มขึ้นสองเท่า
Bradyarrhythmia
การเริ่มต้นการรักษาด้วย Gilenya ส่งผลให้อัตราการเต้นของหัวใจลดลงชั่วคราวและอาจเกี่ยวข้องกับความล่าช้าในการนำ atrioventricular ในการทดลองทางคลินิกในผู้ป่วยที่มีหลายเส้นโลหิตตีบพบว่าอัตราการเต้นของหัวใจลดลงสูงสุดภายใน 6 ชั่วโมงแรกหลังการผ่าตัด " เริ่มการรักษาโดยมีความถี่ลดลงโดยเฉลี่ย 12-13 ครั้งต่อนาทีระหว่างการรักษาด้วย Gilenya 0.5 มก. อัตราการเต้นของหัวใจลดลงต่ำกว่า 40 ครั้งต่อนาทีในผู้ป่วยที่ได้รับการรักษาด้วย Gilenya 0.5 มก. อัตราการเต้นของหัวใจเฉลี่ยกลับสู่การตรวจวัดพื้นฐานภายใน 1 เดือนของการรักษาต่อเนื่อง หัวใจเต้นช้าโดยทั่วไปไม่มีอาการ แต่ผู้ป่วยบางรายมีอาการเล็กน้อยถึงปานกลาง เช่น ความดันเลือดต่ำ เวียนศีรษะ เหนื่อยล้า และ/หรือใจสั่น ซึ่งหายได้ภายใน 24 ชั่วโมงแรกหลังเริ่มการรักษา (ดูหัวข้อ 4.4 และ 5.1 เพิ่มเติม)
ในการศึกษาทางคลินิกในผู้ป่วยที่มีหลายเส้นโลหิตตีบพบว่ามีการบล็อก atrioventricular block ระดับแรก (การขยาย "ช่วง PR ไปยัง ECG") ในผู้ป่วย 4.7% ที่ได้รับ fingolimod 0.5 มก. ในผู้ป่วย 2.8% ผู้ป่วยที่ได้รับ interferon beta- ในกล้ามเนื้อ 1α และ 1.6% ของผู้ป่วยที่ได้รับยาหลอก มีรายงานการบล็อก atrioventricular ระดับที่สองในผู้ป่วยที่ได้รับ Gilenya 0.5 มก. น้อยกว่า 0.2% ในประสบการณ์หลังการขาย มีรายงานช่วงที่แยกได้ชั่วคราวของการแก้ไขบล็อก atrioventricular ที่สมบูรณ์โดยธรรมชาติในช่วงระยะเวลาการตรวจสอบ 6 ชั่วโมงหลังการให้ยา Gilenya ครั้งแรก ประสบการณ์หลังการตลาดมักจะเกิดขึ้นชั่วคราว ไม่มีอาการ และแก้ไขได้ภายใน 24 ครั้งแรก ชั่วโมงของการเริ่มต้นการรักษา แม้ว่าผู้ป่วยส่วนใหญ่ไม่จำเป็นต้องมีการแทรกแซงทางการแพทย์ แต่ผู้ป่วยรายหนึ่งที่ได้รับการรักษาด้วย Gilenya 0, 5 มก. ได้รับ isoprenaline หลังจาก Mobitz type 1 atrioventricular block 1 ระดับที่ไม่มีอาการ
จากประสบการณ์หลังการขายยา เหตุการณ์ที่แยกออกมาซึ่งเริ่มมีอาการช้า ได้แก่ ภาวะ asystole ชั่วคราวและการเสียชีวิตโดยไม่ทราบสาเหตุ เกิดขึ้นภายใน 24 ชั่วโมงหลังการให้ยาครั้งแรก การประเมินกรณีเหล่านี้มีความซับซ้อนจากการมียาร่วมและ/หรือยาที่มีอยู่ก่อนแล้ว เงื่อนไข ความสัมพันธ์ของเหตุการณ์เหล่านี้กับ Gilenya นั้นไม่แน่นอน
ความดันโลหิต
ในการศึกษาทางคลินิกในผู้ป่วยโรคปลอกประสาทเสื่อมแข็ง การรักษาด้วย Gilenya 0.5 มก. มีความสัมพันธ์กับความดันโลหิตซิสโตลิกที่เพิ่มขึ้นโดยเฉลี่ยประมาณ 3 mmHg และความดันโลหิตช่วงล่างประมาณ 1 mmHg การเพิ่มขึ้นเหล่านี้เกิดขึ้นประมาณ 1 เดือนต่อมา การเริ่มต้นการรักษาและคงไว้ด้วย การรักษาต่อเนื่อง มีรายงานผู้ป่วย 6.5% ที่รักษาด้วย fingolimod 0.5 มก. และ 3.3% ของผู้ป่วยที่ได้รับยาหลอก มีรายงานกรณีความดันโลหิตสูงที่อาจต้องรักษาด้วยยาลดความดันโลหิตหรือหยุดใช้ยา Gilenya ภายในเดือนแรกและในวันที่ วันแรกของการรักษา (ดูหัวข้อ 4.4 ผลกระทบต่อความดันโลหิต)
การทำงานของตับ
มีรายงานการเพิ่มขึ้นของเอนไซม์ตับในผู้ป่วยโรคปลอกประสาทเสื่อมแข็งที่รักษาด้วย Gilenya ในการศึกษาทางคลินิกพบว่าระดับ ALT ในเลือดสูงขึ้นโดยไม่แสดงอาการ ≥3 เท่า และ ≥5 เท่าของขีดจำกัดบนของช่วงปกติ (ULN) ใน 8.0% และ 1.8% ของผู้ป่วยที่ได้รับการรักษาด้วย Gilenya ตามลำดับ 0.5 มก. ในผู้ป่วยบางราย การรักษาหลังจากหยุดยา ระดับเอนไซม์ตับ transaminase เกิดขึ้นอีกครั้ง เพื่อยืนยันความสัมพันธ์ระหว่างการเพิ่มขึ้นนี้กับยา ในการทดลองทางคลินิก ระดับเอนไซม์ตับ transaminases เกิดขึ้นได้ทุกเมื่อระหว่างการรักษา แม้ว่าส่วนใหญ่จะเกิดขึ้นในช่วง 12 เดือนแรก ระดับ ALT กลับมาเป็นปกติประมาณ 2 เดือน หลังจากหยุดการรักษาด้วย Gilenya ในผู้ป่วยจำนวนน้อย (N = 10 ที่ขนาด 1.25 มก., N = 2 ที่ขนาด 0.5 มก.) ซึ่งพบระดับ ALT ≥5 เท่าของขีดจำกัดบนของช่วงปกติและผู้ที่ยังคงรักษาด้วย Gilenya ค่า ALT กลับมาเป็นปกติภายในเวลาประมาณ 5 เดือน (ดูหัวข้อ 4.4 การทำงานของตับด้วย)
ความผิดปกติของระบบประสาท
ในการศึกษาทางคลินิก เหตุการณ์ที่เกิดขึ้นไม่บ่อยนักที่เกี่ยวข้องกับระบบประสาท รวมทั้งโรคหลอดเลือดสมองตีบและโรคหลอดเลือดสมองตีบและความผิดปกติทางระบบประสาทที่ผิดปกติ เช่น เหตุการณ์ที่คล้ายกับโรคสมองอักเสบเฉียบพลันที่แพร่กระจาย (EAD)
โรคหลอดเลือด
กรณีที่ไม่ค่อยพบของโรคหลอดเลือดแดงส่วนปลายเกิดขึ้นในผู้ป่วยที่ได้รับการรักษาด้วย fingolimod ในปริมาณที่สูงขึ้น (1.25 มก.)
ระบบทางเดินหายใจ
การลดลงของปริมาณการหายใจที่ถูกบังคับ (FEV1) และความสามารถในการแพร่ของคาร์บอนมอนอกไซด์ (Dlco) ขึ้นอยู่กับขนาดยาเล็กน้อยถูกสังเกตระหว่างการรักษาด้วย Gilenya การลดลงที่เกิดขึ้นในเดือนแรกและยังคงทรงตัวตลอดการรักษา ในเดือนที่ 24 เปอร์เซ็นต์การลดลงจากค่าพื้นฐานใน FEV1 ที่คาดการณ์ไว้คือ 2.7% สำหรับ fingolimod 0.5 มก. และ 1.2% สำหรับยาหลอก ความแตกต่างที่แก้ไขได้หลังจากหยุดการรักษา การลด Dlco ในเดือนที่ 24 เท่ากับ 3.3% สำหรับ fingolimod 0.5 มก. และ 2.7% สำหรับยาหลอก
มะเร็งต่อมน้ำเหลือง
มีรายงานกรณีของมะเร็งต่อมน้ำเหลืองชนิดต่างๆ ทั้งในการทดลองทางคลินิกและประสบการณ์หลังการขาย ซึ่งรวมถึง มะเร็งต่อมน้ำเหลือง B-cell ที่เป็นบวกจากไวรัส Epstein-Barr (EBV) ) มีการศึกษาทางคลินิกสูงกว่าที่คาดไว้ในประชากรทั่วไป
โรคโลหิตจาง
มีรายงานกรณีที่พบได้น้อยมากของโรคโลหิตจาง (โรคโลหิตจาง, HPS) มีผลร้ายแรงในผู้ป่วยที่รักษาด้วย fingolimod ในบริบทของ "การติดเชื้อ" HPS เป็นภาวะที่หายากซึ่งได้รับการอธิบายเกี่ยวกับการติดเชื้อ การกดภูมิคุ้มกัน และโรคภูมิต้านตนเองต่างๆ
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านระบบการรายงานระดับประเทศ ในภาคผนวก 5 .
04.9 ใช้ยาเกินขนาด
การให้ยาเดี่ยวสูงถึง 80 เท่าของขนาดยาที่แนะนำ (0.5 มก.) สามารถทนได้ดีในอาสาสมัครที่มีสุขภาพดี ที่ขนาดยา 40 มก. 5 ใน 6 คนรายงานว่าแน่นหน้าอกที่อ่อนแอหรือมีอาการป่วยไข้ที่เกี่ยวข้องกับปฏิกิริยาทางเดินหายใจ
Fingolimod สามารถทำให้หัวใจเต้นช้าได้ในช่วงเริ่มต้นของการรักษา อัตราการเต้นของหัวใจที่ลดลงมักเกิดขึ้นภายในหนึ่งชั่วโมงของการใช้ยาครั้งแรกและจะสูงสุดภายใน 6 ชั่วโมงแรก ผลกระทบที่เกิดต่อเนื่องกันในเชิงลบของ Gilenya ยังคงมีอยู่เกิน 6 ชั่วโมงและค่อยๆ หายไปในวันถัดไปของการรักษา (ดูหัวข้อ 4.4 สำหรับรายละเอียดเพิ่มเติม) มีรายงานเกี่ยวกับการนำ atrioventricular conduction ช้าลง โดยมีรายงานแยกของ atrioventricular block (ดูหัวข้อ 4.4 และ 4.8)
หากการให้ยาเกินขนาดเกิดขึ้นพร้อมกับการสัมผัสครั้งแรกกับ Gilenya สิ่งสำคัญคือต้องมีการตรวจคลื่นไฟฟ้าหัวใจอย่างต่อเนื่อง (แบบเรียลไทม์) ของผู้ป่วยด้วยการวัดอัตราการเต้นของหัวใจรายชั่วโมงและความดันโลหิต อย่างน้อยในช่วง 6 ชั่วโมงแรก (ดูหัวข้อ 4.4)
จำเป็นต้องมีการตรวจสอบเพิ่มเติม (อย่างน้อยก็จนถึงเช้าวันรุ่งขึ้นและในกรณีใด ๆ จนกว่าอาการจะได้รับการแก้ไข) หากหลังจาก 6 ชั่วโมงนับจากการให้ยาครั้งแรก อัตราการเต้นของหัวใจจะเท่ากับ
Fingolimod ไม่ได้ถูกกำจัดโดยการฟอกไตหรือพลาสมาเฟเรซิส
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มเภสัชบำบัด: ยากดภูมิคุ้มกันแบบเลือก
รหัส ATC: L04AA27
กลไกการออกฤทธิ์
Fingolimod เป็นโมดูเลเตอร์ตัวรับ sphingosine-1-phosphate (S1P)โดยวิธีการของ sphingosine kinase fingolimod จะถูกเปลี่ยนเป็น metabolite fingolimod phosphate ซึ่งเป็นสารออกฤทธิ์ซึ่งจับที่ความเข้มข้นระดับนาโนโมลาร์ต่ำไปยังตัวรับ S1P1 ที่อยู่บนผิวลิมโฟไซต์และข้ามสิ่งกีดขวางเลือดและสมองเพื่อผูกกับตัวรับในระบบประสาทส่วนกลางได้อย่างง่ายดาย ระบบ S1P1 วางอยู่บนเซลล์ของระบบประสาทส่วนกลาง Fingolimod ฟอสเฟต ซึ่งทำหน้าที่เป็นตัวต่อต้านการทำงานของตัวรับ S1P ที่แสดงบนเซลล์ลิมโฟไซต์ ยับยั้งความสามารถของเซลล์ลิมโฟไซต์ในการหลบหนีจากต่อมน้ำเหลือง ส่งผลให้เกิดการกระจายตัวมากกว่าการทำลายของลิมโฟไซต์ การแจกจ่ายซ้ำนี้จะช่วยลดการแทรกซึมของลิมโฟไซต์ที่ทำให้เกิดโรคเข้าสู่ระบบประสาทส่วนกลาง ซึ่งเกี่ยวข้องกับการอักเสบของเส้นประสาทและความเสียหายของเนื้อเยื่อ การศึกษาและการทดลองในสัตว์ทดลอง ในหลอดทดลอง บ่งชี้ว่า fingolimod สามารถกระทำได้โดยการโต้ตอบกับตัวรับ S1P ที่แสดงบนเซลล์ของระบบประสาทส่วนกลาง
ผลทางเภสัชพลศาสตร์
ภายใน 4-6 ชั่วโมงหลังการให้ fingolimod 0.5 มก. ครั้งแรก จำนวนเม็ดเลือดขาวในเลือดส่วนปลายจะลดลงเหลือประมาณ 75% ของค่าพื้นฐาน ต่อเนื่องกับการบริหารรายวัน จำนวนเซลล์เม็ดเลือดขาวยังคงลดลงอย่างต่อเนื่องเป็นเวลาสองสัปดาห์ โดยมีค่าต่ำสุดประมาณ 500 เซลล์/ไมโครลิตร หรือประมาณ 30% ของค่าพื้นฐาน 18% ของผู้ป่วยมีค่าต่ำสุดที่ต่ำกว่า 200 เซลล์ / ไมโครลิตรอย่างน้อยหนึ่งครั้ง ด้วยการรักษาทุกวันอย่างต่อเนื่อง จำนวนเม็ดเลือดขาวยังคงต่ำ ลิมโฟไซต์ T และ B ส่วนใหญ่มักอพยพผ่านอวัยวะน้ำเหลือง: fingolimod ทำหน้าที่ส่วนใหญ่ในเซลล์เหล่านี้ ประมาณ 15-20% ของ T lymphocytes มี TEM (memory effector) ฟีโนไทป์: เซลล์เหล่านี้มีความสำคัญต่อการเฝ้าระวังภูมิคุ้มกันส่วนปลาย เนื่องจากเซลล์ลิมโฟไซต์ชนิดนี้โดยทั่วไปจะไม่ย้ายไปที่อวัยวะน้ำเหลือง fingolimod จึงไม่ทำปฏิกิริยากับเซลล์เหล่านี้ การเพิ่มขึ้นของจำนวนเซลล์เม็ดเลือดขาวส่วนปลายจะเห็นได้ชัดเจนในวันหลังหยุดการรักษาด้วย fingolimod; จำนวนเม็ดเลือดขาวมักจะกลับมาเป็นปกติภายในหนึ่งถึงสองเดือน การใช้ fingolimod แบบเรื้อรังส่งผลให้จำนวนนิวโทรฟิลลดลงเล็กน้อยเท่ากับประมาณ 80% ของค่าพื้นฐาน Fingolimod ไม่ทำปฏิกิริยากับโมโนไซต์
Fingolimod ทำให้อัตราการเต้นของหัวใจลดลงชั่วคราวและการนำ atrioventricular ลดลงเมื่อเริ่มการรักษา (ดูหัวข้อ 4.4 และ 4.8) อัตราการเต้นของหัวใจลดลงสูงสุดภายใน 6 ชั่วโมงของการบริหาร โดย 70% ของผล chronotropic เชิงลบ ด้วยการบริหารให้ครั้งต่อๆ ไป อัตราการเต้นของหัวใจจะกลับสู่การตรวจวัดพื้นฐานภายในหนึ่งเดือน การลดลงของอัตราการเต้นของหัวใจที่เกิดจาก fingolimod สามารถย้อนกลับได้โดยการให้ atropine หรือ isoprenaline ทางหลอดเลือด salmeterol ที่สูดดมยังแสดงให้เห็นว่ามีผล chronotropic ในเชิงบวกเล็กน้อย เมื่อเริ่มการรักษาด้วย fingolimod การหดตัวของหัวใจห้องบนก่อนวัยจะเพิ่มขึ้น แต่ไม่มีอัตราการเกิดภาวะหัวใจห้องบน / กระพือปีกหรือภาวะหัวใจเต้นผิดจังหวะหรือ ectopia เพิ่มขึ้น การรักษาด้วย fingolimod ไม่ส่งผลให้การเต้นของหัวใจลดลง และไม่ส่งผลต่อการตอบสนองของหัวใจ รวมถึงการแปรผันของอัตราการเต้นของหัวใจในแต่ละวันและการตอบสนองต่อการออกแรง
การรักษาด้วย fingolimod ครั้งเดียวหรือซ้ำ 0.5 มก. และ 1.25 มก. เป็นเวลาสองสัปดาห์ ไม่ส่งผลให้มีการดื้อต่อทางเดินหายใจเพิ่มขึ้นอย่างเห็นได้ชัดเมื่อวัดเป็น FEV1 และ Forced Expiratory Flow (FEF) 25-75 อย่างไรก็ตาม เมื่อใช้ fingolimod ≥5 มก. ครั้งเดียว (10 เท่าของขนาดที่แนะนำ) ความต้านทานของทางเดินหายใจจะเพิ่มขึ้นตามขนาดยา การรักษาด้วย fingolimod ขนาด 0.5 มก., 1.25 มก. หรือ 5 มก. ซ้ำ ๆ จะไม่นำไปสู่การขาดออกซิเจนหรือการขาดออกซิเจนภายใต้การออกกำลังกายหรือการตอบสนองของทางเดินหายใจต่อเมธาโคลีนเพิ่มขึ้น บุคคลที่ได้รับ fingolimod ตอบสนองต่อการขยายหลอดลมตามปกติต่อ beta-agonists ที่สูดดม
ประสิทธิภาพและความปลอดภัยทางคลินิก
ประสิทธิภาพของ Gilenya แสดงให้เห็นในการศึกษาสองครั้งที่ประเมินการบริหาร fingolimod 0.5 มก. และ 1.25 มก. วันละครั้งในผู้ป่วยที่มีอาการกำเริบ-remitting หลายเส้นโลหิตตีบ (RRMS) การศึกษาทั้งสองเป็นผู้ป่วยที่ลงทะเบียนซึ่งมีอาการกำเริบ≥ 2 ครั้งในช่วง 2 ปีที่ผ่านมาหรือ ≥1 กำเริบในปีที่แล้ว คะแนนในระดับสถานะความทุพพลภาพขยาย (EDSS) คือ 0-5.5 การศึกษาครั้งที่สามที่ดำเนินการในประชากรผู้ป่วยกลุ่มเดียวกันเสร็จสมบูรณ์หลังจากการลงทะเบียนของ Gilenya
ในการศึกษา D2301 (FREEDOMS) ที่ควบคุมด้วยยาหลอกแบบ double-blind randomized double-blind ที่ควบคุมเป็นเวลา 2 ปี มีผู้ป่วย 1272 ราย (n = 425 ที่ได้รับ fingolimod 0.5 mg, 429 กับ fingolimod 1.25 mg, 418 กับ placebo) ค่ามัธยฐานของลักษณะพื้นฐานคือ อายุ 37 ปี ระยะเวลาโรค 6.7 ปี คะแนน EDSS 2.0 ผลลัพธ์แสดงในตารางที่ 1 ไม่มีความแตกต่างอย่างมีนัยสำคัญระหว่างขนาดยา 0.5 มก. และ 1.25 มก. สำหรับจุดยุติทั้งหมด
ตารางที่ 1: การศึกษา D2301 (เสรีภาพ): ผลลัพธ์หลัก
†ความก้าวหน้าของความทุพพลภาพกำหนดเป็น EDSS เพิ่มขึ้น 1 จุดได้รับการยืนยันเมื่อ 3 เดือน
** NS
จุดยุติทางคลินิกทั้งหมดได้รับการประเมินโดยการวิเคราะห์ ตั้งใจที่จะรักษา. การวิเคราะห์ที่เกี่ยวข้องกับข้อมูล MRI ที่ใช้ชุดข้อมูลที่ประเมินได้
ผู้ป่วยที่เสร็จสิ้นขั้นตอน แกน ของการศึกษา FREEDOMS 24 เดือนสามารถเข้าสู่ระยะการขยายขนาดยาปิดตา (D2301E1) และได้รับ fingolimod ผู้ป่วยที่เข้ารับการรักษาทั้งหมด 920 ราย (n = 331 ต่อเนื่องในขนาด 0.5 มก., 289 ในขนาด 1.25 มก., 155 เปลี่ยนจากยาหลอกเป็น 0.5 มก. และ 145 จากยาหลอกเป็น 1.25 มก.) หลังจาก 12 เดือน (เดือนที่ 36) ผู้ป่วย 856 ราย (93%) ยังคงลงทะเบียน ระหว่างเดือนที่ 24 ถึงเดือนที่ 36 อัตราการกำเริบของโรคต่อปี (ARR) สำหรับผู้ป่วยที่ได้รับ fingolimod 0.5 มก. ในระยะ แกน ของการศึกษาและผู้ที่รับประทานต่อเนื่องในขนาดเดียวกัน (0.5 มก.) คือ 0.17 (0.21 ในระยะ แกน ของการศึกษา) อัตราการกำเริบของโรคต่อปีสำหรับผู้ป่วยที่เปลี่ยนจากยาหลอกเป็น fingolimod 0.5 มก. คือ 0.22 (0.42 ในระยะ แกน ของการศึกษา)
ได้ผลลัพธ์ที่คล้ายคลึงกันในการศึกษาระยะที่ 3, 2 ปี, สุ่ม, double-blind, placebo-controlled (D2309; FREEDOMS 2) ที่ดำเนินการในผู้ป่วย 1,083 คนที่มี relapsing-remitting multiple sclerosis (n = 358 ที่ได้รับการรักษาด้วย fingolimod 0 , 5 มก. , 370 พร้อม fingolimod 1.25 มก., 355 พร้อมยาหลอก) ค่ามัธยฐานของลักษณะพื้นฐานคือ อายุ 41 ปี ระยะเวลาโรค 8.9 ปี คะแนน EDSS 2.5
ตารางที่ 2: การศึกษา D2309 (เสรีภาพ 2): ผลลัพธ์หลัก
†ความก้าวหน้าของความทุพพลภาพกำหนดเป็น EDSS เพิ่มขึ้น 1 จุดได้รับการยืนยันเมื่อ 3 เดือน
** NS
จุดยุติทางคลินิกทั้งหมดได้รับการประเมินโดยการวิเคราะห์ ตั้งใจที่จะรักษา. การวิเคราะห์ที่เกี่ยวข้องกับข้อมูล MRI ที่ใช้ชุดข้อมูลที่ประเมินได้
ในการศึกษา D2302 (TRANSFORMS) ระยะที่ 3 ระยะเวลา 1 ปี การสุ่มตัวอย่าง การควบคุมแบบ double-blind และ หุ่นจำลอง double เทียบกับยาออกฤทธิ์ (interferon beta-1α) รวมผู้ป่วย 1280 ราย (n = 429 รายที่ได้รับ fingolimod 0.5 มก., 420 รายร่วมกับ fingolimod 1.25 มก., 431 รายโดยฉีด interferon beta-1α เข้ากล้ามที่ขนาด 30 ไมโครกรัมสัปดาห์ละครั้ง) ค่ามัธยฐานของลักษณะพื้นฐานคือ อายุ 36 ปี ระยะเวลาโรค 5.9 ปี คะแนน EDSS 2.0 ผลการศึกษาแสดงในตารางที่ 3 ไม่มีความแตกต่างอย่างมีนัยสำคัญระหว่างขนาดยา 0.5 มก. และ 1.25 มก. ในส่วนที่เกี่ยวกับจุดสิ้นสุดของการศึกษา
ตารางที่ 3: การศึกษา D2302 (การแปลง): ผลลัพธ์หลัก
†ความก้าวหน้าของความทุพพลภาพกำหนดเป็น EDSS เพิ่มขึ้น 1 จุดได้รับการยืนยันเมื่อ 3 เดือน
** NS
จุดยุติทางคลินิกทั้งหมดได้รับการประเมินโดยการวิเคราะห์ ตั้งใจที่จะรักษา. การวิเคราะห์ที่เกี่ยวข้องกับข้อมูล MRI ที่ใช้ชุดข้อมูลที่ประเมินได้
ผู้ป่วยที่เสร็จสิ้นขั้นตอน แกน ของการศึกษา TRANSFORMS 12 เดือนสามารถเข้าสู่ระยะการขยายขนาดยาตาบอด (D2302E1) และรับ fingolimod มีผู้ป่วยเข้าร่วมทั้งหมด 1,030 ราย อย่างไรก็ตาม 3 ในจำนวนนี้ไม่ได้รับการรักษา (n = 356 ต่อเนื่องที่ขนาด 0.5 มก., 330 ที่ขนาด 1.25 มก., 167 เปลี่ยนจาก interferon beta-1α เป็น 0, 5 มก. และ 174 จาก interferon beta -1α ที่ 1.25 มก.) หลังจาก 12 เดือน (เดือนที่ 24) ผู้ป่วย 882 ราย (86%) ยังคงลงทะเบียน ระหว่างเดือนที่ 12 ถึง 24 อัตราการกำเริบต่อปี (ARR) สำหรับผู้ป่วยที่ได้รับ fingolimod 0.5 มก. ในระยะ แกน ของการศึกษาและผู้ที่รับประทานต่อเนื่องในขนาดเดียวกัน (0.5 มก.) คือ 0.20 (0.19 ในระยะ แกน ของการศึกษา) อัตราการกำเริบของโรคต่อปีสำหรับผู้ป่วยที่เปลี่ยนจาก interferon beta-1α เป็น fingolimod 0.5 มก. คือ 0.33 (0.48 ในระยะ แกน ของการศึกษา)
ผลรวมจากการศึกษา D2301 และ D2302 แสดงให้เห็นการลดลงอย่างต่อเนื่องและมีนัยสำคัญทางสถิติจากการควบคุมอัตราการกำเริบแบบรายปีในกลุ่มย่อยที่กำหนดโดยเพศ อายุ การรักษา MS ครั้งก่อน กิจกรรมของโรคหรือความทุพพลภาพที่การตรวจวัดพื้นฐาน
การวิเคราะห์เพิ่มเติมของผลการทดลองทางคลินิกแสดงให้เห็นถึงผลการรักษาที่มีนัยสำคัญในกลุ่มย่อยของผู้ป่วยที่มีอาการกำเริบ- remitting หลายเส้นโลหิตตีบ
European Medicines Agency ได้ชะลอภาระหน้าที่ในการส่งผลการศึกษากับ Gilenya ในกลุ่มย่อยอย่างน้อยหนึ่งกลุ่มของประชากรเด็กในโรคปลอกประสาทเสื่อมแข็ง (ดูหัวข้อ 4.2 สำหรับข้อมูลเกี่ยวกับการใช้ในเด็ก)
05.2 "คุณสมบัติทางเภสัชจลนศาสตร์
ข้อมูลเภสัชจลนศาสตร์ได้รับในอาสาสมัครสุขภาพดี ผู้ป่วยปลูกถ่ายไต และผู้ป่วยโรคปลอกประสาทเสื่อมแข็ง
เมแทบอไลต์ที่ออกฤทธิ์ทางเภสัชวิทยาที่รับผิดชอบต่อประสิทธิภาพคือ fingolimod phosphate
การดูดซึม
การดูดซึมของ fingolimod เกิดขึ้นอย่างช้าๆ (Tmax 12-16 ชั่วโมง) และครอบคลุมมาก (≥85%) การดูดซึมอย่างสมบูรณ์ที่ชัดเจนหลังการบริหารช่องปากคือ 93% (ช่วงความเชื่อมั่น: 79-111%) ความเข้มข้นของเลือดที่ สภาวะคงตัว จะบรรลุระดับได้ภายใน 1-2 เดือนหลังจากให้ยา fingolimod และระดับ allo วันละครั้ง สภาวะคงตัว สูงกว่าที่เห็นในขนาดเริ่มต้นประมาณ 10 เท่า
การรับประทานอาหารไม่เปลี่ยนค่าความเข้มข้นสูงสุด (Cmax) หรือค่าการสัมผัสอย่างเป็นระบบ (AUC) ของ fingolimod Fingolimod phosphate Cmax เพิ่มขึ้นเล็กน้อย 34% ในขณะที่ AUC ไม่เปลี่ยนแปลง ดังนั้น Gilenya สามารถรับประทานได้ทั้งในขณะท้องว่างหรือท้องว่าง (ดูหัวข้อ 4.2)
การกระจาย
Fingolimod กระจายอย่างรวดเร็วในเซลล์เม็ดเลือดแดงและมีอยู่ในเซลล์เม็ดเลือด 86% Fingolimod ฟอสเฟตมีการกระจายเซลล์เม็ดเลือดแดงลดลง 17% โปรตีนพลาสม่าจับกับ fingolimod และ fingolimod phosphate สูง (> 99%)
Fingolimod มีการกระจายอย่างกว้างขวางในเนื้อเยื่อโดยมีปริมาตรการกระจายประมาณ 1,200 ± 260 ลิตร
การเปลี่ยนแปลงทางชีวภาพ
ในมนุษย์ fingolimod ถูกเผาผลาญโดย stereoselective phosphorylation แบบย้อนกลับได้ด้วยการก่อตัวของสารออกฤทธิ์ทางเภสัชวิทยา (S) -enantiomer ของ fingolimod phosphate Fingolimod ถูกกำจัดโดยการเปลี่ยนรูปทางชีวภาพออกซิเดชัน เร่งปฏิกิริยาส่วนใหญ่โดย CYP4F2 และอาจเป็นไอโซเอนไซม์อื่น ๆ และการย่อยสลายตามมาด้วยสารที่ไม่ออกฤทธิ์คล้ายกับกรดไขมัน นอกจากนี้ยังสังเกตเห็นการก่อตัวของแอนะล็อกเซราไมด์ที่ไม่ใช่ขั้วที่ไม่ใช้งานทางเภสัชวิทยาของ fingolimod เอนไซม์หลักที่เกี่ยวข้องกับการเผาผลาญของ fingolimod นั้นถูกระบุเพียงบางส่วนและอาจเป็น CYP4F2 หรือ CYP3A4
หลังจากให้ fingolimod [14C] รับประทานครั้งเดียว ส่วนประกอบหลักที่เกี่ยวข้องกับ fingolimod ที่ตรวจพบในเลือดโดยการมีส่วนร่วมของ AUC นานถึง 34 วันหลังจากให้ส่วนประกอบที่ติดฉลากกัมมันตภาพรังสีทั้งหมด คือ fingolimod (23%) fingolimod phosphate ( 10%) และสารเมตาโบไลต์ที่ไม่ออกฤทธิ์บางชนิด (เมแทบอไลต์ของกรดคาร์บอกซิลิก M3 (8%), เมตาบอไลต์เซราไมด์ M29 (9%) และเมตาโบไลต์เซราไมด์ M30 (7%))
การกำจัด
การกวาดล้างเลือดของ fingolimod เท่ากับ 6.3 ± 2.3 L / h และค่าครึ่งชีวิตการกำจัดของปลายทางเฉลี่ย (t1/2) คือ 6-9 วัน ระดับเลือดของ fingolimod และ fingolimod phosphate ลดลงแบบคู่ขนานในระยะสุดท้ายจึงส่งผลให้มีครึ่งหนึ่งที่คล้ายคลึงกัน - มีชีวิตอยู่สำหรับทั้งสองโมเลกุล
หลังการให้ยาทางปากประมาณ 81% ของขนาดยาจะถูกขับออกทางปัสสาวะอย่างช้าๆ ในรูปของสารที่ไม่ออกฤทธิ์ Fingolimod และ fingolimod phosphate ไม่ถูกขับออกทางปัสสาวะไม่เปลี่ยนแปลงแต่ปรากฏเป็นส่วนประกอบหลักในอุจจาระ โดยแต่ละปริมาณมีสัดส่วนน้อยกว่า 2.5% ของขนาดยา . หลังจาก 34 วัน การฟื้นตัวของขนาดยาที่ให้คือ 89%
ความเป็นลิเนียร์
ความเข้มข้นของ fingolimod และ fingolimod phosphate เพิ่มขึ้นในสัดส่วนที่เห็นได้ชัดหลังจากให้ยาวันละ 0.5 มก. หรือ 1.25 มก. ซ้ำ ๆ
ลักษณะเฉพาะในประชากรจำเพาะ
เภสัชจลนศาสตร์ของ fingolimod และ fingolimod phosphate ไม่ได้แยกความแตกต่างระหว่างเพศชายและเพศหญิง ในผู้ป่วยที่มาจากชาติพันธุ์ที่แตกต่างกัน หรือในผู้ป่วยที่มีความบกพร่องทางไตเล็กน้อยถึงรุนแรง
ในผู้ป่วยที่มีความบกพร่องทางตับในระดับเล็กน้อย ปานกลาง หรือรุนแรง (Child-Pugh คลาส A, B และ C) ไม่มีการเปลี่ยนแปลงของ fingolimod Cmax ในขณะที่ fingolimod AUC เพิ่มขึ้น 12%, 44% และ 103% ในผู้ป่วยที่มีความบกพร่องทางตับอย่างรุนแรง ( Child-Pugh class C), fingolimod phosphate Cmax ลดลง 22% และ AUC ไม่เปลี่ยนแปลงอย่างมีนัยสำคัญ เภสัชจลนศาสตร์ของ fingolimod phosphate ยังไม่ได้รับการประเมินในผู้ป่วยที่มีความบกพร่องทางตับในระดับเล็กน้อยถึงปานกลาง ครึ่งชีวิตที่กำจัดชัดเจนของ fingolimod ไม่เปลี่ยนแปลงในอาสาสมัครที่มีความบกพร่องของตับเล็กน้อย ในขณะที่เพิ่มขึ้นประมาณ 50% ในผู้ป่วยที่มีความบกพร่องของตับในระดับปานกลางหรือรุนแรง
ไม่ควรใช้ Fingolimod ในผู้ป่วยที่มีความบกพร่องทางตับอย่างรุนแรง (Child-Pugh class C) (ดูหัวข้อ 4.3) การรักษาด้วย Fingolimod ควรเริ่มด้วยความระมัดระวังในผู้ป่วยที่มีความบกพร่องทางตับในระดับเล็กน้อยและปานกลาง (ดูหัวข้อ 4.2)
ประสบการณ์ทางคลินิกและข้อมูลเภสัชจลนศาสตร์ในผู้ป่วยที่มีอายุมากกว่า 65 ปีมีข้อ จำกัด ควรใช้ Gilenya ด้วยความระมัดระวังในผู้ป่วยที่มีอายุ 65 ปีขึ้นไป (ดูหัวข้อ 4.2)
ประชากรเด็ก
ข้อมูลจากการศึกษาการปลูกถ่ายไตซึ่งรวมถึงเด็กอายุมากกว่า 11 ปีจำนวน 7 คนมีข้อจำกัด (การศึกษา FTY720A0115) การเปรียบเทียบข้อมูลเหล่านี้กับข้อมูลของอาสาสมัครผู้ใหญ่ที่มีสุขภาพดีนั้นมีความเกี่ยวข้องเพียงเล็กน้อยและไม่มีข้อสรุปที่มีความหมายใดๆ เกี่ยวกับคุณสมบัติทางเภสัชจลนศาสตร์ของ fingolimod ในเด็ก
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ข้อมูลด้านความปลอดภัยพรีคลินิกของ fingolimod ได้รับการประเมินในหนู หนู หนู สุนัข และลิง อวัยวะเป้าหมายหลักคือระบบน้ำเหลือง (ต่อมน้ำเหลืองและต่อมน้ำเหลืองฝ่อ), ปอด (การเพิ่มของน้ำหนัก, การเจริญเติบโตมากเกินไปของกล้ามเนื้อเรียบที่รอยต่อ bronchioloalveolar) และในสปีชีส์ต่างๆ หัวใจ (ผล chronotropic เชิงลบ, ความดันโลหิตเพิ่มขึ้น, การเปลี่ยนแปลงของ perivascular และกล้ามเนื้อหัวใจตาย การเสื่อมสภาพ); ในการศึกษา 2 ปี fingolimod ใช้งานกับหลอดเลือด (vasculopathy) เฉพาะในหนูที่มีขนาด 0.15 มก. / กก. ขึ้นไปซึ่งเทียบเท่ากับการสัมผัสทั่วร่างกายของมนุษย์ (AUC) ประมาณ 4 เท่าในขนาดรายวัน 0 , 5 มก.
ไม่พบหลักฐานการก่อมะเร็งในการศึกษาระยะเวลา 2 ปีในหนูที่ได้รับ fingolimod ในขนาดยาทางปากจนถึงขนาดยาสูงสุดที่ยอมรับได้ 2.5 มก. / กก. ซึ่งแสดงถึงระยะขอบประมาณ 50 เท่าของการได้รับสัมผัสทั่วร่างกายของมนุษย์ (AUC) ที่ขนาดยา 0.5 มก. อย่างไรก็ตาม ในการศึกษา 2 ปีในหนูทดลอง พบอุบัติการณ์ของมะเร็งต่อมน้ำเหลืองชนิดร้ายที่ปริมาณ 0.25 มก. / กก. และสูงกว่าซึ่งเทียบเท่ากับการสัมผัสของมนุษย์ประมาณ 6 เท่า ระบบ (AUC) ในปริมาณรายวันของ 0.5 มก.
ในการศึกษาในสัตว์ทดลอง ไม่พบ fingolimod ว่าเป็นสารก่อกลายพันธุ์หรือ clastogenic
Fingolimod ไม่มีผลต่อจำนวนอสุจิ / การเคลื่อนไหวหรือความอุดมสมบูรณ์ของหนูเพศผู้และเพศเมียจนถึงขนาดยาที่ทดสอบสูงสุด (10 มก. / กก.) ซึ่งแสดงถึงระยะขอบประมาณ 150 เท่าของการได้รับสัมผัสทั่วร่างกายของมนุษย์ (AUC) ที่ปริมาณ 0.5 ต่อวัน มก.
Fingolimod แสดงให้เห็นว่าเป็นสารก่อมะเร็งในหนูเมื่อให้ยาในขนาด 0.1 มก. / กก. หรือสูงกว่า ความผิดปกติของอวัยวะภายในของทารกในครรภ์ที่พบบ่อยที่สุด ได้แก่ หลอดเลือดแดงถาวรและข้อบกพร่องของผนังกั้นห้องล่างไม่สามารถประเมินศักยภาพในการทำให้ทารกอวัยวะพิการในกระต่ายได้เต็มที่ อย่างไรก็ตาม อัตราการเสียชีวิตของตัวอ่อนและทารกในครรภ์เพิ่มขึ้นในขนาด 1.5 มก. / กก. ขึ้นไป และการลดลงของทารกในครรภ์ที่มีชีวิตและการชะลอการเจริญเติบโตของทารกในครรภ์ที่ขนาด 5 มก. / กก. กก.
ในหนูแรท การรอดชีวิตของลูกสุนัขรุ่น F1 ลดลงในช่วงหลังคลอดในระยะแรกในปริมาณที่ไม่ก่อให้เกิดความเป็นพิษต่อมารดา อย่างไรก็ตาม รุ่น F1 ไม่ได้รับผลกระทบจากการรักษาด้วย fingolimod ในส่วนที่เกี่ยวกับน้ำหนักตัว พัฒนาการ พฤติกรรม และภาวะเจริญพันธุ์
Fingolimod ถูกขับออกมาในนมของสัตว์ที่ให้นมบุตรที่บำบัดแล้ว Fingolimod และสารเมตาบอลิซึมของ Fingolimod ข้ามอุปสรรครกในกระต่ายที่ตั้งครรภ์
การประเมินความเสี่ยงด้านสิ่งแวดล้อม (การประเมินความเสี่ยงด้านสิ่งแวดล้อม, เคยเป็น)
ไม่คาดว่าจะมีความเสี่ยงด้านสิ่งแวดล้อมจากการใช้ Gilenya โดยผู้ป่วยโรคปลอกประสาทเสื่อมแข็งที่กำเริบ
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
เนื้อหาแคปซูล:
แมกนีเซียมสเตียเรต
แมนนิทอล
เปลือกแคปซูล:
เหล็กออกไซด์สีเหลือง (E172)
ไทเทเนียมไดออกไซด์ (E171)
เยลลี่
หมึก:
แล็กเกอร์ (E904)
แอลกอฮอล์แห้ง
ไอโซโพรพิลแอลกอฮอล์
บิวทิลแอลกอฮอล์
โพรพิลีนไกลคอล
น้ำบริสุทธิ์
สารละลายแอมโมเนียเข้มข้น
โพแทสเซียมไฮดรอกไซด์
แบล็กไอรอนออกไซด์ (E172)
เหล็กออกไซด์สีเหลือง (E172)
ไทเทเนียมไดออกไซด์ (E171)
ไดเมทิโคน
06.2 ความเข้ากันไม่ได้
ไม่เกี่ยวข้อง
06.3 ระยะเวลาที่ใช้ได้
2 ปี.
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
อย่าเก็บที่อุณหภูมิสูงกว่า 25 องศาเซลเซียส
เก็บในบรรจุภัณฑ์เดิมเพื่อป้องกันตัวยาจากความชื้น
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
แพ็คที่ประกอบด้วยแคปซูลแข็ง 7, 28 หรือ 98 แคปซูลหรือหลายแพ็คที่มี 84 (3 แพ็คจาก 28) ใน PVC / PVDC / ตุ่มอลูมิเนียม
แพ็คที่บรรจุแคปซูลแข็งขนาด 7 x 1 ในตุ่มขนาดยาที่มีรูพรุนใน PVC / PVDC / อลูมิเนียม
ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
06.6 คำแนะนำในการใช้งานและการจัดการ
ไม่มีคำแนะนำพิเศษ
07.0 ผู้ทรงอำนาจการตลาด
บริษัท โนวาร์ทิส ยูโรฟาร์ม จำกัด
ถนนวิมเบิลเฮิรสต์
ฮอร์แชม
West Sussex, RH12 5AB
สหราชอาณาจักร
08.0 หมายเลขอนุญาตการตลาด
EU / 1/11/677 / 001-006
040949012
040949024
040949036
040949048
040949051
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
17.03.2011
10.0 วันที่แก้ไขข้อความ
มิถุนายน 2014