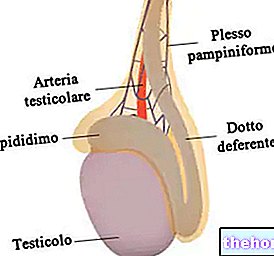
โครงสร้างและหน้าที่
เฮโมโกลบินเป็นเมทัลโลโปรตีนที่มีอยู่ในเซลล์เม็ดเลือดแดงซึ่งมีหน้าที่ขนส่งออกซิเจนในกระแสเลือด อันที่จริง ออกซิเจนละลายได้ในน้ำปานกลางเท่านั้น ดังนั้นปริมาณที่ละลายในเลือด (น้อยกว่า 2% ของทั้งหมด) จึงไม่เพียงพอที่จะตอบสนองความต้องการเมตาบอลิซึมของเนื้อเยื่อ ความจำเป็นในการเป็นพาหะเฉพาะจึงชัดเจน
ในกระแสเลือด ออกซิเจนไม่สามารถจับโดยตรงและย้อนกลับกับโปรตีนได้ เช่น เกิดขึ้นแทนสำหรับโลหะ เช่น ทองแดงและเหล็ก ไม่น่าแปลกใจที่จุดศูนย์กลางของหน่วยย่อยโปรตีนแต่ละหน่วยของเฮโมโกลบินที่ห่อหุ้มด้วยเปลือกโปรตีน เราพบสิ่งที่เรียกว่าอวัยวะเทียม กลุ่ม EME โดยมีหัวใจโลหะแทนด้วยอะตอมของเหล็กในสถานะ Fe2 + ออกซิเดชัน (สถานะลดลง) ซึ่งจับออกซิเจนในลักษณะย้อนกลับได้
การตรวจเลือด
- ค่าฮีโมโกลบินปกติในเลือด: 13-17 g / 100 ml
ในผู้หญิงค่าจะต่ำกว่าผู้ชายโดยเฉลี่ย 5-10%
สาเหตุที่เป็นไปได้ของฮีโมโกลบินสูง
- Polycythemias
- พักระยะยาวบนที่สูง
- โรคปอดเรื้อรัง
- โรคหัวใจ
- ยาสลบในเลือด (การใช้อีริโทรพอยอิตินและอนุพันธ์หรือสารที่เลียนแบบการกระทำของพวกมัน)
สาเหตุที่เป็นไปได้ของฮีโมโกลบินต่ำ
- โรคโลหิตจาง
- การขาดธาตุเหล็ก (การขาดธาตุเหล็ก)
- เลือดออกมาก
- มะเร็ง
- การตั้งครรภ์
- ธาลัสซีเมีย
- เบิร์นส์
ปริมาณออกซิเจนในเลือดจึงถูกกำหนดโดยผลรวมของปริมาณเล็กน้อยที่ละลายในพลาสมาโดยมีส่วนจับกับธาตุเหล็กเฮโมโกลบิน
ออกซิเจนในเลือดมากกว่า 98% จับกับฮีโมโกลบินซึ่งจะหมุนเวียนในกระแสเลือดที่จัดสรรไว้ภายในเซลล์เม็ดเลือดแดง หากไม่มีฮีโมโกลบิน เม็ดเลือดแดงจะไม่สามารถทำหน้าที่ลำเลียงออกซิเจนในเลือดได้
ด้วยบทบาทสำคัญของโลหะนี้ การสังเคราะห์ฮีโมโกลบินจึงจำเป็นต้องได้รับธาตุเหล็กในอาหารอย่างเพียงพอ ธาตุเหล็กประมาณ 70% ในร่างกายมีอยู่ในกลุ่มฮีโมโกลบิน
เฮโมโกลบินประกอบด้วย 4 หน่วยย่อยที่มีโครงสร้างคล้ายกับ myoglobin *
* ในขณะที่เฮโมโกลบินขนส่งออกซิเจนจากปอดไปยังเนื้อเยื่อ ไมโอโกลบินจะนำออกซิเจนที่ปล่อยออกมาจากเฮโมโกลบินไปยังอวัยวะต่างๆ ของเซลล์ที่ใช้ออกซิเจน (เช่น ไมโตคอนเดรีย)

เฮโมโกลบินเป็นเมทัลโลโปรตีนขนาดใหญ่และซับซ้อน โดยมีลักษณะเป็นสายโปรตีนทรงกลมสี่สายที่พันรอบกลุ่มฮีมที่มี Fe2 + ตามลำดับ
สำหรับแต่ละโมเลกุลของเฮโมโกลบิน เราจึงพบกลุ่มฮีมสี่กลุ่มที่ห่อหุ้มด้วยสายโปรตีนทรงกลมที่สัมพันธ์กัน เนื่องจากมีธาตุเหล็กสี่อะตอมในแต่ละโมเลกุลของฮีโมโกลบิน โมเลกุลของเฮโมโกลบินแต่ละโมเลกุลสามารถจับอะตอมออกซิเจนสี่ตัวเข้ากับตัวมันเองได้ตามปฏิกิริยาที่ผันกลับได้:
Hb + 4O2 ← → Hb (O2) 4
อย่างที่ทราบกันดีว่าหน้าที่ของเฮโมโกลบินคือการนำออกซิเจนในปอด ปล่อยไปยังเซลล์ที่ต้องการ นำคาร์บอนไดออกไซด์ออกจากร่างกายและปล่อยเข้าสู่ปอดโดยที่ chilo เริ่มต้นอีกครั้ง
ในระหว่างทางเดินของเลือดในเส้นเลือดฝอยของถุงลมปอด เฮโมโกลบินจับออกซิเจนกับตัวมันเอง ซึ่งต่อมาจะปล่อยไปยังเนื้อเยื่อในระบบไหลเวียนรอบข้าง การแลกเปลี่ยนนี้เกิดขึ้นเนื่องจากพันธะของออกซิเจนกับธาตุเหล็กของกลุ่ม EME นั้นไม่ชัดเจนและไวต่อปัจจัยหลายประการ ที่สำคัญที่สุดคือความตึงเครียดหรือความดันบางส่วนของออกซิเจน
การผูกมัดของออกซิเจนกับเฮโมโกลบินและผลกระทบของบอร์
ในปอดความตึงเครียดของออกซิเจนในพลาสมาเพิ่มขึ้นเนื่องจากการแพร่กระจายของก๊าซจากถุงลมไปยังเลือด (↑ PO2); การเพิ่มขึ้นนี้ทำให้เฮโมโกลบินจับกับออกซิเจนอย่างกระตือรือร้น ตรงกันข้ามเกิดขึ้นในเนื้อเยื่อส่วนปลายซึ่งความเข้มข้นของออกซิเจนที่ละลายในเลือดลดลง (↓ PO2) และความดันบางส่วนของคาร์บอนไดออกไซด์เพิ่มขึ้น (↑ CO2) สิ่งนี้กระตุ้นให้เฮโมโกลบินปล่อยออกซิเจนและกลายเป็นประจุ CO2 ทำให้แนวคิดเรียบง่ายที่สุด ยิ่งมีคาร์บอนไดออกไซด์ในเลือดมากเท่าไร ออกซิเจนก็จะยิ่งจับกับฮีโมโกลบินน้อยลงเท่านั้น.
แม้ว่าปริมาณออกซิเจนที่ละลายในเลือดในร่างกายจะต่ำมาก แต่ก็มีบทบาทพื้นฐาน ในความเป็นจริง ปริมาณนี้มีอิทธิพลอย่างมากต่อความแข็งแรงพันธะระหว่างออกซิเจนและฮีโมโกลบิน (รวมทั้งแสดงถึง "ค่าอ้างอิงที่สำคัญในการควบคุมการช่วยหายใจในปอด)
เมื่อสรุปทุกอย่างด้วยกราฟ ปริมาณออกซิเจนที่เชื่อมโยงกับฮีโมโกลบินจะเพิ่มขึ้นเมื่อเทียบกับ pO2 ตามเส้นโค้งซิกมอยด์:

ความจริงที่ว่าบริเวณที่ราบสูงนั้นใหญ่มากทำให้ขอบความปลอดภัยที่สำคัญที่ความอิ่มตัวสูงสุดของเฮโมโกลบินระหว่างทางเข้าสู่ปอด แม้ว่า pO2 ที่ระดับถุงปกติจะเท่ากับ 100 มม. ปรอท การสังเกตจากตัวเลขที่เราสังเกตในความเป็นจริง แม้แต่ความดันบางส่วนของออกซิเจนเท่ากับ 70 mmHg (การเกิดโรคโดยทั่วไปหรืออยู่ที่ระดับความสูง) เปอร์เซ็นต์ของฮีโมโกลบินอิ่มตัวยังคงใกล้เคียงกับ 100%
ในบริเวณที่มีความลาดชันสูงสุด เมื่อความตึงบางส่วนของออกซิเจนลดลงต่ำกว่า 40 mmHg ความสามารถของฮีโมโกลบินในการจับออกซิเจนจะลดลงอย่างกะทันหัน
ในสภาวะการพักผ่อน PO2 ในของเหลวภายในเซลล์จะอยู่ที่ประมาณ 40 mmHg; ในตำแหน่งนี้เนื่องจากกฎของแก๊สออกซิเจนที่ละลายในพลาสมาจะแพร่กระจายไปยังเนื้อเยื่อที่ด้อยกว่าของ O2 ผ่านเยื่อหุ้มเส้นเลือดฝอย ดังนั้น ความตึงในพลาสมาของ O2 จะลดลงไปอีกและทำให้เกิดการปลดปล่อยออกซิเจนจากฮีโมโกลบิน . ในทางกลับกัน ความตึงเครียดของออกซิเจนในเนื้อเยื่อจะลดลงเหลือ 15 mmHg หรือน้อยกว่านั้น ในระหว่างการออกแรงทางกายภาพอย่างรุนแรง ส่งผลให้ออกซิเจนในเลือดลดลงอย่างมาก
อย่างที่กล่าวไปแล้ว ในสภาพการพักผ่อน ปริมาณออกซิเจนเฮโมโกลบินที่สำคัญจะออกจากเนื้อเยื่อ เหลือไว้ใช้ในกรณีจำเป็น (เช่น เพื่อจัดการกับการเผาผลาญที่เพิ่มขึ้นอย่างกะทันหันในเซลล์บางเซลล์)
เส้นทึบที่แสดงในภาพด้านบนเรียกว่าเส้นโค้งการแยกตัวของฮีโมโกลบิน โดยทั่วไปจะถูกกำหนด ในหลอดทดลอง ที่ pH 7.4 และที่อุณหภูมิ 37 ° C
ผลกระทบของบอร์มีผลทั้งต่อการบริโภค O2 ที่ระดับปอดและการปล่อยออกที่ระดับเนื้อเยื่อ
ในที่ที่มีคาร์บอนไดออกไซด์ละลายน้ำมากกว่าในรูปของไบคาร์บอเนต เฮโมโกลบินจะปล่อยออกซิเจนได้ง่ายขึ้นและกลายเป็นประจุด้วยคาร์บอนไดออกไซด์ (ในรูปของไบคาร์บอเนต)

ผลเช่นเดียวกันนี้ได้มาจากการทำให้เลือดเป็นกรด ยิ่งค่า pH ของเลือดลดลงและออกซิเจนยังคงจับกับฮีโมโกลบินน้อยลง ไม่น่าแปลกใจที่คาร์บอนไดออกไซด์ในเลือดจะละลายส่วนใหญ่อยู่ในรูปของกรดคาร์บอนิกซึ่งแยกตัวออกจากกัน



เพื่อเป็นเกียรติแก่ผู้ค้นพบ ผลของ pH หรือคาร์บอนไดออกไซด์ต่อการแยกตัวของออกซิเจนเรียกว่าผลกระทบจากบอร์
ตามที่คาดไว้ ในสภาพแวดล้อมที่เป็นกรด เฮโมโกลบินจะปล่อยออกซิเจนได้ง่ายกว่า ในขณะที่ในสภาพแวดล้อมพื้นฐาน พันธะกับออกซิเจนจะแข็งแกร่งกว่า

ปัจจัยอื่นๆ ที่สามารถปรับเปลี่ยนความสัมพันธ์ของฮีโมโกลบินต่อออกซิเจน ได้แก่ อุณหภูมิ โดยเฉพาะอย่างยิ่ง ความสัมพันธ์ของฮีโมโกลบินกับออกซิเจนจะลดลงตามอุณหภูมิของร่างกายที่เพิ่มขึ้น ซึ่งเป็นประโยชน์อย่างยิ่งในช่วงฤดูหนาวและฤดูใบไม้ผลิ เนื่องจากอุณหภูมิของเลือดในปอด (เมื่อสัมผัสกับเลือดในปอด) อากาศของสภาพแวดล้อมภายนอก) ต่ำกว่าที่ไปถึงเนื้อเยื่อซึ่งจะช่วยอำนวยความสะดวกในการปล่อยออกซิเจน

2.3 ไดฟอสโฟกลีเซอเรตเป็นสารตัวกลางในไกลโคไลซิสที่ส่งผลต่อความสัมพันธ์ของฮีโมโกลบินกับออกซิเจน หากความเข้มข้นภายในเซลล์เม็ดเลือดแดงเพิ่มขึ้น ความสัมพันธ์ของฮีโมโกลบินต่อออกซิเจนจะลดลง ซึ่งจะทำให้ออกซิเจนไปยังเนื้อเยื่อได้ง่ายขึ้น ไม่น่าแปลกใจที่ความเข้มข้นของเม็ดเลือดแดง ไดฟอสโฟกลีเซอเรตเพิ่มขึ้น 2,3 เช่น ในภาวะโลหิตจาง ภาวะหัวใจและปอดไม่เพียงพอ และระหว่างอยู่ในระดับความสูงที่สูง
โดยทั่วไป ผลของ 2,3 bisphosphoglycerate จะค่อนข้างช้า โดยเฉพาะอย่างยิ่งเมื่อเทียบกับการตอบสนองอย่างรวดเร็วต่อการเปลี่ยนแปลงของ pH อุณหภูมิ และความดันบางส่วนของคาร์บอนไดออกไซด์

ผลของบอร์มีความสำคัญมากในระหว่างการทำงานของกล้ามเนื้อที่รุนแรง ในสภาวะดังกล่าว อันที่จริง ในเนื้อเยื่อที่สัมผัสกับความเครียดมากที่สุด อุณหภูมิและความดันของคาร์บอนไดออกไซด์ในท้องถิ่นจะเพิ่มขึ้น ดังนั้น ความเป็นกรดในเลือด ตามที่อธิบายไว้ข้างต้น ทั้งหมดนี้สนับสนุนการปล่อยออกซิเจนไปยังเนื้อเยื่อ โดยเปลี่ยนเส้นโค้งการแยกตัวของฮีโมโกลบินไปทางขวา