เพื่อให้สามารถพูดในลักษณะที่เข้าใจได้ของ "เฮโมโกลบิน (Hb),มันมีประโยชน์ในการดูแลครั้งแรก ไมโอโกลบิน (Mb) ซึ่งคล้ายกับเฮโมโกลบินมากแต่ง่ายกว่ามาก ระหว่างเฮโมโกลบินและไมโอโกลบินมีความสัมพันธ์ทางเครือญาติใกล้ชิด: ทั้งสองเป็นโปรตีนคอนจูเกตและกลุ่มเทียม (ส่วนที่ไม่ใช่โปรตีน) เป็นกลุ่ม heme.
Myoglobin เป็นโปรตีนทรงกลมที่ประกอบด้วยสายโซ่เดียวที่มีกรดอะมิโนประมาณหนึ่งร้อยห้าสิบตัว (ขึ้นอยู่กับสิ่งมีชีวิต) และมีน้ำหนักโมเลกุลประมาณ 18 Kd
ดังที่กล่าวไว้ มันถูกติดตั้งด้วยหมู่ heme ซึ่งสอดแทรกอยู่ในส่วนที่ไม่ชอบน้ำ (หรือไลโปฟิลิก) ของโปรตีน ซึ่งประกอบด้วยส่วนพับที่เกี่ยวข้องกับโครงสร้าง α-helix ของโปรตีนเส้นใย
Myoglobin ประกอบด้วยส่วนของ α-helices เป็นหลัก ซึ่งมีอยู่ในจำนวนแปดส่วนและประกอบด้วยสารตกค้างที่ไม่มีขั้วเกือบทั้งหมด (leucine, valine, methionine และ phenylalanine) ในขณะที่ไม่มีขั้วตกค้าง (aspartic acid, glutamic acid, lysine และอาร์จินีน); สารตกค้างเพียงขั้วเดียวคือฮิสทิดีนสองตัวซึ่งมีบทบาทสำคัญในการยึดออกซิเจนกับกลุ่มฮีม
กลุ่ม heme เป็นกลุ่ม chromophore (ดูดซับในสิ่งที่มองเห็นได้) และเป็นกลุ่มการทำงานของ myoglobin
ดูเพิ่มเติม: glycated hemoglobin - hemoglobin ในปัสสาวะ
เคมีนิดหน่อย

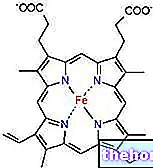
พันธะระหว่างโปรโตพอร์ไฟรินกับธาตุเหล็กเป็นพันธะทั่วไปของสารประกอบโคออร์ดิเนตซึ่งเป็นสารประกอบทางเคมีซึ่งอะตอมกลาง (หรือไอออน) ก่อตัวพันธะกับสารเคมีชนิดอื่นๆ ในจำนวนที่มากกว่าเลขออกซิเดชัน (ประจุไฟฟ้า) ในกรณีของ heme พันธะเหล่านี้จะย้อนกลับได้และอ่อนแอ
หมายเลขประสานงาน (จำนวนพันธะประสานงาน) ของเหล็กคือหก: สามารถมีโมเลกุลได้ 6 ตัวรอบ ๆ เหล็กซึ่งใช้อิเล็กตรอนร่วมกัน
ในการสร้างสารประกอบประสานงานนั้น ต้องใช้ออร์บิทัลสองออร์บิทัลที่มีทิศทางที่ถูกต้อง: อันหนึ่งสามารถ "รับ" อิเล็กตรอนได้ และอีกอันสามารถบริจาคได้
ใน heme ธาตุเหล็กสร้างพันธะระนาบสี่พันธะที่มีอะตอมไนโตรเจนสี่อะตอมที่ศูนย์กลางของวงแหวนโปรโต-พอร์ไฟริน และพันธะที่ห้าที่มีไนโตรเจนฮิสทิดีนใกล้เคียง เหล็กมีพันธะประสานอิสระลำดับที่หก และสามารถจับกับออกซิเจนได้
เมื่อเหล็กอยู่ในรูปของไอออนอิสระ ออร์บิทัลของธาตุเหล็ก NS พวกเขาทั้งหมดมีพลังงานเท่ากัน ใน myoglobin ไอออนของเหล็กจะจับกับโปรโตพอร์ไฟรินและฮิสติดีน: สปีชีส์เหล่านี้รบกวนออร์บิทัลด้วยสนามแม่เหล็ก NS เหล็กบาง; ขอบเขตของการก่อกวนจะแตกต่างกันสำหรับออร์บิทัลต่างๆ NS ขึ้นอยู่กับการวางแนวของพื้นที่และของสายพันธุ์ที่ก่อกวน เนื่องจากพลังงานทั้งหมดของออร์บิทัลจะต้องคงที่ การก่อกวนทำให้เกิดการแยกกันอย่างมีพลังระหว่างออร์บิทัลต่างๆ: พลังงานที่ออร์บิทัลบางส่วนได้มานั้นเทียบเท่ากับพลังงานที่ออร์บิทัลอื่นๆ สูญเสียไป
ถ้าการแยกตัวที่เกิดขึ้นระหว่างออร์บิทัลมีขนาดไม่ใหญ่มาก ควรใช้การจัดเรียงแบบอิเล็กทรอนิกส์ที่มีสปินสูง: อิเล็กตรอนที่ยึดจับจะพยายามจัดเรียงตัวเองในสปินคู่ขนานในระดับย่อยให้ได้มากที่สุด (หลายหลากสูงสุด) ในทางกลับกัน ถ้าการก่อกวนรุนแรงมากและมีช่องว่างขนาดใหญ่ระหว่างออร์บิทัล การจับคู่อิเล็กตรอนพันธะในออร์บิทัลพลังงานต่ำ (สปินต่ำ) อาจสะดวกกว่า
เมื่อเหล็กจับกับออกซิเจน โมเลกุลจะถือว่ามีการจัดหมุนต่ำในขณะที่เหล็กมีพันธะประสานที่หกฟรี โมเลกุลจะมีการจัดการหมุนสูง
ด้วยความแตกต่างของการหมุนนี้ ผ่านการวิเคราะห์สเปกตรัมของ myoglobin เราจึงสามารถเข้าใจได้ว่าออกซิเจน (MbO2) ถูกผูกไว้กับมันหรือไม่ (Mb)
Myoglobin เป็นโปรตีนจากกล้ามเนื้อทั่วไป (แต่ไม่พบในกล้ามเนื้อเท่านั้น)
Myoglobin ถูกสกัดจากวาฬสเปิร์มซึ่งมีอยู่ในปริมาณมากและทำให้บริสุทธิ์
สัตว์จำพวกวาฬมีการหายใจเหมือนมนุษย์: มีปอด พวกมันต้องดูดซับอากาศผ่านกระบวนการหายใจ วาฬสเปิร์มจะต้องนำออกซิเจนเข้าสู่กล้ามเนื้อให้มากที่สุดเท่าที่จะทำได้เพื่อสะสมออกซิเจนโดยผูกมัดกับไมโอโกลบินที่มีอยู่ในตัว จากนั้นออกซิเจนจะถูกปล่อยออกมาอย่างช้าๆ เมื่อจุ่มลงในสัตว์จำพวกวาฬ เพราะเมแทบอลิซึมของมันต้องใช้ออกซิเจน ยิ่งปริมาณมาก ของออกซิเจนที่วาฬสเปิร์มสามารถดูดซับและมีออกซิเจนมากขึ้นในระหว่างการดำน้ำ
Myoglybin จับออกซิเจนในลักษณะที่ย้อนกลับได้และมีอยู่ในเนื้อเยื่อส่วนปลายในเปอร์เซ็นต์ที่มากขึ้นยิ่งใช้เนื้อเยื่อในการทำงานกับอุปกรณ์ออกซิเจนที่อยู่ห่างไกลจากเวลามากขึ้น
<--- Myoglobin เป็นโปรตีนที่มีอยู่ในกล้ามเนื้อ ซึ่งมีหน้าที่เหมือนกับ "อ่างเก็บน้ำ" ออกซิเจน
สิ่งที่ทำให้เนื้อแดงมากหรือน้อยคือเนื้อหาของฮีโมโปรตีน (เป็นฮีมที่ทำให้เนื้อแดง)
เฮโมโกลบินมีโครงสร้างที่คล้ายคลึงกันหลายประการกับไมโอโกลบิน และสามารถจับโมเลกุลออกซิเจนในลักษณะย้อนกลับได้ แต่ในขณะที่ myoglobin ถูกกักขังอยู่ในกล้ามเนื้อและเนื้อเยื่อส่วนปลายโดยทั่วไป เฮโมโกลบินจะพบในเม็ดเลือดแดงหรือเซลล์เม็ดเลือดแดง (เป็นเซลล์หลอก กล่าวคือ ไม่ใช่เซลล์จริง) ซึ่งคิดเป็น 40% ของเลือด
ตรงกันข้ามกับไมโอโกลบิน การทำงานของเฮโมโกลบินคือการนำออกซิเจนในปอด ปล่อยเข้าไปในเซลล์ที่จำเป็น นำคาร์บอนไดออกไซด์และปล่อยเข้าสู่ปอดเมื่อวงจรเริ่มต้นขึ้นอีกครั้ง
แอล"เฮโมโกลบิน มันคือเตตระมิเตอร์ กล่าวคือ มันประกอบด้วยสายโพลีเปปไทด์สี่สายแต่ละสายมีหมู่ฮีมและเหมือนกันสองต่อสอง (ในมนุษย์มีสายอัลฟาสองสายและสายเบตาสองสาย)
หน้าที่หลักของเฮโมโกลบินคือการขนส่งออกซิเจน หน้าที่อื่นของเลือดที่เกี่ยวข้องกับเฮโมโกลบินคือการขนส่งสารไปยังเนื้อเยื่อ
ในเส้นทางจากปอด (อุดมไปด้วยออกซิเจน) ไปยังเนื้อเยื่อ เฮโมโกลบินนำออกซิเจน (ในขณะเดียวกันสารอื่นๆ ไปถึงเนื้อเยื่อ) ในขณะที่เส้นทางกลับกัน จะนำของเสียที่เนื้อเยื่อเก็บสะสมไว้ไปด้วย โดยเฉพาะคาร์บอน ไดออกไซด์ที่ผลิตขึ้นในการเผาผลาญ
ในการพัฒนามนุษย์นั้นมียีนที่แสดงออกในช่วงระยะเวลาหนึ่งเท่านั้น ด้วยเหตุนี้จึงมีฮีโมโกลบินที่แตกต่างกัน: ทารกในครรภ์, ตัวอ่อน, ของผู้ใหญ่
สายโซ่ที่ประกอบกันเป็นเฮโมโกลบินที่แตกต่างกันเหล่านี้มีโครงสร้างที่แตกต่างกัน แต่ด้วยความคล้ายคลึงกันบางประการที่จริงแล้วหน้าที่ของฮีโมโกลบินนั้นเหมือนกันมากหรือน้อย
คำอธิบายของการมีอยู่ของสายโซ่ที่แตกต่างกันหลายสายมีดังต่อไปนี้: ในกระบวนการวิวัฒนาการของสิ่งมีชีวิต แม้แต่เฮโมโกลบินก็มีวิวัฒนาการที่เชี่ยวชาญในการขนส่งออกซิเจนจากพื้นที่ที่อุดมไปด้วยไปยังพื้นที่ที่ขาดแคลน ของสายวิวัฒนาการ l" เฮโมโกลบินขนส่งออกซิเจนในสิ่งมีชีวิตขนาดเล็ก ในระหว่างการวิวัฒนาการ สิ่งมีชีวิตถึงขนาดที่ใหญ่ขึ้น ดังนั้นเฮโมโกลบินจึงถูกดัดแปลงเพื่อให้สามารถขนส่งออกซิเจนไปยังพื้นที่ที่อยู่ไกลจากจุดที่มันอุดมไปด้วย; เป็น การทำเช่นนี้พวกเขาได้รับการเข้ารหัสในระหว่างกระบวนการวิวัฒนาการโครงสร้างใหม่ของสายโซ่ที่ประกอบเป็นเฮโมโกลบิน
Myoglobin จับออกซิเจนแม้ในความกดดันเล็กน้อยในเนื้อเยื่อส่วนปลายมีความดัน (PO2) ประมาณ 30 mmHg: myoglobin ที่ความดันนี้ไม่ปล่อยออกซิเจนดังนั้นจึงไม่มีประสิทธิภาพในการเป็นพาหะของออกซิเจน ในทางกลับกัน เฮโมโกลบิน มันมีพฤติกรรมที่ยืดหยุ่นกว่า: มันจับออกซิเจนกับแรงกดดันสูงและปล่อยออกเมื่อความดันลดลง
เมื่อโปรตีนทำงานตามหน้าที่ มันสามารถเปลี่ยนแปลงรูปร่างได้เล็กน้อย ตัวอย่างเช่น myoglobin ที่เติมออกซิเจนมีรูปร่างที่แตกต่างจาก myoglobin ที่ไม่มีออกซิเจนและการกลายพันธุ์นี้ไม่ส่งผลกระทบต่อเพื่อนบ้าน
สถานการณ์จะแตกต่างไปจากกรณีของโปรตีนที่เกี่ยวข้อง เช่น เฮโมโกลบิน: เมื่อโซ่ออกซิเจนถูกเหนี่ยวนำให้เปลี่ยนรูปร่างแต่การปรับเปลี่ยนนี้เป็นสามมิติดังนั้นสายโซ่อื่นๆ ของเตตระมิเตอร์ก็ได้รับผลกระทบเช่นกัน ซึ่งกันและกัน , แสดงให้เห็นว่าการปรับเปลี่ยนของหนึ่งส่งผลกระทบต่อเพื่อนบ้านอื่น ๆ แม้ว่าจะมีขอบเขตที่แตกต่างกัน เมื่อโซ่ให้ออกซิเจน โซ่อื่น ๆ ของ tetrameter จะถือว่า "ทัศนคติที่ไม่เป็นมิตรน้อยกว่า" ต่อออกซิเจน: ความยากลำบากในการเชื่อมโยง ออกซิเจนจะลดลงเมื่อโซ่ใกล้กับออกซิเจนในทางกลับกัน เช่นเดียวกันสำหรับ deoxygenation
โครงสร้างควอเทอร์นารีของดีออกซีเฮโมโกลบินเรียกว่ารูปแบบ T (ตึงเครียด) ในขณะที่ออกซีเฮโมโกลบินเรียกว่ารูปแบบ R (ปล่อย) ในสภาวะตึงเครียดมีชุดของปฏิกิริยาไฟฟ้าสถิตที่ค่อนข้างแรงระหว่างกรดอะมิโนที่เป็นกรดและกรดอะมิโนพื้นฐานที่นำไปสู่โครงสร้างที่เข้มงวดของดีออกซีเฮโมโกลบิน (นี่คือสาเหตุที่ "รูปแบบตึงเครียด") ในขณะที่เมื่อออกซิเจนเชื่อมโยงกัน เอนทิตีของสิ่งเหล่านี้ การโต้ตอบลดลง (ด้วยเหตุนี้ "แบบฟอร์มเผยแพร่") ยิ่งไปกว่านั้น ในกรณีที่ไม่มีออกซิเจน ประจุของฮิสทิดีน (ดูโครงสร้าง) จะเสถียรโดยประจุตรงข้ามของกรดแอสปาร์ติก ในขณะที่เมื่อมีออกซิเจน มีแนวโน้มที่โปรตีนจะสูญเสียโปรตอน ทั้งหมดนี้เกี่ยวข้องกับว่าเฮโมโกลบินที่เติมออกซิเจนนั้นเป็นกรดที่แรงกว่าเฮโมโกลบินที่เติมออกซิเจน: บอร์เอฟเฟค.
ขึ้นอยู่กับค่า pH กลุ่มฮีมจับกับออกซิเจนได้ง่ายกว่าหรือน้อยลง: ในสภาพแวดล้อมที่เป็นกรด ฮีโมโกลบินจะปล่อยออกซิเจนได้ง่ายขึ้น (รูปแบบตึงเครียดจะคงที่) ในขณะที่ในสภาพแวดล้อมพื้นฐาน พันธะกับออกซิเจนจะทำได้ยากขึ้น

เฮโมโกลบินแต่ละตัวจะปล่อยโปรตอน 0.7 ต่อโมลของออกซิเจน (O2) ที่ป้อน
ผลของบอร์ช่วยให้เฮโมโกลบินปรับปรุงความสามารถในการขนส่งออกซิเจน
ฮีโมโกลบินที่เดินทางจากปอดไปยังเนื้อเยื่อต้องปรับสมดุลตัวเองตามหน้าที่ของความดัน ค่า pH และอุณหภูมิ
มาดูผลกระทบของอุณหภูมิกัน
อุณหภูมิในถุงลมในปอดนั้นต่ำกว่าอุณหภูมิภายนอกประมาณ 1-1.5 ° C ในขณะที่อุณหภูมิในกล้ามเนื้ออยู่ที่ประมาณ 36.5-37 ° C เมื่ออุณหภูมิเพิ่มขึ้น ปัจจัยความอิ่มตัวจะลดลง (ที่ความดันเดียวกัน): สิ่งนี้เกิดขึ้นเนื่องจากพลังงานจลน์เพิ่มขึ้นและการแยกตัวเป็นที่ชื่นชอบ

มีปัจจัยอื่นๆ ที่อาจส่งผลต่อความสามารถของฮีโมโกลบินในการจับกับออกซิเจน ซึ่งหนึ่งในนั้นคือความเข้มข้นของ 2,3 bisphosphoglycerate
2,3 bisphosphoglycerate เป็นเมแทบอลิซึมที่มีอยู่ในเม็ดเลือดแดงที่มีความเข้มข้น 4-5 mM (ในส่วนอื่น ๆ ของร่างกายไม่มีความเข้มข้นสูงเช่นนี้)
ที่ pH ทางสรีรวิทยา 2,3 bisphosphoglycerate จะถูกลดโปรตอนและมีประจุลบห้าตัว มันถูกเชื่อมระหว่างสายเบต้าสองสายของเฮโมโกลบินเนื่องจากสายเหล่านี้มีความเข้มข้นสูงของประจุบวก ปฏิกิริยาทางไฟฟ้าสถิตระหว่างสายเบตาและ 2,3 บิสฟอสโฟกลีเซอเรตทำให้เกิดความแข็งแกร่งในระบบ: ได้โครงสร้างที่ตึงเครียดซึ่งสัมพันธ์กับออกซิเจนเพียงเล็กน้อย ในระหว่างการให้ออกซิเจน บิสฟอสโฟกลีเซอเรต 2,3 จะถูกขับออก
ในเม็ดเลือดแดง c "เป็นเครื่องมือพิเศษที่แปลง 1,3 bisphosphoglycerate (ผลิตโดยเมแทบอลิซึม) เป็น 2,3 bisphosphoglycerate เพื่อให้มีความเข้มข้น 4-5 mM ดังนั้นเฮโมโกลบินจึงสามารถแลกเปลี่ยน "ออกซิเจนในเนื้อเยื่อได้
ฮีโมโกลบินที่มาถึงเนื้อเยื่ออยู่ในสถานะที่ปล่อยออกมา (จับกับออกซิเจน) แต่ในบริเวณใกล้เคียงของเนื้อเยื่อ มันถูกคาร์บอกซิเลตและผ่านไปยังสภาวะตึงเครียด: โปรตีนในสถานะนี้มีแนวโน้มที่จะจับกับออกซิเจนน้อยลงด้วยความเคารพ สู่สถานะที่ปล่อยออกมาดังนั้นเฮโมโกลบินจึงปล่อยออกซิเจนไปยังเนื้อเยื่อ นอกจากนี้ โดยปฏิกิริยาระหว่างน้ำและคาร์บอนไดออกไซด์ มีการผลิตไอออน H + ดังนั้นจึงมีออกซิเจนเพิ่มขึ้นเนื่องจากผลของบอร์
คาร์บอนไดออกไซด์แพร่กระจายเข้าสู่เม็ดเลือดแดงที่ผ่านเยื่อหุ้มพลาสมา เนื่องจากเม็ดเลือดแดงประกอบด้วยเลือดประมาณ 40% เราควรคาดหวังว่าจะมีคาร์บอนไดออกไซด์เพียง 40% ที่กระจายจากเนื้อเยื่อเข้าสู่เซลล์ จริงๆ แล้ว 90% ของคาร์บอนไดออกไซด์จะเข้าสู่เม็ดเลือดแดงเพราะมีเอนไซม์ที่เปลี่ยนคาร์บอนไดออกไซด์ ในกรดคาร์บอนิก ส่งผลให้ความเข้มข้นคงที่ของคาร์บอนไดออกไซด์ในเม็ดเลือดแดงอยู่ในระดับต่ำ ดังนั้นอัตราการเข้าจึงสูง

ปรากฏการณ์อีกประการหนึ่งที่เกิดขึ้นเมื่อเม็ดเลือดแดงไปถึงเนื้อเยื่อคือ: โดยการไล่ระดับ "HCO3- (อนุพันธ์ของคาร์บอนไดออกไซด์) ออกจาก" เม็ดเลือดแดง และเพื่อให้สมดุลกับประจุลบ เรามี " รายการของคลอไรด์ซึ่ง กำหนดการเพิ่มขึ้นของแรงดันออสโมติก: เพื่อความสมดุลของรูปแบบนี้ยังมีการเข้าสู่น้ำซึ่งทำให้เกิดการบวมของเม็ดเลือดแดง (ผล HAMBURGER) ปรากฏการณ์ตรงกันข้ามเกิดขึ้นเมื่อเม็ดเลือดแดงไปถึงถุงลมปอด: ภาวะเงินฝืดของเม็ดเลือดแดง (ผล HALDANE) ดังนั้นเม็ดเลือดแดง (มุ่งตรงไปยังปอด) จึงกลมกว่าหลอดเลือดแดง

























-e-trattamento-con-il-taping-kinesiologico-.jpg)