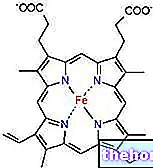
กรดอะมิโนและโปรตีนเป็นตัวกลางในการผ่านจากโลกแร่ไปสู่สิ่งมีชีวิต
ตามชื่อที่บ่งบอก กรดอะมิโนเป็นสารอินทรีย์สองฟังก์ชัน: ประกอบด้วยฟังก์ชันอะมิโน (-NH2) และฟังก์ชันคาร์บอกซิล (-COOH); พวกเขาสามารถเป็น α, β, γ ฯลฯ ขึ้นอยู่กับตำแหน่งที่ครอบครองโดยหมู่อะมิโนเทียบกับหมู่คาร์บอกซี:



กรดอะมิโนที่มีความสำคัญทางชีววิทยาคือกรดอัลฟาอะมิโนทั้งหมด
โครงสร้างโปรตีนประกอบด้วยกรดอะมิโน 20 ชนิด
ดังที่เห็นได้จากโครงสร้างทั่วไปที่แสดงไว้ข้างต้น กรดอะมิโนทั้งหมดมีส่วนร่วมและส่วนอื่นที่กำหนดคุณลักษณะของพวกมัน (แสดงโดยทั่วไปด้วย R)
จากกรดอะมิโน 20 ชนิด มี 19 ชนิดที่แอคทีฟเชิงแสง (พวกมันเบี่ยงเบนระนาบของแสงโพลาไรซ์)
กรดอะมิโนส่วนใหญ่มีหมู่อะมิโนเพียงหมู่เดียวและคาร์บอกซิลหนึ่งตัวจึงถูกเรียกว่า กรดอะมิโนที่เป็นกลาง; ที่มีคาร์บอกซิลพิเศษเรียกว่า กรดอะมิโน ในขณะที่กลุ่มอะมิโนเสริมคือ กรดอะมิโนพื้นฐาน.
กรดอะมิโนเป็นของแข็งที่เป็นผลึกและมีความสามารถในการละลายน้ำได้ดี
การขาดกรดอะมิโนบางชนิดในอาหารทำให้เกิดการเปลี่ยนแปลงอย่างร้ายแรงในการพัฒนา อันที่จริง สิ่งมีชีวิตของมนุษย์ไม่สามารถสังเคราะห์กรดอะมิโนบางชนิดที่เรียกว่าจำเป็นได้อย่างแม่นยำ (ต้องใช้ร่วมกับอาหาร) ในขณะที่กรดอะมิโนสามารถผลิตได้เพียงกรดอะมิโนบางตัวเท่านั้น (กรดอะมิโนที่ไม่จำเป็น)
โรคหนึ่งอันเนื่องมาจากการขาดกรดอะมิโนที่จำเป็นคือโรคที่รู้จักกันในชื่อ kwashiorkor (คำที่มาจากภาษาแอฟริกันซึ่งแปลว่า "ที่หนึ่งและที่สอง"); โรคนี้ส่งผลกระทบต่อลูกคนหัวปีแต่หลังคลอดลูกคนที่สองเพราะลูกคนแรกขาดนมแม่ซึ่งมีโปรตีนในปริมาณที่เหมาะสม โรคนี้จึงแพร่หลายในหมู่ประชากรที่ขาดสารอาหารและเกี่ยวข้องกับอาการท้องร่วง การขาดความอยากอาหารซึ่งนำไปสู่ความอ่อนแอของสิ่งมีชีวิตอย่างต่อเนื่อง
ดังที่ได้กล่าวไปแล้ว กรดอะมิโนธรรมชาติ ยกเว้นไกลซีน (เป็นกรดเอ-อะมิโนที่มีไฮโดรเจนแทนที่จะเป็นหมู่ R และมีขนาดเล็กที่สุดในยี่สิบ) มีฤทธิ์ทางแสงเนื่องจากมีอสมมาตรอย่างน้อยหนึ่งตัว คาร์บอน. ในกรดอะมิโนธรรมชาติ โครงแบบสัมบูรณ์ของคาร์บอนอสมมาตรซึ่งเชื่อมโยงเฉพาะหมู่อะมิโนและคาร์บอกซีเท่านั้นที่เป็นของซีรีย์ L
กรด D-amino ไม่เคยเป็นส่วนหนึ่งของโครงสร้างของโปรตีน
เราจำได้ว่า:
DNA ---- การถอดรหัส→ m-RNA ---- การแปล→โปรตีน
การถอดรหัสสามารถเข้ารหัสเป็นกรดแอล-อะมิโน; กรดดี-อะมิโนสามารถบรรจุอยู่ในโครงสร้างที่ไม่ใช่โปรตีน (เช่น ในผนังเยื่อบุของแบคทีเรีย: ในแบคทีเรียไม่มี "ข้อมูลทางพันธุกรรมสำหรับการมีกรดดี-อะมิโนสำหรับบทบาทในการป้องกัน อย่างไรก็ตาม มี" ข้อมูลทางพันธุกรรมสำหรับเอนไซม์ ซึ่งจัดการกับผนังเยื่อบุของแบคทีเรีย)
กลับไปที่กรดอะมิโน: โครงสร้างที่แตกต่างกันของกลุ่ม R กำหนดลักษณะเฉพาะของกรดอะมิโนแต่ละชนิดและมีส่วนสนับสนุนเฉพาะในลักษณะของโปรตีน
ดังนั้นจึงคิดว่าจะแบ่งกรดอะมิโนตามลักษณะของหมู่ R:
กรดอะมิโนที่มีขั้วแต่ไม่มีประจุ:
ไกลซีน (R = H-)
ซีรีน (R = HO-CH2-)
ธรีโอนีนจำเป็น
ธรีโอนีนมีศูนย์กลางสมมาตรสองแห่ง: มีเพียง 2S, 3R ทรีโอนีนที่มีอยู่ในธรรมชาติ
ธรีโอนีนเป็นกรดอะมิโนจำเป็น (อย่าสับสนกับที่ขาดไม่ได้: กรดอะมิโนทั้งหมดมีความจำเป็น) จึงต้องรับประทานพร้อมกับอาหาร กล่าวคือ รับประทานอาหารที่มีส่วนประกอบดังกล่าว เพราะดังที่ได้กล่าวไปแล้วว่ามรดกทางพันธุกรรมไม่มีอยู่ใน เซลล์ของมนุษย์ สามารถผลิตกรดอะมิโนได้ (มรดกนี้มีอยู่ในพืชหลายชนิดและดีกว่า)
กลุ่มไฮดรอกซิลของซีรีนและทรีโอนีนสามารถทำให้เอสเทอริฟายด์ได้ด้วยกลุ่มฟอสโฟริล (ได้รับฟอสโฟเซอรีนและฟอสโฟทรีโอนีน) กระบวนการนี้เรียกว่า ฟอสโฟรีเลชั่น; ฟอสโฟรีเลชั่นใช้ในการแปลสัญญาณระหว่างภายในและภายนอกเซลล์
ซีสเตอีน (R = HS-CH2-)
ซัลเฟอร์ซิลของซิสเทอีนสามารถโปรตอนได้ง่ายกว่าไฮดรอกซิลของซีรีน: กำมะถันและออกซิเจนเป็นทั้งกลุ่มที่หก แต่กำมะถันสามารถออกซิไดซ์ได้ง่ายกว่าเพราะมีขนาดที่ใหญ่กว่า
ไทโรซีน [R = H2O- (C6H4) -CH2-]
เอ็นบี
(C6H4) = แหวนเบนซินไดแทนที่ได
เช่นเดียวกับซีรีนและทรีโอนีน ไฮดรอกซิลสามารถทำให้เกิดการเอสเทอริไฟด์ (ฟอสโฟรีเลต)แอสพาราจีน (R = NH2-CO-CH2-)
กลูตามีน (R = NH2-CO-CH2-CH2-)
กรดอะมิโนไม่มีขั้ว
มีกลุ่มด้านข้างไม่ชอบน้ำ ภายในคลาสนี้เราแยกแยะ:
อะลิฟาติก:
อะลานีน (R = CH3-)
วาลีน (R = (CH3) 2-CH-) จำเป็น
ลิวซีน (R = (CH3) 2-CH-CH2-) จำเป็น
ไอโซลิวซีน (R =
) จำเป็น
เมไทโอนีน (R = CH3-S-CH2-CH2-) จำเป็น
เยื่อหุ้มเซลล์ประกอบด้วยไขมันไบเลเยอร์ที่มีโปรตีนยึดเกาะด้วยคุณสมบัติไม่ชอบน้ำ ดังนั้นจึงประกอบด้วยอะลานีน วาลีน ไอโซลิวซีนและลิวซีน ในทางกลับกัน เมไทโอนีนเป็นกรดอะมิโนที่มักมีอยู่ในปริมาณเล็กน้อย (ประมาณ 1%)
โพรลีน
อะโรเมติก:
ฟีนิลอะลานีน (R = Ph-CH2-) Ph = ฟีนิล: เบนซีนโมโนแทนที่ที่จำเป็น
ทริปโตเฟน (R =
จำเป็น
กรดอะมิโนสองตัวนี้ เป็นอะโรมาติก ดูดซับใกล้รังสีอัลตราไวโอเลต (ประมาณ 300 นาโนเมตร) ดังนั้นจึงเป็นไปได้ที่จะใช้ประโยชน์จากเทคนิคของ UV spectrophotometry เพื่อกำหนดความเข้มข้นของโปรตีนที่รู้จักซึ่งมีกรดอะมิโนเหล่านี้
กรดอะมิโนที่มีประจุ
ในทางกลับกันพวกเขาจะแบ่งออกเป็น:
กรดอะมิโนที่เป็นกรด (มีขั้วเรซิดิวที่มีประจุลบที่ pH 7) เป็นเช่นนี้เพราะสามารถให้ประจุ H + บวกได้:
กรดแอสปาร์ติก
กรดกลูตามิก (R =
)
กรดอะมิโนเหล่านี้มาจากแอสพาราจีนและกลูตามีนตามลำดับ ทั้งสี่มีอยู่ในธรรมชาติและนี่หมายความว่า c "เป็นข้อมูลเฉพาะสำหรับแต่ละคน นั่นคือ c" เป็นแฝดสามหลักใน DNA ที่กำหนดรหัสสำหรับแต่ละคน
กรดอะมิโนพื้นฐาน (มีขั้วเรซิดิวที่มีประจุบวกที่ pH 7) เป็นเช่นนี้เพราะสามารถรับประจุ H + บวกได้:
ไลซีน (R =
) จำเป็น
อาร์จินีน (R =
)
ฮิสติดีน (R =
)
มีโปรตีนซึ่งมีอนุพันธ์ของกรดอะมิโนในสายโซ่ด้านข้าง ตัวอย่างเช่น อาจมีฟอสโฟเซอรีน (ไม่มีข้อมูลทางพันธุกรรมที่เข้ารหัสฟอสโฟเซอรีน มีเพียงซีรีน) ฟอสโฟเซอรีนเป็นการดัดแปลง หลังการแปล: หลังจากการสังเคราะห์โปรตีนเกิดขึ้น
DNA ---- การถอดรหัส→ m-RNA ---- การแปล→โปรตีน
การดัดแปลงหลังการแปลดังกล่าวสามารถเกิดขึ้นได้ที่สายด้านข้างของโปรตีน
ดูเพิ่มเติม: โปรตีน ดูที่เคมี