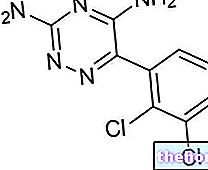
สารออกฤทธิ์: สตรอนเทียม (strontium ranelate)
OSSEOR เม็ด 2 กรัมสำหรับสารแขวนลอยในช่องปาก
เหตุใดจึงใช้ Osseor? มีไว้เพื่ออะไร?
OSSEOR เป็นยาที่ใช้รักษาโรคกระดูกพรุนขั้นรุนแรง:
- ในสตรีวัยหมดประจำเดือน
- ในผู้ชายที่เป็นผู้ใหญ่
มีความเสี่ยงสูงที่จะเกิดการแตกหักซึ่งไม่สามารถใช้การรักษาทางเลือกอื่นได้ ในสตรีวัยหมดประจำเดือน strontium ranelate ช่วยลดความเสี่ยงของกระดูกสันหลังและกระดูกสะโพกหัก
โรคกระดูกพรุน
ร่างกายจะทำลายกระดูกเก่าและสร้างกระดูกใหม่อย่างต่อเนื่อง ในกรณีของโรคกระดูกพรุน ร่างกายจะทำลายกระดูกมากกว่าที่ก่อตัว จึงค่อย ๆ สูญเสียมวลกระดูกและกระดูกจะบางลงและเปราะบางมากขึ้น โดยเฉพาะในสตรีหลังวัยหมดประจำเดือน
หลายคนที่เป็นโรคกระดูกพรุนไม่มีอาการใดๆ และเป็นไปไม่ได้ที่จะไม่รู้ด้วยซ้ำว่าคุณเป็นโรคกระดูกพรุน อย่างไรก็ตาม โรคกระดูกพรุนมีแนวโน้มที่จะกระดูกหัก (กระดูกหัก) โดยเฉพาะในกระดูกสันหลัง สะโพก และข้อมือ
OSSEOR ทำงานอย่างไร
OSSEOR ซึ่งมีสารออกฤทธิ์ strontium ranelate อยู่ในกลุ่มยาที่ใช้รักษาโรคกระดูก
OSSEOR ช่วยลดการทำลายกระดูกและกระตุ้นการสร้างกระดูกใหม่ ซึ่งจะช่วยลดความเสี่ยงของกระดูกหัก กระดูกใหม่ที่ก่อตัวขึ้นนั้นมีคุณภาพปกติ
ข้อห้าม เมื่อไม่ควรใช้ Osseor
อย่าใช้OSSEOR
- หากคุณแพ้สตรอนเทียมราเนเลตหรือส่วนผสมอื่นๆ ของ OSSEOR (ระบุไว้ในหัวข้อที่ 6)
- หากคุณมีหรือเคยเป็นลิ่มเลือดอุดตัน (เช่น ส่งผลต่อหลอดเลือดที่ขาหรือปอด)
- หากคุณถูกทำให้ไม่สามารถเคลื่อนไหวได้อย่างถาวรหรือเป็นระยะเวลาหนึ่ง เช่น ถ้าคุณอยู่ในรถเข็นคนพิการ หรือถ้าคุณติดเตียง หรือหากคุณต้องการเข้ารับการผ่าตัด หรือหากคุณอยู่ในระยะพักฟื้นหลังการผ่าตัด ความเสี่ยงของการเกิดลิ่มเลือดอุดตันในหลอดเลือดดำ (ลิ่มเลือดอุดตันที่ขาหรือปอด) อาจสูงขึ้นหากไม่สามารถเคลื่อนไหวได้เป็นเวลานาน
- หากคุณรู้จักโรคหัวใจขาดเลือดหรือโรคหลอดเลือดสมองเช่น หากคุณได้รับการวินิจฉัยว่ามีอาการหัวใจวาย โรคหลอดเลือดสมอง หรืออาการขาดเลือดชั่วคราว (ลดการไหลเวียนของเลือดไปยังสมองชั่วคราว หรือที่เรียกว่า "mini-stroke") โรคหลอดเลือดหัวใจตีบ หรือการอุดตันของหลอดเลือดในหัวใจหรือสมอง .
- หากคุณมีหรือมีปัญหากับการไหลเวียนโลหิต (โรคหลอดเลือดแดงส่วนปลาย) หรือถ้าคุณมีการผ่าตัดหลอดเลือดแดงที่ขา
- หากคุณมีความดันโลหิตสูงที่ไม่ได้ควบคุมโดยการรักษา
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนใช้ Osseor
พูดคุยกับแพทย์หรือเภสัชกรของคุณก่อนใช้ OSSEOR:
- หากคุณมีความเสี่ยงต่อโรคหัวใจ ได้แก่ ความดันโลหิตสูง คอเลสเตอรอลสูง เบาหวาน การสูบบุหรี่ - หากคุณมีความเสี่ยงที่จะเกิดลิ่มเลือดอุดตัน
- หากคุณมีโรคไตอย่างรุนแรง
แพทย์ของคุณจะประเมินสภาพของหัวใจและหลอดเลือดของคุณเป็นระยะ ๆ โดยปกติทุก 6 ถึง 12 เดือนตลอดระยะเวลาของการรักษาด้วย OSSEOR
ในระหว่างการรักษา หากเกิดอาการแพ้ (เช่น ใบหน้า ลิ้นหรือลำคอบวม หายใจลำบากหรือกลืนลำบาก มีผื่นที่ผิวหนัง) คุณควรหยุดใช้ OSSEOR ทันทีและติดต่อแพทย์ของคุณ (ดูหัวข้อ 4)
มีรายงานเกี่ยวกับผื่นผิวหนังที่อาจเป็นอันตรายถึงชีวิต (Stevens-Johnson Syndrome (SJS), toxic epidermal necrolysis และปฏิกิริยาภูมิไวเกินอย่างรุนแรง (DRESS)) ด้วยการใช้ OSSEOR
ความเสี่ยงสูงสุดของการเกิดปฏิกิริยาทางผิวหนังอย่างรุนแรงคือภายในสองสามสัปดาห์แรกของการรักษาโรคสตีเวนส์-จอห์นสันซินโดรมและภาวะเนื้อร้ายที่ผิวหนังชั้นนอกที่เป็นพิษ และโดยทั่วไปประมาณ 3-6 สัปดาห์สำหรับ DRESS
หากคุณมีอาการผื่นขึ้นหรือมีอาการทางผิวหนังอย่างรุนแรง (ดูหัวข้อที่ 4) ให้หยุดใช้ OSSEOR ติดต่อแพทย์ของคุณทันทีและรายงานว่าคุณกำลังใช้ยานี้
หากคุณเคยประสบกับภาวะ Stevens-Johnson syndrome, toxic epidermal necrolysis หรือ DRESS ขณะใช้ OSSEOR คุณไม่ควรเริ่มการรักษาใหม่ด้วย OSSEOR
หากคุณเป็นคนเชื้อสายเอเชีย ให้ปรึกษาแพทย์ก่อนใช้ OSSEOR เนื่องจากคุณอาจมีความเสี่ยงสูงที่จะเกิดปฏิกิริยาทางผิวหนัง
เด็กและวัยรุ่น
OSSEOR ไม่ได้มีไว้สำหรับใช้ในเด็กและวัยรุ่น (อายุต่ำกว่า 18 ปี)
ปฏิกิริยา ยาหรืออาหารชนิดใดที่สามารถเปลี่ยนแปลงผลของ Osseor
ยาอื่นๆ และ OSSEOR
แจ้งให้แพทย์หรือเภสัชกรทราบ หากคุณกำลังรับประทาน เพิ่งกำลังรับประทาน หรืออาจกำลังใช้ยาอื่นอยู่
หยุดใช้ OSSEOR หากคุณต้องใช้ยาเตตราไซคลีนแบบรับประทาน เช่น ด็อกซีไซคลินหรือควิโนโลน เช่น ซิโปรฟลอกซาซิน (ยาปฏิชีวนะสองประเภท) คุณสามารถรีสตาร์ท OSSEOR ได้เมื่อคุณใช้ยาปฏิชีวนะเหล่านี้เสร็จแล้ว หากไม่แน่ใจ ให้ปรึกษาแพทย์หรือเภสัชกร คุณกำลังใช้ยาที่มีแคลเซียม ให้รออย่างน้อย 2 ชั่วโมงก่อนที่จะใช้ OSSEOR หากคุณกำลังใช้ยาลดกรด (ยาเพื่อบรรเทาอาการเสียดท้อง) ให้กินยา OSSEOR อย่างน้อย 2 ชั่วโมง หากไม่สามารถทำได้ สามารถรับประทานยาทั้งสองพร้อมกันได้
หากจำเป็นต้องทดสอบระดับแคลเซียมในเลือดหรือปัสสาวะ คุณต้องแจ้งห้องปฏิบัติการว่าคุณกำลังใช้ OSSEOR เนื่องจากอาจรบกวนวิธีการทดสอบบางอย่าง
OSSEOR พร้อมอาหารและเครื่องดื่ม
อาหาร นม และอนุพันธ์ของมันช่วยลดการดูดซึมของสตรอนเทียม ราเนเลต ขอแนะนำให้ใช้ OSSEOR ในช่วงเวลาระหว่างมื้ออาหาร ก่อนนอน อย่างน้อย 2 ชั่วโมงหลังรับประทานอาหาร นม และอนุพันธ์ของนม หรืออาหารเสริมแคลเซียม
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
การตั้งครรภ์และให้นมบุตร
อย่าใช้ OSSEOR ในระหว่างตั้งครรภ์หรือเมื่อคุณให้นมบุตร ในกรณีที่รับประทานยาโดยไม่ได้ตั้งใจระหว่างตั้งครรภ์หรือให้นมบุตร ให้หยุดรับประทานยาทันทีและแจ้งให้แพทย์ทราบ
การขับรถและการใช้เครื่องจักร
OSSEOR ไม่น่าจะส่งผลกระทบต่อความสามารถในการขับขี่หรือใช้เครื่องจักร
OSSEOR มีสารให้ความหวาน (E951):
หากคุณมีฟีนิลคีโตนูเรีย (ความผิดปกติของการเผาผลาญที่สืบทอดมาได้ยาก) ให้ปรึกษาแพทย์ก่อนเริ่มใช้ยานี้
ปริมาณ วิธีการ และระยะเวลาในการบริหาร วิธีใช้ Osseor: Posology
การรักษาควรเริ่มต้นโดยแพทย์ที่มีประสบการณ์ในการรักษาโรคกระดูกพรุนเท่านั้น
ใช้ยานี้ตามที่แพทย์หรือเภสัชกรบอกเสมอ หากมีข้อสงสัย ควรปรึกษาแพทย์หรือเภสัชกร
OSSEOR ใช้สำหรับช่องปาก ปริมาณที่แนะนำคือหนึ่งซอง 2g ต่อวัน
ขอแนะนำให้ใช้ OSSEOR ก่อนนอน อย่างน้อย 2 ชั่วโมงหลังอาหารเย็น คุณสามารถเข้านอนได้ทันทีหลังจากรับประทาน OSSEOR หากต้องการ
นำเม็ดที่อยู่ในซองใส่หลังจากใส่สารแขวนลอยลงในแก้วที่มีน้ำอย่างน้อย 30 มล. (ประมาณหนึ่งในสามของแก้วมาตรฐาน) (ดูคำแนะนำด้านล่าง) OSSEOR สามารถโต้ตอบกับนมและอนุพันธ์ของนมได้ ดังนั้นจึงเป็น สิ่งสำคัญคือ OSSEOR จะต้องผสมกับน้ำเท่านั้นเพื่อให้แน่ใจว่ายาทำงานได้อย่างถูกต้อง
- เทเม็ดจากซองลงในแก้ว
- เพิ่มน้ำ;
- ผัดจนเม็ดกระจายตัวในน้ำอย่างสมบูรณ์
ดื่มทันที. อย่าปล่อยให้ผ่านไปนานกว่า 24 ชั่วโมงก่อนที่จะดื่มสารแขวนลอย หากไม่สามารถรับประทานยาได้ในทันทีด้วยเหตุผลบางประการ อย่าลืมผสมยาอีกครั้งก่อนดื่ม
แพทย์ของคุณอาจแนะนำให้คุณทานอาหารเสริมแคลเซียมและวิตามินดีนอกเหนือจาก OSSEOR อย่ากินอาหารเสริมแคลเซียมก่อนนอนในเวลาเดียวกันกับ OSSEOR
แพทย์ของคุณจะบอกคุณว่าต้องใช้ OSSEOR ต่อไปนานแค่ไหน การรักษาโรคกระดูกพรุนมักใช้เวลานาน การใช้ยา OSSEOR ต่อไปตราบเท่าที่แพทย์สั่งเป็นสิ่งสำคัญ
ยาเกินขนาด จะทำอย่างไรถ้าคุณได้รับ Osseor มากเกินไป
หากคุณรับ OSSEOR มากกว่าที่ควร
หากคุณใช้ซอง OSSEOR มากกว่าที่แพทย์สั่ง โปรดแจ้งให้แพทย์หรือเภสัชกรทราบ พวกเขาอาจแนะนำให้คุณดื่มนมหรือทานยาลดกรดเพื่อลดการดูดซึมสารออกฤทธิ์
หากคุณลืมทาน OSSEOR
อย่าใช้ยาสองครั้งเพื่อชดเชยปริมาณที่ลืม เพียงทานยาครั้งต่อไปตามเวลาที่กำหนด
หากคุณหยุดใช้ OSSEOR
สิ่งสำคัญคือต้องใช้ OSSEOR ต่อไปตราบเท่าที่แพทย์ของคุณกำหนดไว้ OSSEOR สามารถรักษาโรคกระดูกพรุนที่รุนแรงได้หากได้รับอย่างต่อเนื่องเท่านั้น หากคุณมีคำถามเพิ่มเติมเกี่ยวกับการใช้ยานี้ โปรดสอบถามแพทย์หรือเภสัชกรของคุณ
ผลข้างเคียง ผลข้างเคียงของ Osseor คืออะไร?
เช่นเดียวกับยาทั้งหมด ยานี้สามารถทำให้เกิดผลข้างเคียงได้ แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
หยุดใช้ OSSEOR และแจ้งให้แพทย์ทราบทันทีหากมีผลข้างเคียงดังต่อไปนี้:
ร่วมกัน (อาจส่งผลกระทบมากถึง 1 ใน 10 ผู้ป่วย):
- หัวใจวาย : เจ็บหน้าอกอย่างกะทันหันซึ่งอาจขยายไปถึงแขนซ้าย กราม ท้อง หลังและ/หรือไหล่ อาการอื่น ๆ อาจเป็น: คลื่นไส้ / อาเจียน, เหงื่อออก, หายใจถี่, ใจสั่น, (มาก) อ่อนเพลียและ / หรือเวียนศีรษะ ในผู้ป่วยที่มีความเสี่ยงสูงต่อโรคหัวใจ หัวใจวายอาจเกิดขึ้นได้กับความถี่ทั่วไป หากคุณเป็นผู้ป่วยที่มีความเสี่ยงสูง แพทย์ของคุณจะไม่สั่ง OSSEOR
- ลิ่มเลือดในเส้นเลือด (ลิ่มเลือดอุดตัน): ปวด, แดง, บวมที่ขา, เจ็บหน้าอกกะทันหันหรือหายใจลำบาก
หายาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 ผู้ป่วย):
- สัญญาณของปฏิกิริยาภูมิไวเกินอย่างรุนแรง (DRESS): เริ่มแรกเป็นอาการคล้ายไข้หวัดใหญ่และมีผื่นขึ้นบนใบหน้า จากนั้นผื่นขึ้นเป็นวงกว้างที่มีอุณหภูมิสูง (ผิดปกติ) เพิ่มระดับเอนไซม์ตับที่พบในการตรวจเลือด (ผิดปกติ) เพิ่มสีขาวบางประเภท เซลล์เม็ดเลือด (eosinophilia) (หายาก) และต่อมน้ำเหลืองโต (ผิดปกติ)
หายากมาก (อาจส่งผลกระทบมากถึง 1 ใน 10,000 ผู้ป่วย):
- สัญญาณของผื่นที่ผิวหนังที่อาจเป็นอันตรายถึงชีวิต (กลุ่มอาการสตีเวนส์-จอห์นสัน, การตายของเนื้อร้ายที่ผิวหนังที่เป็นพิษ): เริ่มแรกเป็นปื้นคล้ายเป้าหมายสีแดงหรือเป็นหย่อมๆ กลมๆ มักจะมีตุ่มพองตรงกลางลำตัว อาการเพิ่มเติมอาจรวมถึงการเป็นแผลที่ปาก คอ จมูก อวัยวะเพศ และเยื่อบุตาอักเสบ (ตาบวมและแดง) ผื่นผิวหนังที่อาจเป็นอันตรายถึงชีวิตเหล่านี้มักมาพร้อมกับอาการคล้ายไข้หวัดใหญ่ ผื่นอาจลุกลามจนพุพองทั่วร่างกายหรือลอกของผิวหนัง
ผลข้างเคียงที่เป็นไปได้อื่น ๆ
พบบ่อยมาก (อาจส่งผลกระทบมากกว่า 1 ใน 10 คน): อาการคัน ลมพิษ ผื่นผิวหนัง อาการบวมน้ำที่ผิวหนัง (angioedema) (เช่น อาการบวมที่ใบหน้า ลิ้นหรือลำคอ หายใจลำบากหรือกลืนลำบาก) ปวดกระดูก แขนขา กล้ามเนื้อ และ/หรือ ในข้อต่อกล้ามเนื้อเป็นตะคริว
ทั่วไป: อาเจียน ปวดท้อง กรดไหลย้อน อาหารไม่ย่อย ท้องผูก ท้องอืด นอนหลับยาก การอักเสบของตับ (ตับอักเสบ) แขนขาบวม หลอดลมทำงานมากเกินไป (อาการต่างๆ ได้แก่ หายใจมีเสียงวี๊ด หายใจถี่และไอ) เพิ่มระดับของกล้ามเนื้อ เอนไซม์ (creatine phosphokinase) คลื่นไส้, ท้องร่วง, ปวดหัว, กลาก, ความจำเสื่อม, เป็นลม, รู้สึกเสียวซ่า, เวียนศีรษะ, เวียนศีรษะ อย่างไรก็ตาม ผลกระทบเหล่านี้ไม่รุนแรงและเกิดขึ้นชั่วคราว และโดยปกติไม่จำเป็นต้องหยุดการรักษา แจ้งให้แพทย์ทราบ หากผลข้างเคียงเหล่านี้เป็นปัญหาหรือเกิดขึ้นอย่างต่อเนื่อง
ผิดปกติ (อาจส่งผลกระทบมากถึง 1 ใน 100 คน): การชัก การระคายเคืองของเยื่อบุในช่องปาก (เช่น แผลในปากและการอักเสบของเหงือก) ผมร่วง สับสน รู้สึกไม่สบาย ปากแห้ง ระคายเคืองผิวหนัง
หายาก: ลดการผลิตเซลล์เม็ดเลือดในไขกระดูก หากคุณหยุดการรักษาเนื่องจากปฏิกิริยาภูมิไวเกิน คุณไม่ควรรีสตาร์ท OSSEOR
การรายงานผลข้างเคียง
หากคุณได้รับผลข้างเคียง ให้ปรึกษาแพทย์หรือเภสัชกร ซึ่งรวมถึงผลข้างเคียงที่อาจเกิดขึ้นซึ่งไม่ได้ระบุไว้ในเอกสารฉบับนี้ คุณยังสามารถรายงานผลข้างเคียงได้โดยตรงผ่านระบบการรายงานระดับประเทศที่ระบุไว้ในภาคผนวก 5 โดยการรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
เก็บยานี้ให้พ้นสายตาและมือเด็ก
ห้ามใช้ยานี้หลังจากวันหมดอายุซึ่งระบุไว้บนกล่องและซองหลังคำว่า EXP วันหมดอายุหมายถึงวันสุดท้ายของเดือนนั้น เมื่อสร้างใหม่ในน้ำ สารแขวนลอยจะคงตัวเป็นเวลา 24 ชั่วโมง
อย่างไรก็ตาม ขอแนะนำให้ดื่มสารแขวนลอยทันทีหลังจากเตรียมอาหาร (ดูหัวข้อที่ 3) ยานี้ไม่ต้องการเงื่อนไขการเก็บรักษาพิเศษใด ๆ
อย่าทิ้งยาผ่านทางน้ำเสียหรือของเสียในครัวเรือนถามเภสัชกรของคุณถึงวิธีทิ้งยาที่คุณไม่ได้ใช้อีกต่อไป ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
องค์ประกอบและรูปแบบยา
OSSEOR ประกอบด้วยอะไรบ้าง
- สารออกฤทธิ์คือสตรอนเทียมราเนเลต แต่ละซองมีสตรอนเทียมราเนเลต 2 กรัม
- ส่วนผสมอื่นๆ ได้แก่ แอสพาเทม (E 951) มอลโทเดกซ์ทริน แมนนิทอล (E 421)
คำอธิบายของ OSSEOR ที่ดูเหมือนและเนื้อหาของแพ็ค
OSSEOR มีอยู่ในซองที่มีเม็ดสีเหลืองสำหรับแขวนลอยในช่องปาก OSSEOR บรรจุในซองขนาด 7, 14, 28, 56, 84 หรือ 100 ซอง ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่แสดงอาจไม่ทันสมัย
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
OSSEOR 2G แกรนูลสำหรับการระงับช่องปาก
▼ ผลิตภัณฑ์ยาอาจมีการตรวจสอบเพิ่มเติม ซึ่งจะช่วยให้ระบุข้อมูลความปลอดภัยใหม่ได้อย่างรวดเร็ว ผู้เชี่ยวชาญด้านการดูแลสุขภาพจะต้องรายงานอาการไม่พึงประสงค์ที่น่าสงสัย ดูหัวข้อ 4.8 สำหรับข้อมูลเกี่ยวกับวิธีการรายงานอาการไม่พึงประสงค์
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
แต่ละซองมีสตรอนเทียมราเนเลต 2 กรัม
สารเพิ่มปริมาณที่ทราบผล:
แต่ละซองยังมีแอสพาเทม 20 มก. (E 951)
สำหรับรายการสารปรุงแต่งทั้งหมด ดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
เม็ดสำหรับระงับช่องปาก
เม็ดสีเหลือง
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
การรักษาโรคกระดูกพรุนขั้นรุนแรง:
• ในสตรีวัยหมดประจำเดือน
• ในผู้ชายที่เป็นผู้ใหญ่
มีความเสี่ยงสูงที่จะเกิดกระดูกหัก ซึ่งการรักษาด้วยยาอื่น ๆ ที่ได้รับอนุมัติสำหรับการรักษาโรคกระดูกพรุนนั้นไม่สามารถทำได้ เช่น ข้อห้ามหรือการแพ้ยา
ในสตรีวัยหมดประจำเดือน สตรอนเทียม ราเนเลตช่วยลดความเสี่ยงของกระดูกสันหลังและกระดูกสะโพกหัก (ดูหัวข้อ 5.1)
การตัดสินใจกำหนดสตรอนเทียมราเนเลตควรขึ้นอยู่กับการประเมินความเสี่ยงโดยรวมของผู้ป่วยแต่ละราย (ดูหัวข้อ 4.3 และ 4.4)
04.2 วิทยาและวิธีการบริหาร
การรักษาควรเริ่มต้นโดยแพทย์ที่มีประสบการณ์ในการรักษาโรคกระดูกพรุนเท่านั้น
ปริมาณ
ปริมาณที่แนะนำคือซองละ 2 กรัมวันละครั้งสำหรับการบริหารช่องปาก
เนื่องจากธรรมชาติของสภาพที่กำลังรับการรักษา สตรอนเทียมราเนเลตจึงเหมาะสำหรับการใช้งานในระยะยาว
การดูดซึมของสตรอนเทียมราเนเลตจะลดลงจากอาหาร นม และอนุพันธ์ของมัน ดังนั้น ควรให้ OSSEOR ระหว่างมื้ออาหาร เนื่องจากการดูดซึมช้า ควรให้ OSSEOR ก่อนนอน อย่างน้อยสองชั่วโมงหลังอาหาร (ดูหัวข้อ 4.5 และ 5.2)
ผู้ป่วยที่ได้รับการรักษาด้วยสตรอนเซียมราเนเลตควรรับประทานวิตามินดีและอาหารเสริมแคลเซียมหากรับประทานอาหารไม่เพียงพอ
ผู้ป่วยสูงอายุ
ประสิทธิภาพและความปลอดภัยของสตรอนเทียมราเนเลตได้รับการแสดงให้เห็นในกลุ่มตัวอย่างขนาดใหญ่ของผู้ชายที่เป็นผู้ใหญ่และสตรีวัยหมดประจำเดือนทุกวัย (สูงสุด 100 ปีที่รวม) ที่เป็นโรคกระดูกพรุน ไม่จำเป็นต้องปรับขนาดยาตามอายุ
ผู้ป่วยไตวาย
ไม่แนะนำ Strontium ranelate ในผู้ป่วยที่มีภาวะไตวายอย่างรุนแรง (creatinine clearance น้อยกว่า 30 มล. / นาที) (ดูหัวข้อ 4.4 และ 5.2) ไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยที่มีภาวะไตวายเล็กน้อยถึงปานกลาง (clearance of creatinine 30 - 70 ml / นาที) (ดูหัวข้อ 4.4 และ 5.2)
ผู้ป่วยที่มีภาวะตับไม่เพียงพอ
ไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยที่มีภาวะตับไม่เพียงพอ (ดูหัวข้อ 5.2)
ประชากรเด็ก
ความปลอดภัยและประสิทธิภาพของ OSSEOR ในเด็กอายุต่ำกว่า 18 ปียังไม่ได้รับการจัดตั้งขึ้น ไม่มีข้อมูล
วิธีการบริหาร
สำหรับใช้ในช่องปาก
เม็ดของซองควรใช้หลังจากระงับในแก้วที่มีน้ำอย่างน้อย 30 มล. (ประมาณหนึ่งในสามของแก้วปกติ)
แม้ว่าการศึกษาการใช้งานได้แสดงให้เห็นว่าสตรอนเซียมราเนเลตยังคงคงตัวในการระงับเป็นเวลา 24 ชั่วโมงหลังการเตรียมการ ควรระงับการระงับทันทีหลังจากเตรียม
04.3 ข้อห้าม
• ภูมิไวเกินต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อ 6.1
• การอุดตันของเส้นเลือดดำในปัจจุบันหรือก่อนหน้า (VTE) รวมถึงการอุดตันของหลอดเลือดดำส่วนลึกและเส้นเลือดอุดตันที่ปอด
• การตรึงชั่วคราวหรือถาวร เช่น การผ่าตัดหรือการนอนบนเตียงเป็นเวลานาน
• ประวัติโรคหัวใจขาดเลือด โรคหลอดเลือดแดงส่วนปลาย และ / หรือโรคหลอดเลือดสมองในอดีตหรือปัจจุบัน
• ความดันโลหิตสูงที่ไม่สามารถควบคุมได้
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
เหตุการณ์หัวใจขาดเลือด
ในการวิเคราะห์แบบรวมกลุ่มของการทดลองทางคลินิกแบบสุ่มที่มีกลุ่มควบคุมด้วยยาหลอกในผู้ป่วยโรคกระดูกพรุนในวัยหมดประจำเดือนพบว่าผู้ป่วยที่ได้รับ OSSEOR มีอาการกล้ามเนื้อหัวใจตายเพิ่มขึ้นอย่างมีนัยสำคัญเมื่อเทียบกับผู้ที่ได้รับยาหลอก (ดูหัวข้อ 4.8)
ผู้ป่วยควรได้รับการประเมินความเสี่ยงโรคหัวใจและหลอดเลือดก่อนเริ่มการรักษา
ผู้ป่วยที่มีปัจจัยเสี่ยงที่สำคัญต่อการเกิดโรคหัวใจและหลอดเลือด (เช่น ความดันโลหิตสูง ไขมันในเลือดสูง เบาหวาน การสูบบุหรี่) ควรได้รับการรักษาด้วยสตรอนเทียม ราเนเลตหลังจากการพิจารณาอย่างรอบคอบแล้วเท่านั้น (ดูหัวข้อ 4.3 และ 4.8)
ในระหว่างการรักษาด้วย OSSEOR ความเสี่ยงต่อโรคหัวใจและหลอดเลือดเหล่านี้ควรได้รับการตรวจสอบเป็นระยะ ๆ โดยปกติทุก 6-12 เดือน
ควรหยุดการรักษาหากผู้ป่วยเป็นโรคหัวใจขาดเลือด โรคหลอดเลือดแดงส่วนปลาย โรคหลอดเลือดสมอง หรือถ้าความดันโลหิตสูงไม่ได้รับการควบคุม (ดูหัวข้อ 4.3)
ลิ่มเลือดอุดตันหลอดเลือดดำ
ในการศึกษาที่ควบคุมด้วยยาหลอกระยะที่ 3 การรักษาด้วยสตรอนเทียม ราเนเลตสัมพันธ์กับอุบัติการณ์การเกิดลิ่มเลือดอุดตันในหลอดเลือดดำ (VTE) ประจำปีที่เพิ่มขึ้น รวมถึงภาวะหลอดเลือดอุดตันในปอด (ดูหัวข้อ 4.8) ไม่ทราบสาเหตุของการเพิ่มขึ้นนี้ OSSEOR มีข้อห้ามในผู้ป่วยที่มีภาวะลิ่มเลือดอุดตันในหลอดเลือดดำก่อนหน้านี้ (ดูหัวข้อ 4.3) และควรใช้ด้วยความระมัดระวังในผู้ป่วยที่มีความเสี่ยงต่อการเกิด VTE
ในระหว่างการรักษาผู้ป่วยอายุมากกว่า 80 ปีที่มีความเสี่ยงต่อ VTE ความจำเป็นในการรักษาด้วย OSSEOR อย่างต่อเนื่องควรได้รับการประเมินใหม่ ควรยุติการรักษาด้วย OSSEOR โดยเร็วที่สุดในกรณีที่เจ็บป่วยหรือมีอาการที่นำไปสู่การตรึง (ดูหัวข้อ 4.3) และควรใช้มาตรการป้องกันที่เหมาะสม ไม่ควรให้การบำบัดต่อจนกว่าสภาวะที่นำไปสู่การตรึงจะไม่ได้รับการแก้ไข และผู้ป่วยสามารถเคลื่อนที่ได้อย่างสมบูรณ์ เมื่อเกิด VTE ควรยุติ OSSEOR
ใช้ในผู้ป่วยไตวาย
ในกรณีที่ไม่มีข้อมูลความปลอดภัยของกระดูกในผู้ป่วยที่มีภาวะไตวายอย่างรุนแรงที่ได้รับสตรอนเทียม ราเนเลต OSSEOR ไม่แนะนำในผู้ป่วยที่มีระดับครีเอตินินน้อยกว่า 30 มล. / นาที (ดูหัวข้อ 5.2) ตามแนวทางปฏิบัติทางคลินิกที่ดี แนะนำให้ติดตามการทำงานของไตเป็นระยะในผู้ป่วยที่มีภาวะไตวายเรื้อรัง ควรประเมินความต่อเนื่องของการรักษาด้วย OSSEOR ในผู้ป่วยที่เป็นโรคไตวายอย่างรุนแรงเป็นรายบุคคล
ปฏิกิริยาทางผิวหนัง
มีรายงานการเกิดปฏิกิริยาทางผิวหนังที่คุกคามชีวิต (Stevens-Johnson Syndrome (SJS), toxic epidermal necrolysis (NET) และผื่นจากยาที่มีอาการ eosinophilia และอาการทางระบบ (DRESS)) ระหว่างการใช้ OSSEOR
ผู้ป่วยควรได้รับแจ้งถึงอาการและอาการแสดง และตรวจสอบปฏิกิริยาทางผิวหนังอย่างใกล้ชิด ความเสี่ยงสูงสุดของการเกิด SJS หรือ NET คือภายในสองสามสัปดาห์แรกของการรักษา และภายใน 3-6 สัปดาห์สำหรับ DRESS
หากอาการและอาการแสดงของ SJS หรือ NET (เช่น ผื่นผิวหนังลุกลามบ่อยครั้งโดยมีแผลพุพองและเยื่อเมือก) หรือ DRESS (เช่น ผื่น ไข้ ภาวะอีโอซิโนฟีเลีย และการมีส่วนร่วมอย่างเป็นระบบ (เช่น โรคเนื้องอกในไต โรคตับอักเสบ โรคไต และโรคปอด) เกิดขึ้นคั่นระหว่างหน้า) ให้รักษาด้วย OSSEOR ควรหยุดทันที
ผลลัพธ์ที่ดีที่สุดในการจัดการ SJS, NET หรือ DRESS จะได้รับหลังจากการวินิจฉัยตั้งแต่เนิ่นๆ และการหยุดยาที่ต้องสงสัยทันที การหยุดการรักษาแต่เนิ่นๆ เกี่ยวข้องกับการพยากรณ์โรคที่ดีขึ้น ภาพทางคลินิกของ DRESS ได้รับการแก้ไขในกรณีส่วนใหญ่โดยหยุดการรักษาด้วย OSSEOR และการเริ่มต้นของการรักษาด้วย corticosteroid เมื่อจำเป็น การฟื้นตัวอาจช้าและในบางกรณีมีรายงานการกำเริบของโรคหลังจากหยุดการรักษาด้วยคอร์ติโคสเตียรอยด์
ในผู้ป่วยที่พัฒนา SJS, NET หรือ DRESS โดยใช้ OSSEOR การบำบัดด้วย OSSEOR จะต้องไม่เริ่มต้นใหม่อีกต่อไป
มีรายงานอุบัติการณ์ของปฏิกิริยาภูมิไวเกินรวมถึงผื่นที่ผิวหนัง SJS หรือ NET ที่สูงขึ้นแม้ว่าจะยังไม่ค่อยเกิดขึ้นในผู้ป่วยที่เชื้อสายเอเชีย
ปฏิสัมพันธ์กับการทดสอบในห้องปฏิบัติการ
สตรอนเทียมรบกวนวิธีการวัดสีเพื่อกำหนดความเข้มข้นของแคลเซียมในเลือดและปัสสาวะ ดังนั้นในการปฏิบัติทางคลินิก ต้องใช้วิธีการฉายรังสีอะตอมมิกในพลาสมาแบบเหนี่ยวนำคู่ควบคู่หรือวิธีการดูดกลืนแสงอะตอมมิกเพื่อให้แน่ใจว่ามีการประเมินความเข้มข้นของแคลเซียมในเลือดและปัสสาวะอย่างถูกต้อง
สารเพิ่มปริมาณ
OSSEOR มีแอสพาเทมซึ่งเป็นแหล่งของฟีนิลอะลานีนซึ่งอาจเป็นอันตรายต่อผู้ป่วยฟีนิลคีโตนูเรีย
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
อาหาร นมและอนุพันธ์ และผลิตภัณฑ์ยาที่มีแคลเซียมสามารถลดการดูดซึมของสตรอนเทียม เรเนเลตได้ประมาณ 60 - 70% ดังนั้น การบริหาร OSSEOR และผลิตภัณฑ์เหล่านี้ควรแยกกันอย่างน้อยสองชั่วโมง (ดูหัวข้อ 4.2 และ 5.2)
เนื่องจากไพเพอร์ไดวาเลนต์สามารถสร้างสารเชิงซ้อนที่ดูดซึมได้ไม่ดีด้วยยาเตตราไซคลีนในช่องปาก (เช่น ด็อกซีไซคลิน) และยาปฏิชีวนะควิโนโลน (เช่น ซิโปรฟลอกซาซิน) ที่ระดับทางเดินอาหาร จึงไม่แนะนำให้ใช้สตรอนเทียม ราเนเลตร่วมกับผลิตภัณฑ์ยาเหล่านี้ เพื่อเป็นการป้องกันไว้ก่อน OSSEOR ควรหยุดในระหว่างการรักษาด้วย tetracyclines ในช่องปากหรือยาปฏิชีวนะ quinolone
การศึกษาทางคลินิก ในร่างกาย ปฏิกิริยาระหว่างยาได้แสดงให้เห็นว่าการบริโภคอะลูมิเนียมและแมกนีเซียมไฮดรอกไซด์ในสองชั่วโมงก่อนหรือในเวลาเดียวกันกับสตรอนเทียม เรเนเลต ทำให้การดูดซึมสตรอนเทียม เรเนเลตลดลงเล็กน้อย (AUC ลดลง 20-25%) ในขณะที่ การดูดซึมยังคงไม่เปลี่ยนแปลงในทางปฏิบัติเมื่อให้ยาลดกรดเป็นเวลา 2 ชั่วโมงหลังจากรับประทานสตรอนเทียม ราเนเลต ดังนั้นจึงควรรับประทานยาลดกรดอย่างน้อยสองชั่วโมงหลังจากรับประทาน OSSEOR อย่างไรก็ตาม เนื่องจากแนะนำให้ใช้ OSSEOR ก่อนนอนเมื่อตารางการจ่ายยานี้ไม่มีผลบังคับใช้ ใช้ร่วมกันยังคงเป็นที่ยอมรับ
ไม่พบปฏิสัมพันธ์กับการเสริมวิตามินดีในช่องปาก
ในการทดลองทางคลินิก ไม่มีการแสดงปฏิกิริยาทางคลินิกหรือการเพิ่มระดับสตรอนเทียมในเลือดอย่างมีนัยสำคัญกับผลิตภัณฑ์ยา ซึ่งในทางปฏิบัติในปัจจุบัน มีการสั่งจ่ายยาร่วมกับ OSSEOR ทั่วไป รวมถึง: ยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (รวมถึงกรดอะซิติลซาลิไซลิก) , anilides (เช่น พาราเซตามอล), ตัวบล็อก H2 และตัวยับยั้งโปรตอนปั๊ม, ยาขับปัสสาวะ, ดิจอกซินและไกลโคไซด์หัวใจ, ไนเตรตอินทรีย์และยาขยายหลอดเลือดอื่น ๆ สำหรับโรคหัวใจ, ตัวบล็อกแคลเซียมแชนเนล, ตัวบล็อกเบต้า, สารยับยั้ง ACE, คู่อริ angiotensin II, beta-2- คัดเลือก ตัวเร่งปฏิกิริยาตัวรับ adrenergic, สารต้านการแข็งตัวของเลือดในช่องปาก, สารยับยั้งการรวมตัวของเกล็ดเลือด, สแตติน, ไฟเบรตและอนุพันธ์เบนโซไดอะซีพีน
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์
ไม่มีข้อมูลจากการใช้สตรอนเทียมราเนเลตในสตรีมีครรภ์ การศึกษาในสัตว์ทดลองได้แสดงให้เห็นในปริมาณที่สูง ผลกระทบของกระดูกแบบย้อนกลับในลูกหลานของหนูและกระต่ายที่รับการรักษาระหว่างตั้งครรภ์ (ดูหัวข้อ 5.3) หากใช้ OSSEOR โดยไม่ได้ตั้งใจในระหว่างตั้งครรภ์ ควรหยุดการรักษา
เวลาให้อาหาร
ข้อมูลทางเคมีกายภาพแนะนำการขับสตรอนเทียมราเนเลตในน้ำนมแม่ ไม่ควรใช้ OSSEOR ในระหว่างการให้นม
ภาวะเจริญพันธุ์
ไม่มีผลต่อภาวะเจริญพันธุ์ของเพศชายและเพศหญิงในการศึกษาในสัตว์ทดลอง
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
Strontium ranelate ไม่มีหรือมีอิทธิพลเล็กน้อยต่อความสามารถในการขับหรือใช้เครื่องจักร
04.8 ผลกระทบที่ไม่พึงประสงค์
สรุปข้อมูลความปลอดภัย
OSSEOR ได้รับการศึกษาในการทดลองทางคลินิกที่เกี่ยวข้องกับคนประมาณ 8,000 คน ความปลอดภัยในระยะยาวได้รับการประเมินในการศึกษาระยะที่ 3 ในสตรีวัยหมดประจำเดือนที่เป็นโรคกระดูกพรุนที่รักษานานถึง 60 เดือนด้วยสตรอนเทียมราเนเลต 2 กรัมต่อวัน (n = 3,352) หรือยาหลอก (n = 3,317) อายุเฉลี่ย ณ เวลาที่รวมคือ 75 ปีและ 23% ของผู้ป่วยที่ลงทะเบียนเรียนอยู่ระหว่าง 80 ถึง 100 ปี
ในการวิเคราะห์แบบรวมกลุ่มของการทดลองกลุ่มควบคุมด้วยยาหลอกแบบสุ่มในผู้ป่วยโรคกระดูกพรุนในวัยหมดประจำเดือน อาการไม่พึงประสงค์ที่พบบ่อยที่สุดคืออาการคลื่นไส้และท้องร่วง โดยทั่วไปรายงานเมื่อเริ่มการรักษา โดยไม่มีความแตกต่างที่เห็นได้ชัดเจนระหว่างกลุ่มในระยะหลัง การยุติการรักษามีสาเหตุหลักมาจากอาการคลื่นไส้
ไม่มีความแตกต่างในลักษณะของอาการไม่พึงประสงค์ระหว่างกลุ่มที่ได้รับการรักษา ไม่ว่าผู้ป่วยจะอายุน้อยกว่าหรืออายุมากกว่า 80 ปีในขณะที่เข้ารับการรักษา
ตารางอาการไม่พึงประสงค์
มีรายงานอาการไม่พึงประสงค์ดังต่อไปนี้ในระหว่างการทดลองทางคลินิกและ / หรือระหว่างการใช้สตรอนเทียม ranelate หลังการขาย อาการไม่พึงประสงค์แสดงอยู่ด้านล่างโดยใช้แบบแผนต่อไปนี้: พบบ่อยมาก (≥1 / 10); ทั่วไป (≥1 / 100,
§ ความถี่ในการทดลองทางคลินิกมีความคล้ายคลึงกันในกลุ่มยาและกลุ่มยาหลอก
* รายงานว่าหายากในประเทศแถบเอเชีย
# สำหรับอาการไม่พึงประสงค์ที่ไม่ได้สังเกตพบในการทดลองทางคลินิก ขีดจำกัดสูงสุดของช่วงความเชื่อมั่น 95% จะต้องไม่เกิน 3 / X โดยที่ X แสดงถึงขนาดตัวอย่างทั้งหมดจากการทดลองทางคลินิกทั้งหมดและการศึกษาที่เกี่ยวข้อง
เศษส่วนกระดูกและกล้ามเนื้อ > 3 เท่าของขีดจำกัดบนของช่วงปกติ ในกรณีส่วนใหญ่ ค่าเหล่านี้จะถูกทำให้เป็นมาตรฐานโดยธรรมชาติโดยไม่มีการเปลี่ยนแปลงในการรักษา
คำอธิบายของอาการไม่พึงประสงค์ที่เลือก
ลิ่มเลือดอุดตันหลอดเลือดดำ
ในการศึกษาระยะที่ 3 อุบัติการณ์ประจำปีของการเกิดลิ่มเลือดอุดตันในหลอดเลือดดำ (VTE) ที่สังเกตพบในช่วง 5 ปีอยู่ที่ประมาณ 0.7% โดยมีความเสี่ยงสัมพัทธ์เท่ากับ 1.4 (95% CI = [1.0; 2, 0]) ในผู้ป่วยที่ได้รับยาสตรอนเทียมราเนเลตเทียบกับยาหลอก (ดูหัวข้อ 4.4)
กล้ามเนื้อหัวใจตาย
ในการวิเคราะห์แบบรวมกลุ่มของการทดลองทางคลินิกแบบสุ่มที่มีกลุ่มควบคุมด้วยยาหลอกในผู้ป่วยโรคกระดูกพรุนในวัยหมดประจำเดือนพบว่ามีกล้ามเนื้อหัวใจตายเพิ่มขึ้นอย่างมีนัยสำคัญในผู้ป่วยที่ได้รับยาสตรอนเทียมราเนเลตเมื่อเทียบกับผู้ป่วยที่ได้รับยาหลอก (1.7% เทียบกับที่ 1.1%) โดยมีความเสี่ยงสัมพัทธ์ 1.6 (95% CI = [1.07; 2.38])
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านระบบการรายงานระดับประเทศ
04.9 ใช้ยาเกินขนาด
อาการ
ในการศึกษาทางคลินิกเพื่อประเมินการบริหารซ้ำของสตรอนเทียม ราเนเลต 4 กรัมต่อวันเป็นเวลานานกว่า 25 วันในสตรีวัยหมดประจำเดือนที่มีสุขภาพดี พบว่าสามารถทนต่อยาได้ดี การให้ยาครั้งเดียวในปริมาณมากถึง 11 กรัมในอาสาสมัครชายที่มีสุขภาพดีอายุน้อยไม่ก่อให้เกิดอาการเฉพาะใดๆ
การจัดการ
จากการสังเกตการให้ยาเกินขนาดในการทดลองทางคลินิก (มากถึง 4 กรัม / วันเป็นระยะเวลาสูงสุด 147 วัน) ไม่พบผลกระทบที่เกี่ยวข้องทางคลินิก
การให้นมหรือยาลดกรดอาจมีประโยชน์ในการลดการดูดซึมของสารออกฤทธิ์ ในกรณีที่ให้ยาเกินขนาดมาก อาจพิจารณาถึงความเป็นไปได้ที่จะกระตุ้นให้อาเจียนเพื่อกำจัดสารออกฤทธิ์ที่ไม่ดูดซึม
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มเภสัชบำบัด: ยารักษาโรคกระดูก - ยาอื่นๆ ที่มีผลต่อโครงสร้างกระดูกและการทำให้เป็นแร่, รหัส ATC: M05BX03
กลไกการออกฤทธิ์
ในหลอดทดลอง, สตรอนเทียม ranelate:
- เพิ่มการสร้างกระดูกในการเพาะเลี้ยงเนื้อเยื่อกระดูก เช่นเดียวกับการจำลองแบบของสารตั้งต้นของ osteoblast และการสังเคราะห์คอลลาเจนในการเพาะเลี้ยงเซลล์กระดูก
- ลดการสลายของกระดูกโดยลดการสร้างความแตกต่างของ osteoclast และกิจกรรมการสลายของกระดูก
สิ่งนี้เป็นตัวกำหนดความสมดุลของการหมุนเวียนของกระดูกเพื่อสนับสนุนการก่อตัวของกระดูก
กิจกรรมของสตรอนเทียมราเนเลตได้รับการแสดงให้เห็นในการศึกษาทดลองหลายครั้ง โดยเฉพาะอย่างยิ่ง ในหนูที่ไม่บุบสลาย สตรอนเทียม ราเนเลตจะเพิ่มมวลกระดูก trabecular จำนวนและความหนาของ trabeculae ส่งผลให้ความแข็งแรงของกระดูกดีขึ้น
สตรอนเทียมส่วนใหญ่จะถูกดูดซึมบนพื้นผิวผลึก และมีเพียงบางส่วนเท่านั้นที่จะทดแทนแคลเซียมในผลึกอะพาไทต์ในกระดูกที่เพิ่งสร้างใหม่ทั้งในสัตว์และมนุษย์ภายใต้การบำบัด Strontium ranelate ไม่เปลี่ยนลักษณะของผลึกกระดูก ในการตรวจชิ้นเนื้อกระดูกอุ้งเชิงกรานที่ได้รับหลังการรักษาด้วยสตรอนเทียมราเนเลต 2 กรัม / วันนานถึง 60 เดือนในการศึกษาระยะที่ 3 พบว่าไม่มีผลเสียต่อคุณภาพของกระดูกหรือการทำให้เป็นแร่
ผลรวมของการกระจายสตรอนเทียมในกระดูก (ดูหัวข้อ 5.2) และการดูดซึมเอ็กซ์เรย์ของสตรอนเทียมที่สูงขึ้นเมื่อเทียบกับแคลเซียม ส่งผลให้ค่าความหนาแน่นของกระดูกเพิ่มขึ้น (BMD) ซึ่งวัดโดยวิธีดูดซับโฟตอนแบบลำแสงคู่ ( ดีเอ็กซ์เอ) . ข้อมูลที่มีอยู่ระบุว่าปัจจัยเหล่านี้คิดเป็นสัดส่วนประมาณ 50% ของการเปลี่ยนแปลง BMD ที่สังเกตได้ในช่วง 3 ปีของการรักษาด้วย OSSEOR 2 กรัมต่อวัน สิ่งนี้ควรนำมาพิจารณาเมื่อประเมินการเปลี่ยนแปลงใน BMD ระหว่างการรักษาด้วย OSSEOR ในการศึกษาระยะที่ 3 ซึ่งแสดงให้เห็นถึงประสิทธิภาพของการรักษา OSSEOR ในการลดการแตกหัก OSSEOR ได้เพิ่มค่าเฉลี่ย BMD จากการรวมประมาณ 4% ต่อปีที่กระดูกสันหลังส่วนเอวและ 2% ต่อปีที่ระดับกระดูกสันหลังส่วนเอว ของคอกระดูกต้นขาซึ่งถึง ขึ้นอยู่กับการศึกษาตามลำดับตั้งแต่ 13 ถึง 15% และจาก 5 ถึง 6% หลังจาก 3 ปี
ในการศึกษาระยะที่ 3 เมื่อเทียบกับยาหลอก ตัวบ่งชี้ทางชีวเคมีของการสร้างกระดูก (อัลคาไลน์ฟอสฟาเตสเฉพาะและโปรเปปไทด์ C-terminal ของโปรคอลลาเจนชนิดที่ 1) เพิ่มขึ้นและการสลายของกระดูก (ซีรัม C-telopeptide และการเชื่อมโยงข้ามทางเดินปัสสาวะของ N-telopeptide) ลดลงจากเดือนที่สามเป็นปีที่สามของการรักษา
นอกจากผลทางเภสัชวิทยาเบื้องต้นของสตรอนเทียม ราเนเลตแล้ว ระดับแคลเซียมและพาราไทรอยด์ฮอร์โมน (PTH) ในซีรัมลดลงเล็กน้อย ความเข้มข้นของฟอสฟอรัสในเลือดและกิจกรรมอัลคาไลน์ฟอสฟาเตสโดยรวมยังถูกสังเกต โดยไม่มีผลกระทบทางคลินิก
ประสิทธิภาพทางคลินิก
โรคกระดูกพรุนถูกกำหนดให้เป็น BMD ของกระดูกสันหลังหรือสะโพกที่มีค่าเบี่ยงเบนมาตรฐาน 2.5 หรือมากกว่าต่ำกว่าค่าเฉลี่ยในประชากรปกติอายุน้อย ปัจจัยเสี่ยงบางประการเกี่ยวข้องกับโรคกระดูกพรุนในวัยหมดประจำเดือน ได้แก่ มวลกระดูกต่ำ ความหนาแน่นของแร่ธาตุของกระดูกต่ำ วัยหมดประจำเดือนก่อนกำหนด การสูบบุหรี่ และประวัติครอบครัวเป็นโรคกระดูกพรุน ผลทางคลินิกของโรคกระดูกพรุนคือ กระดูกหัก ความเสี่ยงของการเกิดกระดูกหักจะเพิ่มขึ้นตามจำนวนปัจจัยเสี่ยงที่เพิ่มขึ้น
การรักษาโรคกระดูกพรุนในวัยหมดประจำเดือน
โปรแกรมการศึกษาเพื่อประเมินการลดการแตกหักด้วย OSSEOR ประกอบด้วยการศึกษาที่ควบคุมด้วยยาหลอกระยะที่ 3 สองการศึกษา: การศึกษา SOTI และการศึกษา TROPOS การศึกษา SOTI เกี่ยวข้องกับสตรีวัยหมดประจำเดือน 1,649 รายที่เป็นโรคกระดูกพรุน (BMD เกี่ยวกับเอวต่ำและกระดูกหักที่แพร่หลาย) และอายุเฉลี่ย 70 ปี การศึกษา TROPOS เกี่ยวข้องกับสตรีวัยหมดประจำเดือนจำนวน 5,091 รายที่เป็นโรคกระดูกพรุน (BMD ที่คอกระดูกต้นขาต่ำและกระดูกหักอย่างน้อยหนึ่งครั้งในผู้ป่วยมากกว่าครึ่งหนึ่ง) และอายุเฉลี่ย 77 ปี การศึกษาของ SOTI และ TROPOS ได้รวบรวมผู้ป่วย 1,556 รายที่อายุเกิน 80 ปี ณ เวลาที่รวมเข้าด้วยกัน (23.1% ของประชากรที่ศึกษา) ในการศึกษาทั้งสองนอกเหนือจากการรักษา (2 กรัม / วันของสตรอนเทียมหรือยาหลอก) ผู้ป่วยได้รับ การเสริมแคลเซียมและวิตามินดีอย่างเพียงพอ
OSSEOR ลดความเสี่ยงสัมพัทธ์ของการแตกหักของกระดูกสันหลังใหม่ 41% ในช่วง 3 ปีของการรักษาในการศึกษา SOTI (ตารางที่ 1) ผลมีนัยสำคัญตั้งแต่ปีแรกและแสดงให้เห็นประโยชน์ที่คล้ายคลึงกันในสตรีที่มีกระดูกหักหลายครั้งเมื่อลงทะเบียนเรียน (หมายถึงกระดูกหักที่เกี่ยวข้องกับอาการปวดหลังและ / หรือความสูงของร่างกายลดลงอย่างน้อย 1 ซม.) ความเสี่ยงสัมพัทธ์ลดลง 38% นอกจากนี้ OSSEOR ยังลดจำนวนผู้ป่วยที่มี "ความสูงของร่างกายลดลง" อย่างน้อย 1 ซม. เมื่อเทียบกับยาหลอก การประเมินคุณภาพชีวิตโดยใช้มาตราส่วน QUALIOST เฉพาะ ตลอดจนคะแนนการรับรู้ด้านสุขภาพทั่วไปของมาตราส่วน SF-36 ทั่วไป บ่งชี้ถึงประโยชน์ของ OSSEOR เมื่อเทียบกับยาหลอก
ประสิทธิภาพของ OSSEOR ในการลดความเสี่ยงของการแตกหักของกระดูกสันหลังใหม่ได้รับการยืนยันโดยการศึกษาของ TROPOS แม้ในผู้ป่วยโรคกระดูกพรุนที่ไม่มีกระดูกหักเปราะบางในขณะที่รวมเข้าด้วยกัน
การวิเคราะห์ร่วมกันของการศึกษา SOTI และ TROPOS พบว่าในผู้ป่วยที่อายุมากกว่า 80 ปีในขณะที่รวม OSSEOR ลดความเสี่ยงของกระดูกหักใหม่ลง 32% ในช่วง 3 ปีของการรักษา (อุบัติการณ์ 19, 1% ด้วย สตรอนเทียม ranelate เทียบกับ 26.5% กับยาหลอก)
ในบทวิเคราะห์เดียว ในภายภาคหน้า ของผู้ป่วยในการศึกษา SOTI และ TROPOS ที่มีกระดูกสันหลังส่วนเอวและ / หรือกระดูกต้นขาในช่วง osteopenic ในช่วงเวลาของการรวมและไม่มีกระดูกหักที่แพร่หลาย แต่มีปัจจัยเสี่ยงการแตกหักเพิ่มเติมอย่างน้อยหนึ่งรายการ (N = 176) OSSEOR ลดความเสี่ยง ของกระดูกสันหลังหักครั้งแรก 72% ใน 3 ปี (อุบัติการณ์ของกระดูกสันหลังหัก 3.6% เมื่อใช้สตรอนเทียม ราเนเลต เทียบกับ 12.0% เมื่อใช้ยาหลอก)
บทวิเคราะห์ ในภายภาคหน้า ดำเนินการในกลุ่มย่อยของผู้ป่วย TROPOS ที่มีความสนใจทางการแพทย์เป็นพิเศษและมีความเสี่ยงสูงที่จะเกิดการแตกหัก [กำหนดเป็นผู้ป่วยที่มี BMD T-score ที่คอต้นขา ≤-3 SD (ช่วงของผู้ผลิตที่สอดคล้องกับ -2.4 SD ตาม NHANES III) และ " อายุ> 74 ปี (n = 1,977 กล่าวคือ 40% ของประชากรที่ศึกษา TROPOS)]
ในกลุ่มนี้ การรักษานานกว่า 3 ปี OSSEOR ลดความเสี่ยงของการเกิดกระดูกสะโพกหักได้ 36% เมื่อเทียบกับยาหลอก (ตารางที่ 2)
การรักษาโรคกระดูกพรุนในผู้ชาย
ประสิทธิภาพของ OSSEOR แสดงให้เห็นในผู้ชายที่เป็นโรคกระดูกพรุนในการศึกษาแบบ double-blind ที่ควบคุมด้วยยาหลอก เป็นเวลา 2 ปี โดยมีการวิเคราะห์หลักที่ดำเนินการหลังจากหนึ่งปีในผู้ป่วย 243 ราย (ประชากร ความตั้งใจที่จะรักษาผู้ป่วย 161 รายที่ได้รับการรักษาด้วยสตรอนเทียมราเนเลต) ที่มีความเสี่ยงสูงที่จะกระดูกหัก (อายุเฉลี่ย 72.7 ปี; BMD เฉลี่ยเอวที่มีคะแนน T -2.6; 28% กระดูกหักที่แพร่หลาย)
ผู้ป่วยทุกรายได้รับอาหารเสริมแคลเซียม (1000 มก.) และวิตามินดี (800 IU) ทุกวัน
การเพิ่มขึ้นอย่างมีนัยสำคัญทางสถิติในค่า BMD สังเกตได้เร็วถึง 6 เดือนนับจากเริ่มการรักษาด้วย OSSEOR เมื่อเทียบกับยาหลอก
ค่า BMD เฉลี่ยของกระดูกสันหลังส่วนเอวเพิ่มขึ้นอย่างมีนัยสำคัญทางสถิติในช่วง 12 เดือน เกณฑ์ประสิทธิภาพหลัก (E (SE) = 5.32%; 95% CI = [3.86; 6.79] : p วัยหมดประจำเดือน
มีการสังเกตการเพิ่มขึ้นของค่า BMD ของคอกระดูกต้นขาและค่า BMD ของกระดูกต้นขาทั้งหมดอย่างมีนัยสำคัญทางสถิติ (p
ประชากรเด็ก
European Medicines Agency ได้ยกเว้นภาระหน้าที่ในการส่งผลการศึกษากับ OSSEOR ในกลุ่มย่อยทั้งหมดของประชากรเด็กที่เป็นโรคกระดูกพรุน (ดูหัวข้อ 4.2 สำหรับข้อมูลเกี่ยวกับการใช้ในเด็ก)
05.2 "คุณสมบัติทางเภสัชจลนศาสตร์
Strontium ranelate ประกอบด้วยอะตอมของสตรอนเทียมที่เสถียร 2 อะตอมและโมเลกุลของกรด ranelic ซึ่งเป็นส่วนประกอบอินทรีย์ที่แสดงถึงการประนีประนอมที่ดีที่สุดในแง่ของน้ำหนักโมเลกุล เภสัชจลนศาสตร์ และการยอมรับของผลิตภัณฑ์ยา เภสัชจลนศาสตร์ของสตรอนเทียมและกรดราเนลิกได้รับการประเมินในอาสาสมัครชายหนุ่มที่มีสุขภาพดี ในสตรีวัยหมดประจำเดือนที่มีสุขภาพดี และในระหว่างการรักษาระยะยาว ในผู้ชายที่เป็นโรคกระดูกพรุน และในสตรีที่เป็นโรคกระดูกพรุนในวัยหมดประจำเดือน รวมทั้งผู้สูงอายุ
การดูดซึม การกระจาย การผูกมัดของกรดราเนลิกกับโปรตีนในพลาสมานั้นต่ำเนื่องจากมีขั้วสูง ไม่มีการสะสมของกรด ranelic และไม่มีหลักฐานการเผาผลาญในสัตว์และมนุษย์ กรด ranelic ที่ดูดซึมจะถูกกำจัดอย่างรวดเร็วโดยไม่เปลี่ยนแปลงทางปัสสาวะ
การดูดซึม
การดูดซึมสตรอนเทียมสัมบูรณ์คือ 25% (ช่วง 19-27%) หลังจากรับประทานสตรอนเทียมราเนเลต 2 กรัมทางปาก ความเข้มข้นในพลาสมาสูงสุดจะอยู่ที่ 3-5 ชั่วโมงหลังจากรับประทานครั้งเดียว 2 กรัม
ถึงสภาวะคงที่หลังจากการรักษา 2 สัปดาห์ การรับประทานสตรอนเทียมราเนเลตร่วมกับแคลเซียมหรืออาหารช่วยลดการดูดซึมสตรอนเทียมได้ประมาณ 60 - 70% เมื่อเทียบกับการให้ยา 3 ชั่วโมงหลังอาหาร เนื่องจากการดูดซึมสตรอนเทียมค่อนข้างช้า จึงควรหลีกเลี่ยงการบริโภคอาหารและแคลเซียมก่อนและหลังรับประทาน OSSEOR . การเสริมวิตามินดีในช่องปากไม่รบกวนการสัมผัสสตรอนเทียม
การกระจาย
สตรอนเทียมมีปริมาตรการกระจายประมาณ 1 ลิตรต่อกิโลกรัม ความผูกพันของสตรอนเทียมกับโปรตีนในพลาสมาของมนุษย์อยู่ในระดับต่ำ (25%) และสตรอนเทียมมี "ความสัมพันธ์ที่ดีกับเนื้อเยื่อกระดูก การวัดความเข้มข้นของสตรอนเทียมในการตรวจชิ้นเนื้อกระดูกอุ้งเชิงกรานของผู้ป่วยที่รักษานานถึง 60 เดือนด้วยสตรอนเทียมราเนเลต 2 กรัมต่อวัน แสดงให้เห็นว่าความเข้มข้นของสตรอนเทียมในกระดูกสามารถไปถึงที่ราบสูงได้หลังจากการรักษาประมาณ 3 ปี ไม่มีข้อมูลผู้ป่วยที่แสดงให้เห็นถึงจลนพลศาสตร์ของการกำจัดสตรอนเทียมออกจากกระดูกหลังจากหยุดยา
การเปลี่ยนแปลงทางชีวภาพ
ในฐานะที่เป็นไอออนบวกแบบไดวาเลนต์ สตรอนเทียมจะไม่ถูกเผาผลาญ Strontium ranelate ไม่ยับยั้งเอนไซม์ cytochrome P450
การกำจัด
การกำจัดสตรอนเทียมขึ้นอยู่กับเวลาและปริมาณการใช้สตรอนเทียมครึ่งชีวิตที่มีประสิทธิภาพคือประมาณ 60 ชั่วโมง การขับธาตุสตรอนเทียมเกิดขึ้นทางไตและทางเดินอาหาร ระดับพลาสมาจะอยู่ที่ประมาณ 12 มล. / นาที (CV 22%) และการล้างไตประมาณ 7 มล. / นาที (CV 28%)
เภสัชจลนศาสตร์ในประชากรโดยเฉพาะ
ผู้ป่วยสูงอายุ
ข้อมูลเภสัชจลนศาสตร์ของประชากรพบว่าไม่มีความสัมพันธ์ระหว่างอายุกับการกวาดล้างสตรอนเทียมในประชากรเป้าหมาย
ไตล้มเหลว
ในผู้ป่วยที่มีความบกพร่องทางไตในระดับปานกลางถึงปานกลาง (creatinine clearance 30-70 mL / min) การกวาดล้างสตรอนเซียมจะลดลงเมื่อการกวาดล้างของ creatinine ลดลง (ประมาณ 30% ลดลงในช่วงการกวาดล้าง creatinine 30 ถึง 70 มล. / นาที) สิ่งนี้นำไปสู่การเพิ่มขึ้น ในระดับสตรอนเทียมในพลาสมา ในการศึกษาระยะที่ 3 ผู้ป่วย 85% มีระดับครีเอตินินระหว่าง 30 ถึง 70 มล. / นาที 6% น้อยกว่า 30 มล. / นาทีในการรวมและการกวาดล้างครีเอตินินเฉลี่ย 50 มล. / นาที ดังนั้น ไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยไตวายระดับปานกลางถึงปานกลางไม่มีข้อมูลทางเภสัชจลนศาสตร์ในผู้ป่วยไตวายขั้นรุนแรง (creatinine clearance)
ตับไม่เพียงพอ
ไม่มีข้อมูลเภสัชจลนศาสตร์ในผู้ป่วยที่มีภาวะตับไม่เพียงพอ เนื่องจากคุณสมบัติทางเภสัชจลนศาสตร์ของสตรอนเทียมจึงไม่คาดว่าจะมีผล
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ข้อมูลที่ไม่ใช่ทางคลินิกเผยให้เห็นว่าไม่มีอันตรายเป็นพิเศษสำหรับมนุษย์จากการศึกษาทั่วไปของ เภสัชวิทยาความปลอดภัย, ความเป็นพิษต่อพันธุกรรม, ศักยภาพในการก่อมะเร็ง.
ในสัตว์ฟันแทะ การให้สตรอนเทียมราเนเลตในปริมาณสูงในช่องปากอย่างเรื้อรังส่งผลให้กระดูกและฟันผิดปกติ ซึ่งประกอบด้วยการแตกหักที่เกิดขึ้นเองตามธรรมชาติและการเกิดแร่ธาตุที่ล่าช้า โดยสามารถย้อนกลับได้หลังจากหยุดการรักษา พบผลกระทบเหล่านี้โดยมีระดับสตรอนเทียมในกระดูกสูงกว่าระดับที่พบในมนุษย์ 2-3 เท่าหลังการรักษานานถึง 3 ปี ข้อมูลเกี่ยวกับการสะสมของสตรอนเทียมราเนเลตในโครงกระดูกเมื่อสัมผัสเป็นเวลานานมีจำกัด
การศึกษาความเป็นพิษต่อพัฒนาการส่งผลให้เกิดความผิดปกติของกระดูกและฟันในลูกของหนูและกระต่าย (เช่น การโค้งคำนับของกระดูกยาวและซี่โครงเป็นคลื่น) ผลกระทบเหล่านี้สามารถย้อนกลับได้ 8 สัปดาห์หลังจากหยุดการรักษา
การประเมินความเสี่ยงด้านสิ่งแวดล้อม (ERA)
การประเมินความเสี่ยงด้านสิ่งแวดล้อมของสตรอนเทียมราเนเลตได้ดำเนินการตามหลักเกณฑ์ของยุโรปที่เกี่ยวข้องกับ ERA
Strontium ranelate ไม่ก่อให้เกิดความเสี่ยงต่อสิ่งแวดล้อม
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
แอสปาร์แตม (E951)
มอลโตเด็กซ์ตริน
แมนนิทอล (E421)
06.2 ความเข้ากันไม่ได้
ไม่เกี่ยวข้อง
06.3 ระยะเวลาที่ใช้ได้
- 3 ปี
- เมื่อละลายในน้ำแล้ว สารแขวนลอยจะคงตัวเป็นเวลา 24 ชั่วโมง อย่างไรก็ตาม ขอแนะนำให้ดื่มสารแขวนลอยทันทีหลังจากเตรียมอาหาร (ดูหัวข้อ 4.2)
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
ยานี้ไม่ต้องการเงื่อนไขการเก็บรักษาพิเศษใด ๆ
สำหรับสภาวะการเก็บรักษาหลังการสร้างผลิตภัณฑ์ยาใหม่ ดูหัวข้อ 6.3
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
กระดาษ / เอทิลีน / อลูมิเนียม / ถุงโพลีเอทิลีน
แพ็ค
แพ็ค 7, 14, 28, 56, 84 หรือ 100 ซอง
ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
06.6 คำแนะนำในการใช้งานและการจัดการ
ไม่มีคำแนะนำพิเศษ
07.0 ผู้ทรงอำนาจการตลาด
LES LABORATOIRES SERVIER
50, rue Carnot
92284 Suresnes cedex
ฝรั่งเศส
08.0 หมายเลขอนุญาตการตลาด
EU / 1/04/287/001
EU / 1/04/287/002
EU / 1/04/287/003
EU / 1/04/287/004
EU / 1/04/287/005
EU / 1/04/287/006
036588061
036588022
036588034
036588046
036588010
036588059
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
วันที่ได้รับอนุญาตครั้งแรก: 21 กันยายน 2547
วันที่ต่ออายุครั้งล่าสุด: 21 กันยายน 2557