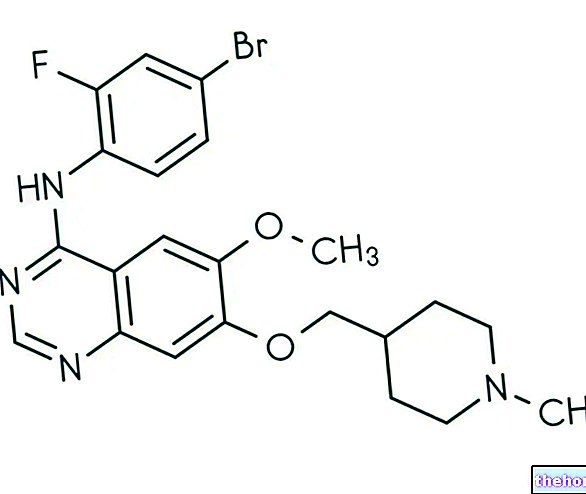
ความหมายของออสโมซิส
ออสโมซิสเป็นทางผ่านที่เกิดขึ้นเองของตัวทำละลาย (ซึ่งในระบบทางชีววิทยามักจะเป็นน้ำ) จากสารละลายที่ตัวถูกละลายจะเจือจางมากขึ้นเพื่อให้มีความเข้มข้นมากขึ้น การเคลื่อนไหวนี้ - ซึ่งเกิดขึ้นผ่านเมมเบรนแบบกึ่งซึมผ่านได้ - ดำเนินต่อไปจนกว่าจะถึงสถานการณ์สมดุลซึ่งทั้งสองโซลูชั่นได้รับและรักษาความเข้มข้นเท่ากัน
ตัวอย่างการปฏิบัติ

เพื่อให้แนวคิดเรื่องออสโมซิสชัดเจนขึ้น ให้ลองนึกภาพว่าเรามีภาชนะที่แบ่งออกเป็นสองส่วนที่มีปริมาตรเท่ากัน (A และ B) ด้วยเมมเบรนแบบกึ่งซึมผ่านได้ (นั่นคือ ซึมผ่านได้เฉพาะตัวทำละลาย - ในกรณีนี้คือน้ำ - ไม่ใช่กับ ตัวละลาย) ช่อง A มีสารละลายในน้ำซึ่งละลายกลูโคสหนึ่งช้อนโต๊ะในขณะที่ในส่วน B เรามีสารละลายน้ำที่มีปริมาตรเท่ากันซึ่งละลายกลูโคสสามช้อนโต๊ะ ความแตกต่างทำให้เกิดการไล่ระดับความเข้มข้นของกลูโคสที่ด้านข้างของเยื่อหุ้มเซลล์ และเนื่องจากน้ำตาลนี้ไม่สามารถข้ามผ่านได้ จึงถึงจุดสมดุลเมื่อน้ำผ่านจากช่อง A (โดยที่กลูโคสจะเจือจางมากขึ้น) ไปยังช่อง B (ซึ่งมีปริมาณมากกว่า ). หากคุณต้องการ อาจกล่าวได้ว่าน้ำผ่านออสโมซิสจากสารละลายที่มีความเข้มข้นมากกว่า (A) ไปยังน้ำที่มีความเข้มข้นน้อยกว่า (B)
หลังจากไหลนี้ ระดับน้ำใน B จะเพิ่มขึ้นและลดลงใน A ทำให้เกิดความแตกต่างในระดับหนึ่งระหว่างทั้งสอง ปรากฏการณ์นี้จะสิ้นสุดลงเมื่อสารละลายทั้งสองมีความเข้มข้นเท่ากัน จากนั้นให้คงที่
สารละลายไฮโปโทนิก ไอโซโทนิก และไฮเปอร์โทนิก
การใช้สารละลายสองชนิดที่มีความเข้มข้นของโมลาร์ต่างกัน (จำนวนอนุภาคที่ละลายในสารละลายต่างกัน) สารละลายที่มีความเข้มข้นของโมลาร์ต่ำที่สุดจะถูกกำหนดให้เป็นไฮโปโทนิกและสารละลายที่มีความเข้มข้นสูงกว่าคือไฮเปอร์โทนิก สารละลายสองชนิดแทน isotonic (หรือ equimolar) เมื่อมีความเข้มข้นเท่ากัน
ในตัวอย่างที่เพิ่งสร้าง สารละลาย B คือไฮเปอร์โทนิก (ดังนั้นจึงมีตัวถูกละลายมากกว่า) มากกว่าตัวอื่น (นิยามเป็นไฮโปโทนิก) ดังนั้น ภายใต้สภาวะปกติ ตัวทำละลายจะเคลื่อนที่โดยการออสโมซิสจากไฮโปโทนิกไปเป็นสารละลายไฮเปอร์โทนิก เราพูดถึงเงื่อนไขมาตรฐานเพราะเล่นกับกฎของฟิสิกส์ เป็นไปได้ที่จะล้มล้างแนวคิดออสโมซิสและชอบการผ่านของตัวทำละลายจากความเข้มข้นที่เจือจางที่สุดไปยังความเข้มข้นสูงสุด (รีเวิร์สออสโมซิส)
แรงดันออสโมติกและรีเวิร์สออสโมซิส
ดังที่แสดงไว้จนถึงตอนนี้ การไหลสุทธิของตัวทำละลาย - ที่เกิดจากออสโมซิส - จะดำเนินต่อไปจนกว่าสารละลายทั้งสองจะมีความเข้มข้นเท่ากันการเคลื่อนไหวนี้สามารถตอบโต้ หยุด หรือย้อนกลับได้โดยใช้แรงกดไปยังส่วนที่มีความเข้มข้นสูงสุด

ในตัวอย่างที่แล้ว การวางลูกสูบในช่อง B (ซึ่งเราจำได้ว่ามีความเข้มข้นสูงกว่า) และกดลงไปด้วยแรงบางอย่างก็เพียงพอแล้ว เพื่อให้น้ำไหลไปทาง A มากขึ้น ในกรณีนี้ เราพูดถึงสิ่งที่ตรงกันข้าม ออสโมซิส
แรงดันออสโมติกคือแรงดันที่ตรงข้ามทางเดินของตัวทำละลายผ่านเมมเบรนแบบกึ่งโปร่งใส ดังนั้นจึงเป็นความดันที่จำเป็นในการต่อต้านออสโมซิส
สำหรับสิ่งที่กล่าวไปแล้ว สารละลายไอโซโทนิกสองชนิดมีแรงดันออสโมติกเท่ากัน ดังนั้นควรเน้นว่าแรงดันออสโมติกขึ้นอยู่กับจำนวนของอนุภาคที่มีอยู่ในสารละลายเท่านั้นและไม่ได้ขึ้นอยู่กับลักษณะของพวกมัน
ออสโมซิสกับร่างกายมนุษย์
พลาสมาเมมเบรนที่ล้อมรอบเซลล์ของร่างกายมนุษย์อันที่จริงแล้วเป็นเยื่อกึ่งซึมผ่านได้ซึ่งทำให้โมเลกุลขนาดเล็ก (เช่นน้ำและยูเรีย) สามารถผ่านได้โดยตรงผ่านออสโมซิส (เช่นน้ำและยูเรีย) แต่ไม่ใช่ของที่มีน้ำหนักโมเลกุลมากกว่า ( เช่น โปรตีน กรดอะมิโน และน้ำตาล) ความสมดุลของออสโมติกในของเหลวในร่างกายจึงเป็นสิ่งจำเป็นเพื่อรับประกันว่าเซลล์จะมีสภาพแวดล้อมที่เหมาะสมที่สุดในการดำรงชีวิต
หากเรานำเซลล์ที่เหมือนกับเซลล์เม็ดเลือดแดงมาจุ่มลงในสารละลายไฮโปโทนิก สิ่งนี้ - โดยออสโมซิส - จะเกิดการบวม (เกิดจากการเข้าของน้ำ) ซึ่งอาจทำให้ระเบิดได้ ในทางกลับกัน หากแช่อยู่ใน สารละลายไฮเปอร์โทนิกที่เซลล์ผ่านเข้าไป เนื่องจากน้ำไหลออกสู่ภายนอก ทำให้เกิดภาวะขาดน้ำอย่างรุนแรงซึ่งทำให้เกิดรอยย่น โชคดีที่เซลล์ในร่างกายของมนุษย์ถูกแช่อยู่ในสารละลายไอโซโทนิกตามสภาพแวดล้อมภายใน และมีระบบต่างๆ ที่จะเก็บของเหลวเหล่านี้ให้อยู่ในสมดุลออสโมติก
แรงดันออสโมติกและการจัดเก็บอาหาร
ลองคิดดูสักครู่เกี่ยวกับแยมโฮมเมด ... น้ำตาลถูกเติมเข้าไปอย่างมากมาย ไม่เพียงแต่จะปรับปรุงรสชาติเท่านั้น แต่ยังเพิ่มอายุการเก็บรักษาอีกด้วย กระนั้น น้ำตาลเป็นองค์ประกอบสำคัญสำหรับชีวิตของจุลินทรีย์หลายชนิดที่เกี่ยวข้องกับการย่อยสลายของผลิตภัณฑ์ ความขัดแย้งที่เห็นได้ชัดนี้ถูกรื้อถอนโดยแนวคิดเรื่องออสโมซิส





.jpg)











-non-sentire-gli-odori.jpg)