สารออกฤทธิ์: Clopidogrel
Plavix 75 มก. เม็ดเคลือบฟิล์ม
เม็ดมีดสำหรับบรรจุภัณฑ์ Plavix มีจำหน่ายสำหรับขนาดบรรจุภัณฑ์:- Plavix 75 มก. เม็ดเคลือบฟิล์ม
- Plavix 300 มก. เม็ดเคลือบฟิล์ม
ทำไมจึงใช้ Plavix? มีไว้เพื่ออะไร?
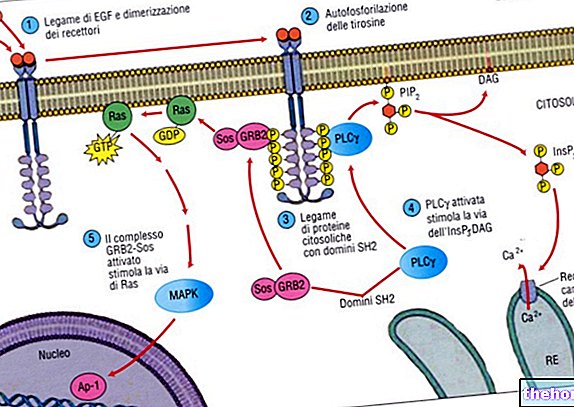
Plavix มี clopidogrel และอยู่ในกลุ่มยาที่เรียกว่ายาต้านเกล็ดเลือด เกล็ดเลือดเป็นองค์ประกอบขนาดเล็กของเลือดที่เกาะกลุ่มกันระหว่างการแข็งตัวของเลือด ยาต้านเกล็ดเลือดจะลดโอกาสการเกิดลิ่มเลือด (ปรากฏการณ์ที่เรียกว่าลิ่มเลือดอุดตัน) โดยการป้องกันการจับตัวเป็นก้อนนี้
ผู้ใหญ่ใช้ Plavix เพื่อป้องกันไม่ให้ลิ่มเลือด (thrombi) ก่อตัวในหลอดเลือดที่แข็งตัว (หลอดเลือดแดง) ซึ่งเป็นกระบวนการที่เรียกว่า atherothrombosis ซึ่งอาจทำให้เกิดเหตุการณ์ atherothrombotic (เช่นโรคหลอดเลือดสมองหัวใจวายหรือความตาย) Plavix ถูกกำหนดให้คุณช่วยป้องกันลิ่มเลือดและเพื่อลดความเสี่ยงของเหตุการณ์ร้ายแรงเหล่านี้เนื่องจาก:
- คุณมีภาวะที่เรียกว่าการแข็งตัวของหลอดเลือดแดง (เรียกอีกอย่างว่าหลอดเลือด) e
- คุณเคยมีอาการหัวใจวาย โรคหลอดเลือดสมอง หรือภาวะที่เรียกว่าโรคหลอดเลือดแดงส่วนปลาย หรือ
- ก่อนหน้านี้คุณเคยมีอาการเจ็บหน้าอกอย่างรุนแรงที่เรียกว่า 'unstable angina' หรือ 'myocardial infarction' (หัวใจวาย) ในการรักษาภาวะนี้ แพทย์ของคุณอาจใส่ขดลวดในหลอดเลือดแดงที่อุดตันหรือตีบเพื่อฟื้นฟูการไหลเวียนของเลือด แพทย์ของคุณอาจกำหนดกรดอะซิติลซาลิไซลิก (สารที่พบในยาหลายชนิดที่ใช้บรรเทาอาการปวดและลดไข้ เช่น ป้องกันการแข็งตัวของเลือด)
- คุณมีการเต้นของหัวใจผิดปกติ ภาวะที่เรียกว่า 'atrial fibrillation' และไม่สามารถใช้ยาที่เรียกว่า 'สารกันเลือดแข็งในช่องปาก' (ตัวรับวิตามินเค) ซึ่งป้องกันไม่ให้เกิดลิ่มเลือดใหม่ก่อตัวและพัฒนาสิ่งที่มีอยู่ คุณจะได้รับแจ้งว่า "สารต้านการแข็งตัวของเลือดในช่องปาก" มีประสิทธิภาพมากกว่ากรดอะซิติลซาลิไซลิกหรือการใช้ Plavix และกรดอะซิติลซาลิไซลิกร่วมกันในการรักษาภาวะนี้หากคุณไม่สามารถใช้ "ยาต้านการแข็งตัวของเลือดในช่องปาก" ได้ และไม่มีความเสี่ยงต่อการตกเลือดมากขึ้น แพทย์ของคุณอาจสั่งยา Plavix ร่วมกับกรดอะซิติลซาลิไซลิก
ข้อห้าม เมื่อไม่ควรใช้ Plavix
อย่าใช้ Plavix
- หากคุณแพ้ (แพ้ง่าย) ต่อ clopidogrel หรือส่วนผสมอื่นๆ ของยานี้ (ระบุไว้ในหัวข้อ 6)
- หากคุณมีเลือดออกเช่นแผลในกระเพาะอาหารหรือมีเลือดออกที่บริเวณสมอง
- หากคุณมีโรคตับรุนแรง
หากคุณคิดว่าสิ่งเหล่านี้ใช้ได้กับคุณ หรือหากคุณมีข้อสงสัยใดๆ เลย โปรดปรึกษาแพทย์ของคุณก่อนใช้ Plavix
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนรับประทาน Plavix
หากเกิดสถานการณ์ใด ๆ ที่กล่าวถึงด้านล่าง แจ้งให้แพทย์ทราบก่อนใช้ยา Plavix:
- หากคุณมีความเสี่ยงต่อการตกเลือด เช่น: - ภาวะทางการแพทย์ที่ทำให้คุณเสี่ยงต่อการตกเลือดภายใน (เช่น "แผลในกระเพาะอาหาร) - ความผิดปกติของเลือดที่ทำให้คุณมีแนวโน้มที่จะมีเลือดออกภายใน (เลือดออกภายในเนื้อเยื่อ อวัยวะ หรือร่างกาย) ข้อต่อ) - อาการบาดเจ็บร้ายแรงล่าสุด - การผ่าตัดล่าสุด (รวมถึงการทำฟัน) - การผ่าตัด (รวมถึงการผ่าตัดทางทันตกรรม) ที่กำหนดไว้สำหรับ 7 วันถัดไป
- หากคุณมีก้อนใน "หลอดเลือดแดงของสมอง (ischemic stroke) ที่เกิดขึ้นภายใน 7 วันที่ผ่านมา
- หากคุณมีโรคไตหรือตับ
- หากคุณเคยมีอาการแพ้หรือมีปฏิกิริยากับยาใด ๆ ที่ใช้รักษาโรคของคุณ
ในขณะที่คุณกำลังใช้ Plavix:
- คุณต้องแจ้งให้แพทย์ทราบหากต้องการเข้ารับการผ่าตัด (รวมทั้งการผ่าตัดทางทันตกรรม)
- คุณควรแจ้งให้แพทย์ทราบทันทีหากคุณมีอาการป่วย (หรือที่เรียกว่า Thrombotic Thrombocytopenic Purpura หรือ PTT) ซึ่งรวมถึงไข้และรอยฟกช้ำใต้ผิวหนังที่ปรากฏเป็นจุดสีแดง โดยมีหรือไม่มีอาการอ่อนล้าอย่างรุนแรง สับสน ผิวเหลือง หรือตา (ดีซ่าน) (ดูหัวข้อที่ 4 "ผลข้างเคียงที่เป็นไปได้")
- หากคุณกรีดหรือทำร้ายตัวเอง อาจใช้เวลานานกว่าปกติกว่าที่เลือดจะหยุดไหล นี่เป็นเพราะวิธีการทำงานของยาเนื่องจากป้องกันไม่ให้เกิดลิ่มเลือด สำหรับบาดแผลเล็กน้อยและการบาดเจ็บ เช่น กรีดตัวเองหรือโกนหนวด ปกติแล้วจะไม่เป็นปัญหา อย่างไรก็ตาม หากคุณกังวลเรื่องเลือดออก คุณควรติดต่อแพทย์ทันที (ดูหัวข้อ 4 'ผลข้างเคียงที่เป็นไปได้')
- แพทย์ของคุณอาจสั่งการตรวจเลือด
เด็กและวัยรุ่น
อย่าให้ยานี้แก่เด็กเนื่องจากไม่ได้ผล
ปฏิกิริยา ยาหรืออาหารใดที่อาจเปลี่ยนผลของ Plavix
แจ้งให้แพทย์หรือเภสัชกรทราบหากคุณกำลังรับประทาน หรืออาจกำลังใช้ยาอื่นอยู่ หรือแม้แต่ยาที่ได้รับโดยไม่มีใบสั่งยา
ยาบางชนิดอาจส่งผลต่อการใช้ Plavix หรือในทางกลับกัน
คุณต้องแจ้งให้แพทย์ทราบอย่างแน่ชัดหากคุณกำลัง:
- ยาต้านการแข็งตัวของเลือด ยาที่ใช้ลดการแข็งตัวของเลือด
- ยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ โดยทั่วไปใช้รักษาอาการเจ็บปวดและ/หรืออาการอักเสบของกล้ามเนื้อหรือข้อต่อ
- เฮปารินหรือยาฉีดอื่น ๆ ที่ใช้ในการลดการแข็งตัวของเลือด
- omeprazole, esomeprazole หรือ cimetidine, ยาที่ใช้รักษาอาการกระเพาะ,
- fluconazole, voriconazole, ciprofloxacin หรือ chloramphenicol ยาที่ใช้รักษาการติดเชื้อแบคทีเรียหรือเชื้อรา
- carbamazepine หรือ oxcarbazepine ยาที่ใช้รักษาโรคลมบ้าหมูบางรูปแบบ
- ทิคโลพิดีน, ยาต้านเกล็ดเลือดอื่นๆ,
- ตัวยับยั้งการรับ serotonin reuptake inhibitor (รวมถึงแต่ไม่จำกัดเพียง fluoxetine หรือ fluvoxamine) ยาที่ปกติใช้รักษาอาการซึมเศร้า
- moclobemide ยาที่ใช้รักษาอาการซึมเศร้า
หากคุณมีอาการเจ็บหน้าอกอย่างรุนแรง (โรคหลอดเลือดหัวใจตีบหรือหัวใจวายที่ไม่เสถียร) คุณอาจได้รับยา Plavix ร่วมกับกรดอะซิติลซาลิไซลิก ซึ่งเป็นสารที่พบในยาหลายชนิดที่ใช้บรรเทาอาการปวดและลดไข้ การใช้กรดอะซิติลซาลิไซลิกเป็นครั้งคราว (ไม่เกิน 1,000 มก. ใน 24 ชั่วโมง) โดยทั่วไปจะไม่ทำให้เกิดปัญหา แต่ควรปรึกษาหารือกับแพทย์หากใช้เป็นเวลานานในสถานการณ์อื่น
Plavix พร้อมอาหารและเครื่องดื่ม
Plavix สามารถรับประทานได้ทั้งที่มีหรือไม่มีอาหาร
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
การตั้งครรภ์และให้นมบุตร
ไม่ควรรับประทานยานี้ในระหว่างตั้งครรภ์
หากคุณกำลังตั้งครรภ์หรือสงสัยว่าคุณกำลังตั้งครรภ์ คุณควรแจ้งให้แพทย์หรือเภสัชกรทราบก่อนใช้ยา Plavix หากคุณตั้งครรภ์ขณะรับประทาน Plavix ให้ปรึกษาแพทย์ทันที เนื่องจากไม่แนะนำให้รับประทาน Plavix ระหว่างตั้งครรภ์
คุณไม่ควรให้นมลูกขณะทานยานี้ หากคุณกำลังให้นมบุตรหรือวางแผนที่จะให้นมลูก ปรึกษาแพทย์ก่อนใช้ยานี้
ปรึกษาแพทย์หรือเภสัชกรเพื่อขอคำแนะนำก่อนรับประทานยาใดๆ
การขับรถและการใช้เครื่องจักร
Plavix ไม่น่าจะส่งผลกระทบต่อความสามารถในการขับและใช้งานเครื่องจักร
Plavix มีแลคโตส
หากคุณได้รับแจ้งจากแพทย์ว่าคุณมี "การแพ้น้ำตาลบางชนิด (เช่น แลคโตส) ให้ปรึกษาแพทย์ก่อนใช้ยานี้
Plavix มีน้ำมันละหุ่งเติมไฮโดรเจน
ซึ่งอาจทำให้ปวดท้องหรือท้องเสียได้
ปริมาณวิธีและเวลาในการบริหาร วิธีใช้ Plavix: Posology
ใช้ยานี้ตามที่แพทย์หรือเภสัชกรบอกเสมอ
หากมีข้อสงสัย ควรปรึกษาแพทย์หรือเภสัชกร หากคุณมีอาการเจ็บหน้าอกอย่างรุนแรง (โรคหลอดเลือดหัวใจตีบหรือหัวใจวายไม่คงที่) แพทย์ของคุณอาจให้ Plavix 300 มก. (1 เม็ด 300 มก. หรือ 4 เม็ด 75 มก.) แก่คุณหนึ่งครั้งในช่วงเริ่มการรักษา หลังจากนั้น ปริมาณที่แนะนำคือ Plavix 75 มก. หนึ่งเม็ดต่อวันโดยรับประทานโดยมีหรือไม่มีอาหารและในเวลาเดียวกันในแต่ละวัน
ต้องใช้ Plavix ตราบเท่าที่แพทย์เห็นว่าจำเป็น
ยาเกินขนาด จะทำอย่างไรถ้าคุณได้รับ Plavix มากเกินไป
หากคุณทาน Plavix มากกว่าที่ควร
ติดต่อแพทย์หรือห้องฉุกเฉินของโรงพยาบาลที่ใกล้ที่สุดเนื่องจากมีความเสี่ยงที่จะมีเลือดออกเพิ่มขึ้น
หากคุณลืมทานยา Plavix
หากคุณลืมกินยา แต่นึกได้ภายใน 12 ชั่วโมงของเวลาปกติ ให้กินหนึ่งเม็ดทันที แล้วกินเม็ดต่อไปตามเวลาปกติ
หากเกิน 12 ชั่วโมง ให้รับประทานยาตามปกติตามเวลาปกติ อย่ารับประทานยา 2 เท่าเพื่อทดแทนยาเม็ดที่ลืม
สำหรับแพ็คขนาด 7, 14, 28 และ 84 เม็ด คุณสามารถตรวจสอบวันที่รับประทานยาเม็ด Plavix ครั้งสุดท้ายได้โดยตรวจสอบปฏิทินที่พิมพ์บนตุ่ม
หากคุณหยุดใช้ Plavix
อย่าหยุดการรักษาเว้นแต่แพทย์จะสั่ง ก่อนหยุดให้ติดต่อแพทย์หรือเภสัชกรของคุณ
หากคุณมีคำถามเพิ่มเติมเกี่ยวกับการใช้ยานี้ ให้สอบถามแพทย์หรือเภสัชกรของคุณ
ผลข้างเคียงของ Plavix คืออะไร?
เช่นเดียวกับยาทั้งหมด ยานี้สามารถทำให้เกิดผลข้างเคียงได้ แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
ติดต่อแพทย์ของคุณทันทีหาก:
- ไข้ สัญญาณของการติดเชื้อหรือความอ่อนแออย่างรุนแรง ผลกระทบเหล่านี้อาจเกิดจากการลดลงในเซลล์เม็ดเลือดบางชนิด
- สัญญาณของปัญหาตับ เช่น ผิวเหลืองและ/หรือตาเหลือง (ดีซ่าน) มีหรือไม่มีเลือดออกซึ่งปรากฏใต้ผิวหนังเป็นจุดระบุสีแดง และ/หรือสับสน (ดูหัวข้อที่ 2 "คำเตือนและข้อควรระวัง")
- บวมในปากหรือผิวหนังผิดปกติ เช่น ผื่น คัน พุพองของผิวหนัง สิ่งเหล่านี้อาจเป็นสัญญาณของอาการแพ้
ผลข้างเคียงที่พบบ่อยที่สุดที่รายงานด้วย Plavix คือเลือดออก เลือดออกสามารถแสดงออกเป็นเลือดออกในกระเพาะอาหารหรือลำไส้ ช้ำ ช้ำ (เลือดออกผิดปกติหรือช้ำใต้ผิวหนัง) เลือดกำเดา เลือดในปัสสาวะ ในบางกรณี เลือดออกในตา กะโหลกศีรษะ ปอด และข้อต่อ
หากคุณมีเลือดออกเป็นเวลานานขณะรับประทาน Plavix
หากคุณกรีดหรือทำร้ายตัวเอง อาจใช้เวลานานกว่าปกติกว่าที่เลือดจะหยุดไหล นี่เป็นเพราะวิธีการทำงานของยาเนื่องจากป้องกันไม่ให้เกิดลิ่มเลือด สำหรับบาดแผลเล็กน้อยและการบาดเจ็บ เช่น กรีดตัวเองหรือโกนหนวด ปกติแล้วจะไม่เป็นปัญหา อย่างไรก็ตาม หากคุณกังวลเรื่องเลือดออก คุณควรติดต่อแพทย์ทันที (ดูหัวข้อ 2 'คำเตือนและข้อควรระวัง')
ผลข้างเคียงอื่น ๆ ได้แก่ :
ผลข้างเคียงที่พบบ่อย (อาจส่งผลกระทบถึง 1 ใน 10 ผู้ป่วย):
ท้องร่วง ท้องอืด อาหารไม่ย่อย หรืออิจฉาริษยา
ผลข้างเคียงที่ไม่ธรรมดา (อาจส่งผลกระทบถึง 1 ใน 100 ผู้ป่วย):
ปวดหัว, แผลในกระเพาะอาหาร, อาเจียน, คลื่นไส้, ท้องผูก, ก๊าซส่วนเกินในกระเพาะอาหารหรือลำไส้, ผื่น, คัน, เวียนศีรษะ, รู้สึกเสียวซ่าและชา
ผลข้างเคียงที่หายาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 ผู้ป่วย):
อาการเวียนศีรษะบ้านหมุน
ผลข้างเคียงที่หายากมาก (อาจส่งผลกระทบมากถึง 1 ใน 10,000 ผู้ป่วย):
ดีซ่าน ปวดท้องรุนแรงโดยมีหรือไม่มีอาการปวดหลัง ไข้, หายใจลำบากบางครั้งเกี่ยวข้องกับอาการไอ; อาการแพ้ทั่วๆ ไป (เช่น ความรู้สึกร้อนเป็นวงกว้างพร้อมกับอาการป่วยไข้ทั่วไปอย่างกะทันหันจนถึงเป็นลม) บวมในปาก; แผลพุพองของผิวหนัง แพ้ผิวหนัง; ปวดในปาก (เปื่อย); ลดความดันโลหิต ความสับสน ภาพหลอน; ปวดข้อ; ปวดกล้ามเนื้อ การเปลี่ยนแปลงในรสชาติ
นอกจากนี้ แพทย์ของคุณอาจระบุการเปลี่ยนแปลงในการตรวจเลือดและปัสสาวะของคุณ
การรายงานผลข้างเคียง
หากคุณได้รับผลข้างเคียง ให้ปรึกษาแพทย์หรือเภสัชกร ซึ่งรวมถึงผลข้างเคียงที่อาจเกิดขึ้นซึ่งไม่ได้ระบุไว้ในเอกสารฉบับนี้
คุณยังสามารถรายงานผลข้างเคียงได้โดยตรงผ่านระบบการรายงานระดับประเทศที่ระบุไว้ในภาคผนวก 5 โดยการรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
เก็บยานี้ให้พ้นสายตาและมือเด็ก
อย่าใช้ยานี้หลังจากวันหมดอายุซึ่งระบุไว้บนกล่องและตุ่มหลังจาก EXP วันหมดอายุหมายถึงวันสุดท้ายของเดือนนั้น
โปรดดูเงื่อนไขการจัดเก็บที่ระบุบนบรรจุภัณฑ์ด้านนอก หาก Plavix จำหน่ายในตุ่ม PVC / PVDC / อลูมิเนียม ให้เก็บที่อุณหภูมิต่ำกว่า 30 ° C หาก Plavix บรรจุในตุ่มอลูมิเนียม / อะลูมิเนียม ผลิตภัณฑ์ยาไม่จำเป็นต้องมีสภาวะการจัดเก็บพิเศษใดๆ
อย่าใช้ยานี้หากคุณสังเกตเห็นสัญญาณการเสื่อมสภาพที่มองเห็นได้
ห้ามทิ้งยาลงในน้ำเสียหรือของเสียในครัวเรือน ถามเภสัชกรว่าจะทิ้งยาที่ไม่ได้ใช้แล้วอย่างไร ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
องค์ประกอบและรูปแบบยา
สิ่งที่ Plavix มี
สารออกฤทธิ์คือ clopidogrel แต่ละเม็ดประกอบด้วย clopidogrel 75 มก. (ในรูปของไฮโดรเจนซัลเฟต)
ส่วนผสมอื่นๆ ได้แก่ (ดูหัวข้อที่ 2 "Plavix ประกอบด้วยแลคโตส" และ "Plavix ประกอบด้วยน้ำมันละหุ่งเติมไฮโดรเจน"):
- แกนแท็บเล็ต: แมนนิทอล (E421), น้ำมันละหุ่งเติมไฮโดรเจน, เซลลูโลส microcrystalline, macrogol 6000 และไฮดรอกซีโพรพิลเซลลูโลสทดแทนต่ำ,
- การเคลือบแท็บเล็ต: แลคโตสโมโนไฮเดรต (น้ำตาลนม), ไฮโปรเมลโลส (E464), ไตรอะซิติน (E1518), เหล็กออกไซด์สีแดง (E 172), ไททาเนียมไดออกไซด์ (E 171)
- สารขัดเงา: ขี้ผึ้ง carnauba
สิ่งที่ Plavix ดูเหมือนและเนื้อหาของแพ็ค
ยาเม็ดเคลือบฟิล์ม Plavix 75 มก. มีลักษณะกลม เหลี่ยมสองด้าน สีชมพู แกะลายด้วยหมายเลข "75" ด้านหนึ่งและหมายเลข "1171" อีกด้านหนึ่ง Plavix บรรจุในกล่องบรรจุที่ประกอบด้วย:
- 7, 14, 28, 30, 84, 90 และ 100 เม็ดใน PVC / PVDC / ตุ่มอลูมิเนียมหรืออลูมิเนียม / พองอลูมิเนียม,
- 50x1 เม็ดในตุ่ม PVC / PVDC / อะลูมิเนียม หรือแผลพุพองอะลูมิเนียมแบบใช้ครั้งเดียว ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่แสดงอาจไม่ทันสมัย
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
PLAVIX 75 MG เม็ดเคลือบฟิล์ม
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
เม็ดเคลือบฟิล์มแต่ละเม็ดประกอบด้วย clopidogrel 75 มก. (ในรูปของไฮโดรเจนซัลเฟต)
สารเพิ่มปริมาณที่ทราบผลกระทบ:
แต่ละเม็ดเคลือบฟิล์มประกอบด้วยแลคโตส 3 มก. และน้ำมันละหุ่งเติมไฮโดรเจน 3.3 มก.
สำหรับรายการสารปรุงแต่งทั้งหมด ดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
เม็ดเคลือบฟิล์ม
สีชมพู กลม สองนูน สลัก "75" ด้านหนึ่งและ "1171" อีกด้านหนึ่ง
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
ป้องกันเหตุการณ์ atherothrombotic
Clopidogrel ระบุไว้ใน:
• ผู้ป่วยผู้ใหญ่ที่มีกล้ามเนื้อหัวใจตาย (ตั้งแต่สองสามวันถึงน้อยกว่า 35 วัน), โรคหลอดเลือดสมองตีบ (จาก 7 วันถึงน้อยกว่า 6 เดือน) หรือโรคหลอดเลือดแดงส่วนปลายที่ได้รับการพิสูจน์แล้ว
• ผู้ป่วยผู้ใหญ่ที่เป็นโรคหลอดเลือดหัวใจเฉียบพลัน:
- โรคหลอดเลือดหัวใจเฉียบพลันที่ไม่มีส่วนสูงของส่วน ST (โรคหลอดเลือดหัวใจตีบที่ไม่เสถียรหรือกล้ามเนื้อหัวใจตายโดยไม่มีคลื่น Q) รวมถึงผู้ป่วยที่ได้รับการใส่ขดลวดหลังการแทรกแซงของหลอดเลือดหัวใจร่วมกับกรดอะซิติลซาลิไซลิก (ASA)
- โรคหลอดเลือดหัวใจเฉียบพลันที่มีความสูงของส่วน ST ร่วมกับ ASA ในผู้ป่วยที่ได้รับการรักษาด้วยยาที่เข้ารับการบำบัดด้วยลิ่มเลือด
การป้องกันการเกิด atherothrombotic และ thromboembolic events ใน atrial fibrillation
มีการระบุ Clopidogrel ร่วมกับ ASA ในการป้องกันเหตุการณ์ atherothrombotic และ thromboembolic รวมถึงโรคหลอดเลือดสมองในผู้ป่วยผู้ใหญ่ที่มีภาวะหัวใจห้องบนที่มีปัจจัยเสี่ยงอย่างน้อยหนึ่งปัจจัยสำหรับเหตุการณ์เกี่ยวกับหลอดเลือดไม่เหมาะสำหรับการรักษาด้วยตัวรับวิตามินเค (AVK) และผู้ที่มี ความเสี่ยงต่อการตกเลือดต่ำ
สำหรับข้อมูลเพิ่มเติม โปรดดูหัวข้อ 5.1
04.2 วิทยาและวิธีการบริหาร
ปริมาณ
• ผู้ใหญ่และประชากรผู้สูงอายุ
Clopidogrel ให้ครั้งเดียว 75 มก.
ในผู้ป่วยโรคหลอดเลือดหัวใจเฉียบพลัน:
- โรคหลอดเลือดหัวใจเฉียบพลันที่ไม่มีส่วนสูงของส่วน ST (โรคหลอดเลือดหัวใจตีบที่ไม่เสถียรหรือกล้ามเนื้อหัวใจตายโดยไม่มีคลื่น Q): การรักษาด้วย Clopidogrel ควรเริ่มต้นด้วยปริมาณการให้ยา 300 มก. เพียงครั้งเดียวแล้วให้ต่อเนื่องที่ 75 มก. วันละครั้ง (ร่วมกับกรดอะซิติลซาลิไซลิก (ASA) 75 มก. -325 มก. ต่อวัน) เนื่องจากปริมาณ ASA ที่สูงขึ้นมีความสัมพันธ์กับความเสี่ยงต่อการตกเลือดที่สูงขึ้น ขอแนะนำว่าขนาด ASA ไม่เกิน 100 มก. ยังไม่มีการกำหนดระยะเวลาการรักษาที่เหมาะสมอย่างเป็นทางการ ข้อมูลการทดลองทางคลินิกสนับสนุนการใช้งานสูงสุด 12 เดือนและเห็นผลสูงสุดที่ 3 เดือน (ดูหัวข้อ 5.1)
- ภาวะกล้ามเนื้อหัวใจตายเฉียบพลันแบบเฉียบพลันกลุ่ม ST: ควรให้ clopidogrel ครั้งเดียว 75 มก. ต่อวันโดยเริ่มด้วยขนาดยา 300 มก. ร่วมกับ ASA โดยมีหรือไม่มี thrombolytics ในผู้ป่วยที่มีอายุมากกว่า 75 ปี ควรให้ clopidogrel โดยไม่ต้องให้ยา การรักษาแบบผสมผสานควรเริ่มให้เร็วที่สุดเท่าที่จะเป็นไปได้หลังจากเริ่มมีอาการและดำเนินต่อไปอย่างน้อย 4 สัปดาห์ ยังไม่มีการศึกษาประโยชน์ของการรวม clopidogrel กับ ASA เกินสี่สัปดาห์ในการตั้งค่านี้ (ดูหัวข้อ 5.1)
ในผู้ป่วยที่มีภาวะ atrial fibrillation สามารถใช้ clopidogrel ได้ในขนาด 75 มก. ต่อวันเพียงครั้งเดียว การรักษาด้วย ASA (75-100 มก. ต่อวัน) ควรเริ่มต้นและต่อเนื่องร่วมกับ clopidogrel (ดูหัวข้อ 5.1)
หากไม่ได้รับยา:
- ภายใน 12 ชั่วโมงของการบริโภคที่กำหนด: ผู้ป่วยควรรับประทานยาทันทีและรับประทานยาต่อไปตามเวลาปกติ
- หากผ่านไปเกิน 12 ชั่วโมง: ผู้ป่วยควรรับประทานยาครั้งต่อไปตามเวลาปกติและไม่ควรรับประทานยาเพิ่มเป็นสองเท่า
• ประชากรเด็ก
ไม่ควรใช้ Clopidogrel ในเด็กเนื่องจากข้อกังวลด้านประสิทธิภาพ (ดูหัวข้อ 5.1)
• ไตล้มเหลว
ประสบการณ์การรักษาในผู้ป่วยที่มีภาวะไตไม่เพียงพอมีจำกัด (ดูหัวข้อ 4.4)
• ตับไม่เพียงพอ
ประสบการณ์การรักษาในผู้ป่วยที่มีความผิดปกติของตับในระดับปานกลางซึ่งอาจเป็นโรคเลือดออกในช่องท้องมีจำกัด (ดูหัวข้อ 4.4)
วิธีการบริหาร
การใช้ช่องปาก.
แท็บเล็ตสามารถรับประทานได้ทั้งที่มีหรือไม่มีอาหาร
04.3 ข้อห้าม
• ภูมิไวเกินต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในส่วนที่ 2 หรือส่วนที่ 6.1
• ภาวะตับวายอย่างรุนแรง
• มีเลือดออกทางพยาธิวิทยา เช่น ในที่ที่มีแผลในกระเพาะอาหารหรือเลือดออกในกะโหลกศีรษะ
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
เลือดออกและพยาธิสภาพทางโลหิตวิทยา
เนื่องจากความเสี่ยงต่อการตกเลือดและอาการไม่พึงประสงค์ทางโลหิตวิทยา ควรพิจารณาประสิทธิภาพของการตรวจนับเม็ดเลือดและ/หรือการทดสอบที่เหมาะสมอื่นๆ ทันที เมื่อใดก็ตามที่มีอาการทางคลินิกที่บ่งชี้ว่ามีเลือดออกในระหว่างการรักษา (ดูหัวข้อ 4.8) เช่นเดียวกับยาต้านเกล็ดเลือดอื่นๆ ควรใช้ clopidogrel ควรใช้ด้วยความระมัดระวังในผู้ป่วยที่มีความเสี่ยงต่อการเลือดออกเพิ่มขึ้นหลังการบาดเจ็บ การผ่าตัด หรือภาวะทางพยาธิวิทยาอื่นๆ และในผู้ป่วยที่ได้รับการรักษาด้วย ASA, heparin, glycoprotein inhibitors IIb / IIIa หรือยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (NSAIDs) รวมถึง COX -2 inhibitors หรือ selective serotonin reuptake inhibitors (SSRIs) ผู้ป่วยควรได้รับการติดตามอย่างใกล้ชิดหากมีอาการเลือดออกรวมถึงเลือดออกในสมองโดยเฉพาะในช่วงสองสามสัปดาห์แรกของการรักษาและ / หรือหลังการทำหัตถการทางหัวใจ การบุกรุกหรือการผ่าตัด ไม่แนะนำให้ใช้ร่วมกันของ clopidogrel และยาต้านการแข็งตัวของเลือดในช่องปาก เนื่องจากอาจทำให้เลือดออกรุนแรงขึ้น (ดูหัวข้อ 4.5)
หากผู้ป่วยต้องได้รับการผ่าตัดทางเลือกที่ไม่แนะนำให้ใช้ยาต้านเกล็ดเลือดชั่วคราว ควรงดการใช้ clopidogrel 7 วันก่อนการผ่าตัด ก่อนทำการผ่าตัดใดๆ และก่อนทำการผ่าตัดใหม่ ยา ผู้ป่วยควรแนะนำแพทย์และทันตแพทย์ว่า กำลังรับการรักษาด้วย clopidogrel Clopidogrel ช่วยยืดเวลาเลือดออกและควรใช้ด้วยความระมัดระวังในผู้ป่วยที่มีรอยโรคเลือดออกง่าย (โดยเฉพาะทางเดินอาหารและลูกตา)
ผู้ป่วยควรได้รับคำแนะนำว่าการใช้ clopidogrel (เพียงอย่างเดียวหรือร่วมกับ ASA) อาจทำให้เลือดออกนานขึ้น และควรแจ้งให้แพทย์ทราบหากมีเลือดออกผิดปกติ (การแปลเป็นภาษาท้องถิ่นหรือระยะเวลา) ที่อาจเกิดขึ้น
Thrombotic thrombocytopenic purpura (ปตท.)
thrombocytopenic purpura (TTP) มีรายงานน้อยมากหลังการใช้ clopidogrel บางครั้งหลังจากได้รับสัมผัสสั้น ๆ ภาวะนี้มีลักษณะเฉพาะคือ thrombocytopenia และ microangiopathic haemolytic anemia ที่เกี่ยวข้องกับหรือมีปัญหาทางระบบประสาท ความผิดปกติของไต หรือมีไข้
TTP เป็นภาวะที่อาจถึงตายได้ซึ่งต้องได้รับการรักษาโดยทันทีรวมทั้งพลาสม่าเฟอเรซิส
ได้รับฮีโมฟีเลีย
มีรายงานการเกิดฮีโมฟีเลียภายหลังการใช้ clopidogrel ในกรณีที่มีการกระตุ้น Partial Thromboplastin Time (aPTT) ที่แยกได้ออกไปโดยมีหรือไม่มีเลือดออกอย่างต่อเนื่อง ควรพิจารณา haemophilia ที่ได้รับ ผู้ป่วยที่มีการยืนยันการวินิจฉัยว่าเป็นโรคฮีโมฟีเลียที่ได้มาควรได้รับการจัดการและรักษาโดยผู้เชี่ยวชาญทางการแพทย์ การรักษาด้วย clopidogrel ควรยุติลง
โรคหลอดเลือดสมองตีบล่าสุด
เนื่องจากขาดข้อมูล จึงไม่แนะนำให้ใช้ clopidogrel ในช่วง 7 วันแรกหลังโรคหลอดเลือดสมองตีบเฉียบพลัน
ไซโตโครม P450 2C19 (CYP2C19)
เภสัชจลนศาสตร์: เมื่อใช้ clopidogrel ในปริมาณที่แนะนำในผู้ป่วยที่ได้รับสาร CYP2C19 ที่ไม่ดี การก่อตัวของสารออกฤทธิ์ของ clopidogrel จะลดลงและผลกระทบต่อการทำงานของเกล็ดเลือดมีน้อย มีการทดสอบเพื่อระบุยีน CYP2C19 ของผู้ป่วย
เนื่องจาก clopidogrel ถูกแปลงเป็นสารออกฤทธิ์โดย CYP2C19 การใช้ผลิตภัณฑ์ยาที่ยับยั้งการทำงานของเอนไซม์นี้จึงคาดว่าจะทำให้ระดับเภสัชวิทยาของสารออกฤทธิ์ของ clopidogrel ลดลง ความเกี่ยวข้องทางคลินิกของการโต้ตอบนี้ไม่แน่นอน เพื่อเป็นการป้องกันไว้ล่วงหน้า ไม่ควรใช้สารยับยั้ง CYP2C19 ระดับรุนแรงหรือปานกลางร่วมกัน (ดูหัวข้อ 4.5 สำหรับรายการของสารยับยั้ง CYP2C19 ดูหัวข้อที่ 5.2 ด้วย)
ปฏิกิริยาข้ามระหว่าง thienopyridines
ผู้ป่วยควรได้รับการประเมินประวัติทางคลินิกของการแพ้ยา thienopyridines (เช่น clopidogrel, ticlopidine, prasugrel) เนื่องจากมีรายงานการเกิดปฏิกิริยาข้ามระหว่าง thienopyridines (ดูหัวข้อ 4.8 "ผลที่ไม่พึงประสงค์") Thienopyridines สามารถทำให้เกิดอาการแพ้ในระดับปานกลางถึงรุนแรงเช่นผื่น, angioedema หรือปฏิกิริยาทางโลหิตวิทยาเช่น thrombocytopenia และ neutropenia ผู้ป่วยที่เคยแพ้และ / หรือปฏิกิริยาทางโลหิตวิทยากับ thienopyridine ตัวใดตัวหนึ่งอาจมีความเสี่ยงเพิ่มขึ้นที่จะเกิดปฏิกิริยาเดียวกันหรือ "ปฏิกิริยาอื่น" กับ thienopyridine อื่น แนะนำให้ติดตามสัญญาณของภาวะภูมิไวเกินในผู้ป่วยที่แพ้ยา thienopyridines
ไตล้มเหลว
ประสบการณ์การรักษากับ clopidogrel มีข้อ จำกัด ในผู้ป่วยที่มีภาวะไตไม่เพียงพอ ควรใช้ Clopidogrel ด้วยความระมัดระวังในผู้ป่วยเหล่านี้ (ดูหัวข้อ 4.2)
ตับไม่เพียงพอ
ประสบการณ์การรักษากับ clopidogrel มีข้อ จำกัด ในผู้ป่วยที่มีความผิดปกติของตับในระดับปานกลางที่อาจมีเลือดออก diathesis ควรใช้ clopidogrel ด้วยความระมัดระวังในผู้ป่วยเหล่านี้ (ดูหัวข้อ 4.2)
สารเพิ่มปริมาณ
Plavix มีแลคโตส ผู้ป่วยที่มีปัญหาทางพันธุกรรมที่หายากของการแพ้กาแลคโตส การขาด Lapp-lactase หรือการดูดซึมน้ำตาลกลูโคส - กาแลคโตส malabsorption ไม่ควรรับประทานยา
ยานี้มีน้ำมันละหุ่งเติมไฮโดรเจนซึ่งอาจทำให้ปวดท้องและท้องร่วง
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
สารกันเลือดแข็งในช่องปาก: ไม่แนะนำให้ใช้ร่วมกับ clopidogrel และ anticoagulants ในช่องปาก เนื่องจากอาจทำให้เลือดออกรุนแรงขึ้น (ดูหัวข้อ 4.4) แม้ว่าการให้ clopidogrel 75 มก. / วันจะไม่เปลี่ยนแปลงเภสัชจลนศาสตร์ของ S-warfarin หรือ International Normalized Ratio (INR) ในผู้ป่วยที่รักษาด้วย warfarin เป็นเวลานาน แต่การให้ clopidogrel และ warfarin ร่วมกันเพิ่มความเสี่ยงต่อการตกเลือด เนื่องจาก ผลอิสระต่อภาวะเลือดคั่ง
สารยับยั้งไกลโคโปรตีน IIb / IIIa: ควรใช้ Clopidogrel ด้วยความระมัดระวังในผู้ป่วยที่ได้รับ glycoprotein IIb / IIIa inhibitors ร่วมกัน (ดูหัวข้อ 4.4)
กรดอะซิทิลซาลิไซลิก (ASA) : ASA ไม่แก้ไขการยับยั้งการรวมตัวของเกล็ดเลือดที่เกิดจาก ADP โดยอาศัย clopidogrel อย่างไรก็ตาม clopidogrel กระตุ้นผลของ ASA ต่อการรวมตัวของเกล็ดเลือดที่เกิดจากคอลลาเจน อย่างไรก็ตาม การให้ ASA 500 มก. ร่วมกันวันละสองครั้งเป็นเวลาหนึ่งวันไม่ได้ทำให้เวลาเลือดออกที่เกิดจาก clopidogrel นานขึ้นอย่างมีนัยสำคัญ ปฏิกิริยาทางเภสัชพลศาสตร์เป็นไปได้ระหว่าง clopidogrel กับกรดอะซิติลซาลิไซลิก โดยมีความเสี่ยงต่อการตกเลือดมากขึ้น ดังนั้น ควรใช้ควบคู่กันด้วยความระมัดระวัง (ดูหัวข้อ 4.4) อย่างไรก็ตาม ให้ clopidogrel และ ASA ร่วมกันนานถึง 1 ปี (ดูหัวข้อ 5.1)
เฮปาริน: ในการศึกษาทางคลินิกที่ดำเนินการกับอาสาสมัครที่มีสุขภาพดี หลังจากได้รับ clopidogrel แล้ว ไม่จำเป็นต้องปรับเปลี่ยนขนาดยาเฮปาริน หรือผลของเฮปารินต่อการแข็งตัวของเลือดเปลี่ยนแปลงไป การใช้ยาเฮปารินร่วมกันไม่มีผลต่อการยับยั้งการรวมตัวของเกล็ดเลือดที่เกิดจาก clopidogrel ปฏิกิริยาทางเภสัชพลศาสตร์เป็นไปได้ระหว่าง clopidogrel และ heparin โดยมีความเสี่ยงที่จะมีเลือดออกมากขึ้น ดังนั้น ควรใช้ควบคู่กันด้วยความระมัดระวัง (ดูหัวข้อ 4.4)
ลิ่มเลือดอุดตัน: ความปลอดภัยของการใช้ยา clopidogrel, fibrin หรือ non-fibrin เฉพาะ thrombolytic และ heparins ร่วมกันได้รับการศึกษาในผู้ป่วยที่มีภาวะกล้ามเนื้อหัวใจตายเฉียบพลัน
อุบัติการณ์ของการมีเลือดออกที่มีนัยสำคัญทางคลินิกคล้ายกับที่สังเกตได้เมื่อใช้ยาละลายลิ่มเลือดและเฮปารินร่วมกับ ASA (ดูหัวข้อ 4.8)
ยากลุ่ม NSAIDs: ในการศึกษาทางคลินิกที่ดำเนินการในอาสาสมัครที่มีสุขภาพดี การใช้ clopidogrel และ naproxen ร่วมกันทำให้เลือดออกในทางเดินอาหารลึกลับเพิ่มขึ้น
อย่างไรก็ตาม เนื่องจากขาดการศึกษาปฏิสัมพันธ์กับยากลุ่ม NSAIDs อื่นๆ จึงยังไม่ชัดเจนว่ามีความเสี่ยงที่จะมีเลือดออกในทางเดินอาหารเพิ่มขึ้นด้วย NSAIDs ทั้งหมดหรือไม่ ดังนั้น ควรใช้ NSAIDs ร่วมกับ COX-2 inhibitors และ clopidogrel ด้วยความระมัดระวัง (ดูหัวข้อ 4.4)
Selective Serotonin Reuptake Inhibitors (SSRIs): เนื่องจาก SSRIs ส่งผลต่อการกระตุ้นเกล็ดเลือดและเพิ่มความเสี่ยงต่อการตกเลือด การให้ SSRIs ร่วมกับ clopidogrel จึงควรดำเนินการด้วยความระมัดระวัง
การรักษาควบคู่อื่นๆ:
เนื่องจาก clopidogrel ถูกแปลงเป็นสารออกฤทธิ์โดย CYP2C19 การใช้ผลิตภัณฑ์ยาที่ยับยั้งการทำงานของเอนไซม์นี้จึงคาดว่าจะทำให้ระดับเภสัชวิทยาของสารออกฤทธิ์ของ clopidogrel ลดลง ความเกี่ยวข้องทางคลินิกของการโต้ตอบนี้ไม่แน่นอน เพื่อเป็นการป้องกันไว้ล่วงหน้า ไม่ควรใช้สารยับยั้ง CYP2C19 ระดับรุนแรงหรือปานกลางร่วมกัน (ดูหัวข้อ 4.4 และ 5.2)
ยาที่ยับยั้ง CYP2C19 ได้แก่ omeprazole และ esomeprazole, fluvoxamine, fluoxetine, moclobemide, voriconazole, fluconazole, ticlopidine, ciprofloxacin, cimetidine, carbamazepine, oxicarbazepine และ chloramphenicol
สารยับยั้งโปรตอนปั๊ม (PPI)
การบริหาร omeprazole ครั้งเดียว 80 มก. / วันและ clopidogrel ร่วมกันและห่างกัน 12 ชั่วโมงลดการได้รับเมตาโบไลต์ที่ใช้งานอยู่ 45% (ขนาดบรรจุ) และ 40% (ขนาดยาบำรุงรักษา) การลดลงเกี่ยวข้องกับการลดลง ในการยับยั้งการรวมตัวของเกล็ดเลือด 39% (ปริมาณการโหลด) และ 21% (ปริมาณการบำรุง) ปฏิกิริยาที่คล้ายคลึงกัน
มีการรายงานข้อมูลที่ขัดแย้งกันเกี่ยวกับผลกระทบทางคลินิกของปฏิกิริยาทางเภสัชจลนศาสตร์ (PK) / เภสัชพลศาสตร์ (PD) ในแง่ของเหตุการณ์หัวใจและหลอดเลือดที่สำคัญในการศึกษาทางคลินิกและการสังเกต เพื่อเป็นการป้องกันไว้ก่อน ไม่ควรใช้ omeprazole และ esomeprazole ร่วมกัน (ดูหัวข้อ 4.4)
การได้รับสารเมตาบอไลต์ลดลงอย่างเห็นได้ชัดเมื่อใช้ pantoprazole และ lansoprazole
ความเข้มข้นในพลาสมาของสารออกฤทธิ์ลดลง 20% (ขนาดยาที่ใส่เข้าไป) และ 14% (ขนาดยาเพื่อการรักษา) ในระหว่างการรักษาร่วมกับ pantoprazole 80 มก. วันละครั้ง สิ่งนี้เกี่ยวข้องกับการลดลงในการยับยั้งการรวมตัวของเกล็ดเลือดเฉลี่ยที่ 15% และ 11% ตามลำดับ ผลลัพธ์เหล่านี้บ่งชี้ว่าสามารถใช้ clopidogrel ร่วมกับ pantoprazole
ไม่มีหลักฐานว่าผลิตภัณฑ์ยาอื่นๆ ที่ลดความเป็นกรดในกระเพาะอาหาร เช่น H2 blockers (ยกเว้น cimetidine ซึ่งเป็นตัวยับยั้ง CYP2C19) หรือยาลดกรดรบกวนการทำงานของเกล็ดเลือดของ clopidogrel
ยาอื่นๆ:
มีการศึกษาทางคลินิกอื่น ๆ อีกหลายอย่างร่วมกับ clopidogrel และการรักษาร่วมกันอื่น ๆ เพื่อตรวจสอบปฏิกิริยาทางเภสัชพลศาสตร์และเภสัชจลนศาสตร์ที่อาจเกิดขึ้น
ไม่พบปฏิกิริยาทางเภสัชพลศาสตร์ที่เกี่ยวข้องเมื่อให้ clopidogrel ร่วมกับ atenolol หรือ nifedipine เพียงอย่างเดียวหรือร่วมกัน นอกจากนี้ ฤทธิ์ทางเภสัชพลศาสตร์ของ clopidogrel ไม่ได้รับผลกระทบอย่างมีนัยสำคัญจากการใช้ phenobarbital หรือ estrogen ร่วมกัน
เภสัชจลนศาสตร์ของ digoxin และ theophylline ไม่ได้รับผลกระทบจากการใช้ยาร่วมกับ clopidogrel ยาลดกรดไม่ได้เปลี่ยนแปลงการดูดซึมของ clopidogrel
ข้อมูลจากการศึกษาของ CAPRIE ระบุว่าสามารถให้ phenytoin และ tolbutamide ซึ่งถูกเผาผลาญโดย CYP2C9 ได้อย่างปลอดภัยควบคู่ไปกับ clopidogrel
นอกเหนือจากข้อมูลที่อธิบายไว้ข้างต้นเกี่ยวกับปฏิกิริยาระหว่างยาเฉพาะแล้ว ยังไม่ได้มีการศึกษาปฏิสัมพันธ์กับยาโคลพิโดเกรลและยาบางชนิดที่มักใช้ให้กับผู้ป่วยโรคหลอดเลือดตีบ อย่างไรก็ตาม ผู้ป่วยที่เข้าร่วมในการทดลองทางคลินิกกับ clopidogrel ได้รับการรักษาร่วมกันหลายอย่าง เช่น ยาขับปัสสาวะ ยา beta blockers ยา ACE inhibitors แคลเซียมแชนเนลบล็อกเกอร์ ยาลดคอเลสเตอรอล ยาขยายหลอดเลือดหัวใจ ยาต้านเบาหวาน (รวมทั้งอินซูลิน) ยากันชัก และ glycoprotein IIb / IIIa antagonists ที่ไม่มี หลักฐานของปฏิกิริยาเชิงลบที่มีนัยสำคัญทางคลินิก
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์
เนื่องจากไม่มีข้อมูลทางคลินิกเกี่ยวกับการได้รับ clopidogrel ในระหว่างตั้งครรภ์ จึงไม่ควรใช้ clopidogrel ในระหว่างตั้งครรภ์เพื่อเป็นการป้องกันไว้ก่อน
การศึกษาในสัตว์ทดลองไม่ได้บ่งชี้ถึงผลร้ายโดยตรงหรือโดยอ้อมในส่วนที่เกี่ยวกับการตั้งครรภ์ พัฒนาการของตัวอ่อน/ทารกในครรภ์ การคลอด หรือพัฒนาการหลังคลอด (ดูหัวข้อ 5.3)
เวลาให้อาหาร
ไม่ทราบว่า clopidogrel ถูกขับออกมาในนมของมนุษย์หรือไม่ การศึกษาในสัตว์ทดลองแสดงให้เห็นว่า clopidogrel ถูกขับออกมาในนม เพื่อเป็นการป้องกันไว้ก่อน ไม่ควรให้นมลูกในระหว่างการรักษาด้วย Plavix
ภาวะเจริญพันธุ์
ในการศึกษาในสัตว์ทดลอง clopidogrel ไม่แสดงภาวะเจริญพันธุ์ที่บกพร่อง
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
Clopidogrel ไม่มีหรือมีอิทธิพลเล็กน้อยต่อความสามารถในการขับหรือใช้เครื่องจักร
04.8 ผลกระทบที่ไม่พึงประสงค์
สรุปข้อมูลความปลอดภัย
Clopidogrel ได้รับการประเมินเพื่อความปลอดภัยในผู้ป่วยมากกว่า 44,000 รายที่เข้าร่วมในการทดลองทางคลินิก รวมถึงกว่า 12,000 รายที่ได้รับการรักษาเป็นเวลา 1 ปีหรือมากกว่า ในการศึกษาของ CAPRIE พบว่า clopidogrel ในขนาด 75 มก. / วัน โดยรวมแล้วเทียบได้กับ ASA 325 มก. / วันโดยไม่คำนึงถึงอายุ เพศ และเชื้อชาติของผู้ป่วย อาการไม่พึงประสงค์ที่เกี่ยวข้องทางคลินิกที่พบใน CAPRIE, CURE, CLARITY การศึกษา , COMMIT และ ACTIVE-A จะกล่าวถึงด้านล่าง
นอกจากประสบการณ์ในการทดลองทางคลินิกแล้ว ยังมีรายงานอาการข้างเคียงที่เกิดขึ้นเองอีกด้วย
เลือดออกเป็นปฏิกิริยาที่รายงานบ่อยที่สุดในการทดลองทางคลินิกและประสบการณ์หลังการขาย โดยส่วนใหญ่รายงานในช่วงเดือนแรกของการรักษา
ในการศึกษา CAPRIE ในผู้ป่วยที่ได้รับ clopidogrel และ ASA อุบัติการณ์โดยรวมของรูปแบบเลือดออกใด ๆ เท่ากับ 9.3% อุบัติการณ์ของกรณีที่รุนแรงมีความคล้ายคลึงกันสำหรับ clopidogrel และ ASA
ในการศึกษา CURE พบว่าไม่มีเลือดออกมากเกินด้วย clopidogrel บวก ASA ใน 7 วันหลังจากการปลูกถ่ายหลอดเลือดหัวใจในผู้ป่วยที่หยุดการรักษานานกว่า 5 วันก่อนการผ่าตัด ใน 5 วันก่อนการผ่าตัดบายพาส อุบัติการณ์คือ 9.6% สำหรับ clopidogrel บวก ASA และ 6.3% สำหรับยาหลอกบวก ASA
ในการศึกษา CLARITY มีเลือดออกโดยรวมเพิ่มขึ้นในกลุ่ม clopidogrel บวก ASA เมื่อเทียบกับกลุ่มยาหลอกร่วมกับ ASA อุบัติการณ์ของการตกเลือดครั้งใหญ่มีความคล้ายคลึงกันในทุกกลุ่มผลลัพธ์นี้สอดคล้องกันในกลุ่มย่อยของผู้ป่วยที่กำหนดโดยลักษณะพื้นฐานและตามประเภทของการบำบัดด้วยการละลายลิ่มเลือดหรือการรักษาด้วยเฮปาริน
ในการศึกษา COMMIT อัตราโดยรวมของการตกเลือดที่สำคัญที่ไม่ใช่สมองหรือมีเลือดออกในสมองมีค่าต่ำและใกล้เคียงกันในทั้งสองกลุ่ม
ในการศึกษา ACTIVE-A อัตราโดยรวมของการตกเลือดที่สำคัญในกลุ่ม clopidogrel + ASA สูงกว่าในกลุ่มยาหลอก + ASA (6.7% เทียบกับ 4.3%) เลือดออกที่สำคัญส่วนใหญ่มาจากภายนอกกะโหลกศีรษะในทั้งสองกลุ่ม (5.3% ในกลุ่ม clopidogrel + ASA; 3.5% ในกลุ่มยาหลอก + ASA) ส่วนใหญ่เกิดขึ้นในทางเดินอาหาร (3.5% เทียบกับ 1.8%) พบเลือดออกในกะโหลกศีรษะมากเกินไปในกลุ่ม clopidogrel + ASA เทียบกับกลุ่มยาหลอก + ASA (1.4% เทียบกับ 0.8% ตามลำดับ) ไม่มีความแตกต่างอย่างมีนัยสำคัญทางสถิติระหว่างกลุ่มในอัตราการเลือดออกร้ายแรง (1.1% ในกลุ่ม clopidogrel + ASA และ 0.7% ในกลุ่มยาหลอก + ASA) และโรคหลอดเลือดสมองตีบ (0.8% และ 0.6% ตามลำดับ)
ตารางอาการไม่พึงประสงค์
อาการไม่พึงประสงค์ที่พบในการศึกษาทางคลินิกหรือที่รายงานโดยธรรมชาติแสดงไว้ในตารางด้านล่าง ความถี่ถูกกำหนดโดยใช้อนุสัญญาต่อไปนี้: ทั่วไป (≥1 / 100,
* ข้อมูลเกี่ยวกับ clopidogrel ที่มีความถี่ "ไม่ทราบ"
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญ ซึ่งช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านระบบการรายงานระดับประเทศ "ภาคผนวก 5 .
04.9 ใช้ยาเกินขนาด
การใช้ยาเกินขนาดของ clopidogrel อาจทำให้เลือดออกเป็นเวลานานและทำให้เกิดภาวะแทรกซ้อนเลือดออกได้ หากพบว่ามีเลือดออกควรพิจารณาการรักษาที่เหมาะสม
ไม่มียาแก้พิษที่เป็นที่รู้จักสำหรับกิจกรรมทางเภสัชวิทยาของ clopidogrel เมื่อจำเป็นต้องมีการแก้ไขอย่างรวดเร็วของการมีเลือดออกเป็นเวลานานการถ่ายเกล็ดเลือดอาจย้อนกลับผลของ clopidogrel
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มยารักษาโรค: ยาต้านเกล็ดเลือด ยกเว้นเฮปาริน
รหัส ATC: B01AC / 04.
กลไกการออกฤทธิ์
Clopidogrel เป็น prodrug หนึ่งใน metabolites ของมันคือตัวยับยั้งการรวมตัวของเกล็ดเลือด
Clopidogrel ต้องถูกเผาผลาญโดยเอนไซม์ CYP450 เพื่อผลิตสารออกฤทธิ์ที่ยับยั้งการรวมตัวของเกล็ดเลือด
เมแทบอไลต์ที่ใช้งานของ clopidogrel คัดเลือกยับยั้งการจับตัวของอะดีโนซีนไดฟอสเฟต (ADP) กับตัวรับ P2Y12 ของเกล็ดเลือด และส่งผลให้ยับยั้งการกระตุ้น ADP ที่เป็นสื่อกลางของ GPIIb-IIIa glycoprotein complex ดังนั้นจึงยับยั้งการรวมตัวของเกล็ดเลือด
เนื่องจากการผูกมัดที่ไม่สามารถย้อนกลับได้ เกล็ดเลือดที่สัมผัสกับ clopidogrel จะได้รับผลกระทบไปตลอดชีวิต (ประมาณ 7-10 วัน) และการฟื้นตัวของการทำงานของเกล็ดเลือดปกติจะเกิดขึ้นโดยขึ้นอยู่กับการหมุนเวียนของเกล็ดเลือด การรวมตัวของเกล็ดเลือดที่เกิดจากตัวเร่งปฏิกิริยาอื่นที่ไม่ใช่ ADP ยังถูกยับยั้งโดยการขัดขวางการขยายของการกระตุ้นเกล็ดเลือดเนื่องจาก ADP ที่ปล่อยออกมา
เนื่องจากสารออกฤทธิ์ถูกผลิตขึ้นโดยกิจกรรมของเอ็นไซม์ CYP450 ซึ่งบางชนิดมีลักษณะหลายรูปแบบหรืออาจมีการยับยั้งโดยผลิตภัณฑ์ยาอื่น ๆ ผู้ป่วยบางรายจึงไม่สามารถยับยั้งเกล็ดเลือดได้อย่างเพียงพอ
คุณสมบัติทางเภสัชพลศาสตร์
ขนาดยาซ้ำ 75 มก. ต่อวันทำให้เกิดการยับยั้งการรวมตัวของเกล็ดเลือดที่เกิดจาก ADP อย่างเห็นได้ชัดตั้งแต่วันแรก การยับยั้งเพิ่มขึ้นเรื่อย ๆ เพื่อให้คงตัวระหว่างวันที่สามถึงเจ็ด ในสภาวะคงตัวนี้ ระดับการยับยั้งเฉลี่ยที่สังเกตพบในขนาด 75 มก. ต่อวันอยู่ในช่วง 40-60% การรวมตัวของเกล็ดเลือดและเวลาที่มีเลือดออกจะค่อยๆ กลับสู่การตรวจวัดพื้นฐาน โดยปกติภายใน 5 วันหลังจากหยุดการรักษา
ประสิทธิภาพและความปลอดภัยทางคลินิก
ความปลอดภัยและประสิทธิภาพของ clopidogrel ได้รับการประเมินใน 5 การศึกษาแบบ double-blind ที่เกี่ยวข้องกับผู้ป่วยมากกว่า 88, 000 ราย: การศึกษา CAPRIE เปรียบเทียบ clopidogrel และ ASA และการศึกษา CURE, CLARITY, COMMIT และ ACTIVE-A ระหว่าง clopidogrel กับยาหลอก ทั้งสองได้รับ ร่วมกับ ASA และการรักษามาตรฐานอื่นๆ
กล้ามเนื้อหัวใจตายเฉียบพลัน (MI) โรคหลอดเลือดสมองล่าสุดหรือโรคหลอดเลือดแดงส่วนปลายที่ได้รับการบันทึกไว้
การศึกษาของ CAPRIE เกี่ยวข้องกับผู้ป่วย 19,185 คนที่มีภาวะไขมันในหลอดเลือดที่แสดงออกโดยกล้ามเนื้อหัวใจตายเมื่อเร็ว ๆ นี้ (
Clopidogrel ลดอุบัติการณ์ของเหตุการณ์ขาดเลือดใหม่อย่างมีนัยสำคัญ (รวม "จุดสิ้นสุด" ของกล้ามเนื้อหัวใจตาย, โรคหลอดเลือดสมองตีบและการเสียชีวิตของหลอดเลือด) เมื่อเทียบกับ ASA ในความตั้งใจที่จะรักษาการวิเคราะห์ พบ 939 เหตุการณ์ในกลุ่ม clopidogrel และ 1,020 เหตุการณ์กับ ASA (ลดความเสี่ยงสัมพัทธ์ (RRR) 8.7%, [95% CI: 0.2 ถึง 16.4]; p = 0.045) ซึ่งสอดคล้องกับผู้ป่วยทุกๆ 1,000 คนที่ได้รับการรักษาเป็นเวลา 2 ปีถึง 10 รายเพิ่มเติม [CI: 0 ถึง 20] ซึ่งเป็น ป้องกันจากเหตุการณ์ขาดเลือดใหม่ การวิเคราะห์การตายโดยรวมเป็นจุดยุติทุติยภูมิไม่พบความแตกต่างที่มีนัยสำคัญระหว่าง clopidogrel (5.8%) และ ASA (6.0%)
ใน "การวิเคราะห์กลุ่มย่อยที่ดำเนินการสำหรับพยาธิสภาพที่มีคุณสมบัติ (กล้ามเนื้อหัวใจตาย โรคหลอดเลือดสมองตีบและโรคหลอดเลือดแดงส่วนปลาย) ประโยชน์ดูเหมือนจะสอดคล้องกันมากขึ้น (ถึงนัยสำคัญทางสถิติที่ p = 0.003) ในผู้ป่วยที่ลงทะเบียนสำหรับโรคหลอดเลือดแดงส่วนปลาย (โดยเฉพาะอย่างยิ่งสำหรับผู้ที่มีประวัติ กล้ามเนื้อหัวใจตาย) (RRR = 23.7%; CI: 8.9 ถึง 36.2) และความสอดคล้องน้อยกว่า (ไม่แตกต่างอย่างมีนัยสำคัญจาก ASA) ในผู้ป่วยโรคหลอดเลือดสมอง (RRR = 7.3%; CI: จาก - 5.7 ถึง 18.7 [p = 0.258]) ในผู้ป่วย ลงทะเบียนในการศึกษาบนพื้นฐานของกล้ามเนื้อหัวใจตายเพียงอย่างเดียวเมื่อเร็ว ๆ นี้ clopidogrel เป็นตัวเลขที่ต่ำกว่า แต่ไม่แตกต่างทางสถิติจาก ASA (RRR = - 4.0%; CI : - 22.5 ถึง 11.7 [p = 0.639]) นอกจากนี้ การวิเคราะห์กลุ่มย่อย ตามอายุแสดงให้เห็นว่าประโยชน์ของ clopidogrel ในผู้ป่วยที่มีอายุมากกว่า 75 ปีนั้นน้อยกว่าที่พบในผู้ป่วยที่อายุ ≤75 ปี
เนื่องจากการศึกษาของ CAPRIE ไม่ได้ออกแบบมาเพื่อประเมินประสิทธิภาพในแต่ละกลุ่มย่อย จึงไม่ชัดเจนว่าความแตกต่างในการลดความเสี่ยงที่เกี่ยวข้องสำหรับเงื่อนไขที่มีคุณสมบัติตามเกณฑ์ต่างๆ นั้นมีอยู่จริงหรือเนื่องมาจากโอกาส
โรคหลอดเลือดหัวใจเฉียบพลัน
การศึกษา CURE ดำเนินการในผู้ป่วย 12,562 รายที่เป็นโรคหลอดเลือดหัวใจเฉียบพลันโดยไม่มีการยกระดับส่วน ST (โรคหลอดเลือดหัวใจตีบที่ไม่เสถียรหรือกล้ามเนื้อหัวใจตายโดยไม่มีคลื่น Q) ซึ่งมีอาการเจ็บหน้าอกตอนล่าสุดหรือมีอาการที่สอดคล้องกับภาวะขาดเลือดใน 24 ชั่วโมง ชั่วโมง ผู้ป่วยต้องมีการเปลี่ยนแปลง ECG อย่างใดอย่างหนึ่งที่สอดคล้องกับ ischemia ใหม่หรือความสูงของเอนไซม์หัวใจหรือ troponin I หรือ T อย่างน้อย 2 เท่าของ ULN ผู้ป่วยได้รับการสุ่มให้รับการรักษาด้วย clopidogrel (ขนาดยา 300 มก. ตาม 75 มก. / วัน N = 6259) หรือยาหลอก (N = 6303) ทั้งสองให้ร่วมกับ ASA (75-325 มก. วันละครั้ง) และการรักษามาตรฐานอื่น ๆ ผู้ป่วยได้รับการรักษานานถึงหนึ่งปี ในการศึกษา CURE ผู้ป่วย 823 คน (6.6%) ได้รับร่วมกัน การรักษาด้วย GPIIb / IIIa receptor antagonists เฮปารินได้รับยาในผู้ป่วยมากกว่า 90% และร้อยละสัมพัทธ์ของ การห้ำหั่นระหว่าง clopidogrel กับยาหลอกไม่ได้รับผลกระทบอย่างมีนัยสำคัญจากการรักษาด้วยเฮปารินร่วมกัน
จำนวนผู้ป่วยที่ประสบกับจุดยุติปฐมภูมิ (การเสียชีวิตจากโรคหัวใจและหลอดเลือด กล้ามเนื้อหัวใจตาย หรือโรคหลอดเลือดสมอง) เท่ากับ 582 (9.3%) ในกลุ่ม clopidogrel และ 719 (11.4%) ในกลุ่มยาหลอก โดยลดความเสี่ยงสัมพัทธ์ 20% (95%) CI 10% ถึง 28%; p = 0.00009) สำหรับกลุ่ม clopidogrel (ลดความเสี่ยงสัมพัทธ์ 17% เมื่อผู้ป่วยได้รับการรักษาอย่างระมัดระวัง, 29% เมื่อเข้ารับการผ่าตัดหลอดเลือดหัวใจตีบ transluminal (PTCA) โดยมีหรือไม่มี stent และ 10% เมื่อได้รับการบายพาสหลอดเลือดหัวใจ กราฟต์ (CABG) การเกิดโรคหัวใจและหลอดเลือดใหม่ (primary endpoint) สามารถลดความเสี่ยงได้ 22% (CI: 8.6 ถึง 33.4), 32% (CI: 12.8 ถึง 46.4), 4% (CI: -26.9 ถึง 26.7), 6% (CI: -33.5 ถึง 34.3) และ 14% (CI: -31.6 ถึง 44.2) ระหว่างช่วงการศึกษา 0-1, 1-3, 3-6, 6-9 และ 9- 12 เดือนตามลำดับ ดังนั้น นอกเหนือจากการรักษา 3 เดือน os การให้ยาในกลุ่ม clopidogrel + ASA ไม่ได้เพิ่มขึ้นอีกในขณะที่ความเสี่ยงของการตกเลือดยังคงมีอยู่ (ดูหัวข้อ 4.4)
การใช้ clopidogrel ใน CURE มีความเกี่ยวข้องกับการลดความจำเป็นในการรักษา thrombolytic (RRR = 43.3%; CI: 24.3% ถึง 57.5%) และ GPIIb / IIIa inhibitors (RRR = 18, 2%; CI: 6.5%, 28.3) %)
จำนวนผู้ป่วยที่เป็นโรค co-primary endpoint (การเสียชีวิตของหัวใจและหลอดเลือด กล้ามเนื้อหัวใจตาย โรคหลอดเลือดสมองหรือภาวะหัวใจขาดเลือดที่ดื้อต่อการรักษา) คือ 1,035 (16.5%) ในกลุ่ม clopidogrel และ 1,187 (18.8%) ในกลุ่มยาหลอก โดยมีความเสี่ยงลดลง 14 % (95% CI 6% ถึง 21%, p = 0.0005) สำหรับกลุ่ม clopidogrelประโยชน์นี้ได้รับแรงหนุนหลักจากการลดลงอย่างมีนัยสำคัญทางสถิติในอุบัติการณ์ของกล้ามเนื้อหัวใจตาย [287 (4.6%) ในกลุ่ม clopidogrel และ 363 (5.8%) ในกลุ่มยาหลอก] ไม่มีผลต่ออัตราการเข้ารับการรักษาในโรงพยาบาลซ้ำสำหรับโรคหลอดเลือดหัวใจตีบที่ไม่เสถียร
ผลลัพธ์ที่ได้จากประชากรที่มีลักษณะแตกต่างกัน (เช่น โรคหลอดเลือดหัวใจตีบไม่คงที่หรือกล้ามเนื้อหัวใจตายโดยไม่มีคลื่น Q ระดับความเสี่ยงต่ำหรือสูง โรคเบาหวาน ความจำเป็นในการปรับหลอดเลือดใหม่ อายุ เพศ ฯลฯ) พบว่าสอดคล้องกับผลลัพธ์ของ "ประถมศึกษา" การวิเคราะห์ โดยเฉพาะอย่างยิ่ง ในการวิเคราะห์แบบ post-hoc ในผู้ป่วย 2,172 ราย (17% ของประชากรทั้งหมดของการศึกษา CURE) ที่ได้รับการจัดวางขดลวด (Stent-CURE) ข้อมูลแสดงให้เห็น RRR ที่มีนัยสำคัญที่ 26.2% สำหรับ clopidogrel มากกว่ายาหลอกสำหรับจุดสิ้นสุดร่วมหลัก (การเสียชีวิตของหัวใจและหลอดเลือด กล้ามเนื้อหัวใจตาย โรคหลอดเลือดสมอง) และ RRR ที่สำคัญที่ 23.9% สำหรับจุดสิ้นสุดร่วมหลักที่สอง (การเสียชีวิตของหัวใจและหลอดเลือด กล้ามเนื้อหัวใจตาย โรคหลอดเลือดสมอง หรือขาดเลือดขาดเลือด นอกจากนี้ ข้อมูลด้านความปลอดภัยของ clopidogrel ในเรื่องนี้ กลุ่มย่อยของผู้ป่วยไม่ได้เปิดเผยปัญหาใด ๆ เป็นพิเศษ ดังนั้น ผลลัพธ์ที่ได้จากกลุ่มย่อยนี้จึงสอดคล้องกับผลลัพธ์โดยรวม ssivi ของการศึกษา
ประโยชน์ที่สังเกตได้จาก clopidogrel นั้นไม่ขึ้นกับการใช้การรักษาโรคหัวใจและหลอดเลือดแบบเฉียบพลันและระยะยาวอื่นๆ (เช่น heparin / LMWH, glycoprotein IIb / IIIa antagonists, ยาลดไขมัน, beta blockers และ ACE inhibitors) ประสิทธิภาพของ clopidogrel คือ โดยไม่ขึ้นกับขนาดยา ASA (75-325 มก. วันละครั้ง)
ในผู้ป่วยที่มีระดับ MI สูงของกลุ่ม ST เฉียบพลัน ความปลอดภัยและประสิทธิภาพของ clopidogrel ได้รับการประเมินในการศึกษาแบบสุ่มตัวอย่างแบบ double-blind และ placebo-controlled 2 เรื่อง CLARITY และ COMMIT
การศึกษา CLARITY ลงทะเบียนผู้ป่วย 3,491 รายที่นำเสนอภายใน 12 ชั่วโมงหลังจากเริ่มมีอาการของระดับ MI ของ ST-segment และเป็นผู้เข้ารับการบำบัดด้วยลิ่มเลือด ผู้ป่วยได้รับ clopidogrel (ขนาดบรรจุ 300 มก. ตามด้วย 75 มก. / วัน) , n = 1752) หรือ ยาหลอก (n = 1739) ร่วมกับ ASA (ขนาดบรรจุ 150 ถึง 325 มก. ตามด้วย 75-162 มก. / วัน) ยาละลายลิ่มเลือด และหากจำเป็น ให้สังเกตเฮปารินเป็นเวลา 30 วัน จุดสิ้นสุดหลักคือ การเกิดขึ้นของเหตุการณ์ใดเหตุการณ์หนึ่งต่อไปนี้: การอุดตันของหลอดเลือดแดงที่เกี่ยวข้องกับ infarct พบได้ที่การตรวจหลอดเลือดหัวใจตีบก่อนถ่ายออก หรือเสียชีวิต หรือการกลับเป็นซ้ำของ MI ก่อนการตรวจหลอดเลือดหัวใจ สำหรับผู้ป่วยที่ไม่ได้รับการตรวจหลอดเลือดหัวใจ จุดสิ้นสุดหลักคือการเสียชีวิตหรือการกลับเป็นซ้ำของ MI ในวันที่ 8 หรือโดยการออกจากโรงพยาบาล ประชากรผู้ป่วยรวมผู้หญิง 19.7% และผู้ป่วย 29.2% นิติบุคคลที่มีอายุมากกว่า 65 ปี โดยรวม 99.7% ของผู้ป่วยได้รับยาละลายลิ่มเลือด (ไฟบรินเฉพาะ: 68.7%, ไฟบรินที่ไม่เฉพาะเจาะจง: 31.1%), เฮปาริน 89.5%, ตัวบล็อคเบต้า 78.7%, สารยับยั้ง ACE 54.7% และสแตติน 63%
อุบัติการณ์ของจุดยุติปฐมภูมิอยู่ที่ 15 เปอร์เซ็นต์ (15.0%) ในผู้ป่วยในกลุ่ม clopidogrel และ 21.7% ในผู้ป่วยในกลุ่มยาหลอก โดยลดลงแน่นอน 6.7% และลดความเสี่ยง 36% ในการให้ clopidogrel (95%) CI: 24, 47%; ฝ่ายที่เกี่ยวข้องกับอาการหัวใจวาย ประโยชน์นี้สอดคล้องกันในกลุ่มย่อยที่กำหนดไว้ล่วงหน้าทั้งหมด รวมทั้งอายุและเพศ ตำแหน่งของอาการหัวใจวาย และประเภทของกลุ่มย่อยละลายลิ่มเลือด หรือเฮปารินที่ใช้
การศึกษา COMMIT ด้วยการออกแบบแฟคทอเรียล 2x2 ลงทะเบียนผู้ป่วย 45,852 รายที่แสดงอาการสงสัยของ MI ภายใน 24 ชั่วโมง โดยสนับสนุนความผิดปกติของคลื่นไฟฟ้าหัวใจ (เช่น ความสูงของส่วน ST ความสูงของส่วน ST หรือการอุดตันของสาขาด้านซ้าย) ผู้ป่วยได้รับ clopidogrel (75 มก. / วัน n = 22.961) หรือยาหลอก (n = 22.891) ร่วมกับ ASA (162 มก. / วัน) เป็นเวลา 28 วันหรือจนกว่าจะออกจากโรงพยาบาล Co-primary endpoints เสียชีวิตจากสาเหตุใด ๆ และ การเกิดขึ้นครั้งแรกของอาการหัวใจวายซ้ำ โรคหลอดเลือดสมอง หรือเสียชีวิต ประชากรรวมผู้หญิง 27.8% ผู้ป่วย 58.4% อายุ≥ 60 ปี (26% ≥ 70 ปี) และ 54.5% ของผู้ป่วยได้รับยาละลายลิ่มเลือด
Clopidogrel ลดความเสี่ยงของการเสียชีวิตจากสาเหตุใด ๆ อย่างมีนัยสำคัญ 7% (p = 0.029) และความเสี่ยงสัมพัทธ์ของการเกิดภาวะหัวใจวายซ้ำ โรคหลอดเลือดสมองหรือการเสียชีวิต 9% (p = 0.002) โดยลดลงอย่างสมบูรณ์ 0.5 % และ 0.9% ตามลำดับ ประโยชน์นี้สอดคล้องกับอายุ เพศ และการใช้ หรืออื่นๆ ของยาละลายลิ่มเลือด และเห็นได้ตั้งแต่ 24 ชั่วโมงแรก
ภาวะหัวใจห้องบนสั่นพลิ้ว
การศึกษา ACTIVE-W และ ACTIVE-A ซึ่งเป็นการศึกษาแยกกันภายในโปรแกรม ACTIVE รวมถึงผู้ป่วยที่มีภาวะหัวใจห้องบน (AF) ที่มีปัจจัยเสี่ยงอย่างน้อยหนึ่งปัจจัยสำหรับเหตุการณ์เกี่ยวกับหลอดเลือด ตามเกณฑ์การลงทะเบียน แพทย์ได้รวมผู้ป่วยไว้ในการศึกษา ACTIVE-W หากพวกเขามีสิทธิ์รับการรักษาด้วยวิตามินเค antagonists (AVKs) (เช่น warfarin) การศึกษา ACTIVE-A รวมผู้ป่วยที่ไม่สามารถได้รับการรักษา AVK เนื่องจากไม่สามารถหรือไม่เต็มใจที่จะรับการรักษา
การศึกษา ACTIVE-W แสดงให้เห็นว่าการรักษาด้วยยาต้านการแข็งตัวของเลือดด้วยคู่อริวิตามินเคมีประสิทธิภาพมากกว่าการรักษาด้วย clopidogrel และ ASA
ACTIVE-A (n = 7,554) เป็นการศึกษาแบบ multicenter, randomized, double-blind, placebo-controlled เปรียบเทียบ clopidogrel 75 มก. / วัน + ASA (N = 3,772) กับยาหลอก + ASA (N = 3,782) ปริมาณที่แนะนำของ ASA อยู่ระหว่าง 75 ถึง 100 มก. / วัน ผู้ป่วยได้รับการรักษานานถึง 5 ปี
ผู้ป่วยที่สุ่มเข้าร่วมโปรแกรม ACTIVE จำเป็นต้องมีเอกสาร AF เช่น AF ถาวรหรือ AF ไม่สม่ำเสมออย่างน้อย 2 ตอนที่เกิดขึ้นในช่วง 6 เดือนที่ผ่านมาและต้องมีปัจจัยเสี่ยงอย่างน้อยหนึ่งอย่างต่อไปนี้:
• อายุ ≥ 75 ปี หรือ
• อายุระหว่าง 55 ถึง 74 ปี e
- เบาหวานที่ต้องใช้ยา o
- เอกสาร MI ก่อนหน้าหรือโรคหลอดเลือดหัวใจที่บันทึกไว้;
• กำลังรับการรักษาสำหรับความดันโลหิตสูงอย่างเป็นระบบ
• จังหวะก่อนหน้า, การโจมตีขาดเลือดชั่วคราว (TIA) หรือเส้นเลือดอุดตันที่ระบบที่ไม่ใช่ CNS;
• หัวใจห้องล่างซ้ายทำงานผิดปกติ โดยมีหัวใจห้องล่างซ้ายทำงานผิดปกติ
• เอกสารเกี่ยวกับโรคหลอดเลือดแดงอุดตันส่วนปลาย
คะแนนเฉลี่ย CHADS2 คือ 2.0 (ช่วง 0-6)
เกณฑ์การยกเว้นหลักสำหรับผู้ป่วยประกอบด้วยแผลในกระเพาะอาหารที่บันทึกไว้ในช่วง 6 เดือนที่ผ่านมา การตกเลือดในสมองก่อนหน้า; ภาวะเกล็ดเลือดต่ำที่สำคัญ (จำนวนเกล็ดเลือด
ผู้ป่วยเจ็ดสิบสาม (73%) ที่ลงทะเบียนในการศึกษา ACTIVE-A ไม่มีสิทธิ์รับ AVK หลังการประเมินทางการแพทย์ ไม่สามารถปฏิบัติตามการตรวจสอบ INR (International Normalized Ratio) แนวโน้มที่จะล้มหรือได้รับบาดเจ็บที่ศีรษะ หรือมีเลือดออกเฉพาะ ความเสี่ยง สำหรับผู้ป่วย 26% การตัดสินใจของแพทย์ขึ้นอยู่กับความไม่เต็มใจของผู้ป่วยที่จะใช้ VKA
41.8% ของประชากรที่ศึกษาเป็นผู้หญิง อายุเฉลี่ย 71 ปี 41.6% ของผู้ป่วยมีอายุ ≥75 ปี โดยรวมแล้ว 23% ของผู้ป่วยได้รับการรักษาด้วย antiarrhythmics, 52.1% ด้วย beta blockers, 54.6% ด้วย ACE inhibitors และ 25% ด้วย statin
จำนวนผู้ป่วยที่มาถึงจุดสิ้นสุดหลัก (เวลาถึงจังหวะแรก, MI, เส้นเลือดอุดตันที่ระบบที่ไม่ใช่ CNS หรือการเสียชีวิตของหลอดเลือด) เป็นผู้ป่วย 832 ราย (22.1%) ในกลุ่ม clopidogrel + ASA และผู้ป่วย 924 ราย (24.4%) ในกลุ่มยาหลอก + ASA กลุ่ม (ลดความเสี่ยงสัมพัทธ์ 11.1%; 95% CI 2.4% -19.1%; p = 0.013) สาเหตุหลักมาจากโรคหลอดเลือดสมองตีบขนาดใหญ่ที่เกิดขึ้นในผู้ป่วย 296 ราย (7.8%) ที่ได้รับการรักษาด้วย clopidogrel + ASA และ 408 ราย (10.8%) รักษาด้วยยาหลอก + ASA (ลดความเสี่ยงสัมพันธ์ 28.4%; 95% CI, 16.8% -38.3%; p = 0.00001)
ประชากรเด็ก
ในการศึกษาขนาดยาที่เพิ่มขึ้นของทารกแรกเกิดหรือทารกอายุไม่เกิน 24 เดือนจำนวน 86 รายที่มีความเสี่ยงต่อการเกิดลิ่มเลือดอุดตัน (PICOLO) ให้ประเมิน clopidogrel ในขนาด 0.01, 0.1 และ 0.2 มก. / กก. ในทารกแรกเกิด และในทารกและ 0.15 มก. / กก. ในทารกแรกเกิดเท่านั้น ปริมาณ 0.2 มก. / กก. มีการยับยั้งเปอร์เซ็นต์เฉลี่ย 49.3% (การรวมตัวของเกล็ดเลือดที่เกิดจาก ADP 5mcM) เทียบได้กับผู้ใหญ่ที่รับประทาน Plavix 75 มก. / วัน ในการศึกษาแบบสุ่ม double-blind กลุ่มคู่ขนาน (CLARINET ) ผู้ป่วยเด็ก 906 คน (ทารกแรกเกิดและทารก) ที่เป็นโรคหัวใจพิการแต่กำเนิดชนิดเขียวอ่อนและมีการแบ่งหลอดเลือดแดงในปอดอย่างเป็นระบบ ได้รับการสุ่มให้ได้รับ clopidogrel 0.2 มก. / กก. (n = 467) หรือยาหลอก (n = 439) ที่มีการรักษาพื้นหลังร่วมกันจนถึงเวลา ของการผ่าตัดระยะที่ 2 ระยะเวลาเฉลี่ยตั้งแต่การปลูกถ่าย palliative shunt ไปจนถึงการให้ยาในการศึกษาครั้งแรกคือ 20 วัน ผู้ป่วยประมาณ 88% ได้รับ ASA พร้อมกัน (ระหว่าง 1 ถึง 23 มก. / กก. / วัน)ไม่มีความแตกต่างที่มีนัยสำคัญระหว่างกลุ่มสำหรับจุดสิ้นสุดการตายแบบผสมหลัก การเกิดลิ่มเลือดอุดตันในหลอดเลือดแดง หรือการแทรกแซงของหัวใจที่เกี่ยวข้องก่อนอายุ 120 วันหลังเหตุการณ์ที่ถือว่าเป็นภาวะลิ่มเลือดอุดตัน (89 [19.1%) สำหรับกลุ่ม clopidogrel และ 90 [ 20.5%] สำหรับกลุ่มยาหลอก) (ดูหัวข้อ 4.2) เลือดออกเป็นอาการไม่พึงประสงค์ที่รายงานบ่อยที่สุดในกลุ่มที่ได้รับ clopidogrel และ placebo อย่างไรก็ตาม ไม่มีความแตกต่างอย่างมีนัยสำคัญในอัตราการตกเลือดระหว่างกลุ่มต่างๆ ในการติดตามความปลอดภัยในระยะยาวของการศึกษานี้ ผู้ป่วย 26 รายที่ยังต้องเข้ารับการรักษา ที่อายุหนึ่งปีได้รับ clopidogrel จนถึงอายุ 18 เดือน ไม่มีข้อกังวลด้านความปลอดภัยในช่วงระยะเวลาติดตามผลที่ยาวนานนี้
การศึกษาของ CLARINET และ PICOLO ดำเนินการโดยใช้สารละลายที่ประกอบด้วย clopidogrel ในการศึกษาการดูดซึมสัมพัทธ์ในผู้ใหญ่ สารละลายที่ประกอบด้วย clopidogrel แสดงระดับการดูดซึมที่ใกล้เคียงกันและมีอัตราการดูดซึมของเมแทบอไลต์ที่ไหลเวียน (ไม่ได้ใช้งาน) ที่สำคัญกว่ายาเม็ดที่ได้รับใบอนุญาตเล็กน้อย
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
การดูดซึม
หลังจากรับประทานครั้งเดียวและรับประทานซ้ำ 75 มก. / วัน clopidogrel จะถูกดูดซึมอย่างรวดเร็ว ระดับสูงสุดของยาในพลาสมาดังกล่าว (ประมาณ 2.2-2.5 ng / ml หลังจากรับประทานยา 75 มก. เพียงครั้งเดียว) เกิดขึ้นประมาณ 45 นาทีหลังการให้ยา การดูดซึมอย่างน้อย 50% ขึ้นอยู่กับการขับเมแทบอไลต์ของ clopidogrel ในปัสสาวะ
การกระจาย
ในหลอดแก้วหรือ clopidogrel และเมแทบอไลต์หลัก (ที่ไม่ใช้งาน) จะจับกับโปรตีนในพลาสมาของมนุษย์ได้อย่างย้อนกลับ (98% และ 94% ตามลำดับ) พันธะไม่อิ่มตัว ในหลอดทดลอง ในความเข้มข้นที่หลากหลาย
การเปลี่ยนแปลงทางชีวภาพ
Clopidogrel ถูกเผาผลาญอย่างกว้างขวางโดยตับ ในหลอดทดลอง และ ในร่างกาย, clopidogrel ถูกเผาผลาญโดยวิถีการเผาผลาญที่สำคัญสองวิธี: หนึ่ง esterase ไกล่เกลี่ยที่นำไปสู่การไฮโดรไลซิสไปยังอนุพันธ์ของกรดคาร์บอกซิลิกที่ไม่ใช้งาน (85% ของสารที่ไหลเวียน) และอีกวิธีหนึ่งเป็นสื่อกลางโดย P450 ไซโตโครมหลายตัว Clopidogrel ถูกเผาผลาญครั้งแรกไปยังเมตาโบไลต์ระดับกลาง 2- oxo -clopidogrel การเปลี่ยนแปลงที่ตามมาของสารตัวกลาง 2-oxo-clopidogrel นำไปสู่การก่อตัวของสารออกฤทธิ์ซึ่งเป็นอนุพันธ์ของ thiol ของ clopidogrel ในหลอดทดลอง เส้นทางการเผาผลาญนี้อาศัย CYP3A4, CYP2C19, CYP1A2, CYP2B6 สารออกฤทธิ์ของไธออลที่แยกได้ ในหลอดแก้วหรือจับกับตัวรับเกล็ดเลือดอย่างรวดเร็วและไม่สามารถย้อนกลับได้ โดยมีผลยับยั้งการรวมตัวของเกล็ดเลือด
หลังจากได้รับ clopidogrel ขนาด 300 มก. เพียงครั้งเดียว Cmax ของ metabolite ที่ใช้งานอยู่จะสูงเป็นสองเท่าหลังจากให้ยาบำรุง 75 มก. เป็นเวลา 4 วัน Cmax สังเกตได้ประมาณ 30 ถึง 60 นาทีหลังการให้ยา
การกำจัด
ในมนุษย์หลังจากได้รับ clopidogrel ที่ติดฉลาก 14C ในช่องปาก ประมาณ 50% จะถูกขับออกทางปัสสาวะและประมาณ 46% ในอุจจาระภายใน 120 ชั่วโมงหลังให้ยา หลังจากให้ยา 75 มก. ครั้งเดียว clopidogrel จะมีครึ่งชีวิตประมาณ 6 ชั่วโมง ครึ่งชีวิตที่กำจัดของเมตาโบไลต์ที่ไหลเวียน (ไม่ได้ใช้งาน) ที่สำคัญคือแปดชั่วโมงหลังจากให้ยาทั้งแบบเดี่ยวและแบบซ้ำ
เภสัชพันธุศาสตร์
CYP2C19 เกี่ยวข้องกับการก่อตัวของทั้งสารออกฤทธิ์และสารตัวกลาง 2-oxo-clopidogrel เภสัชจลนศาสตร์ของสารออกฤทธิ์ของ clopidogrel และฤทธิ์ต้านเกล็ดเลือด ซึ่งวัดโดยวิธีการรวมตัวของเกล็ดเลือด อดีตร่างกายแตกต่างกันไปตามยีน CYP2C19 อัลลีล CYP2C19 * 1 มีหน้าที่ในการเผาผลาญที่ทำงานได้อย่างสมบูรณ์ในขณะที่อัลลีล CYP2C19 * 2 และ CYP2C19 * 3 ไม่ทำงาน อัลลีล CYP2C19 * 2 และ CYP2C19 * 3 ประกอบขึ้นเป็นอัลลีลที่มีความบกพร่องส่วนใหญ่ในเมตาบอลิซึมที่ไม่ดีของคอเคเซียน (85%) และ ในเอเชีย (99%) อัลลีลอื่น ๆ ที่เกี่ยวข้องกับการเผาผลาญที่ขาดหายไปหรือลดลงนั้นมีความถี่น้อยกว่าและรวมถึง CYP2C19 * 4, * 5, * 6, * 7 และ * 8 เมแทบอลิซึมที่ไม่ดีจะมีอัลลีลที่ไม่ทำงานสองอัลลีลที่เผยแพร่ความถี่สำหรับ CYP2C19 จีโนไทป์ของสารเมแทบอลิซึมที่ไม่ดีนั้นมีอยู่ประมาณ 2% สำหรับชาวผิวขาว 4% สำหรับคนผิวดำ และ 14% สำหรับการทดสอบในจีนมีไว้เพื่อระบุจีโนไทป์ CYP2C19 ของผู้ป่วย
การศึกษาข้ามกลุ่มของอาสาสมัครที่มีสุขภาพดี 40 คน 10 คนสำหรับแต่ละกลุ่มการเผาผลาญ CYP2C19 4 กลุ่ม (รวดเร็วมาก กว้างขวาง ปานกลาง และช้า) ประเมินการตอบสนองทางเภสัชจลนศาสตร์และยาต้านเกล็ดเลือดโดยใช้ clopidogrel 300 มก. ตามด้วย 75 มก. / วันและ 600 มก. ตามด้วย 150 มก. / วัน เป็นระยะเวลา 5 วัน (สภาวะคงตัว) สำหรับแต่ละกลุ่ม ไม่มีความแตกต่างอย่างมีนัยสำคัญในการได้รับสารออกฤทธิ์และการยับยั้งการรวมตัวของเกล็ดเลือด (PAH) ระหว่างสารที่ออกฤทธิ์เร็ว รุนแรง และระดับกลาง ในกลุ่มที่เมแทบอลิซึมไม่ดี การสัมผัสกับสารออกฤทธิ์ลดลง 63% 71% เมื่อเทียบกับสารเมแทบอลิซึมที่กว้างขวาง การตอบสนองของเกล็ดเลือดตามขนาดยา 300 มก. / 75 มก. ของ clopidogrel ลดลงในผู้ที่ได้รับเมตาบอลิซึมที่ไม่ดีโดยมีค่าเฉลี่ย PAH (5 μM ADP) 24% (24 ชั่วโมง) และ 37% (วันที่ 5) เมื่อเทียบกับ " PAH ที่พบในเมแทบอลิซึมที่กว้างขวางโดย 39% (24 ชั่วโมง) และ 58% (วันที่ 5) และที่สังเกตพบในสารเมแทบอลิซึมระดับกลาง 37% (24 ชั่วโมง) และ 60% (วันที่ 5)
เมื่อผู้ที่ได้รับสารเมแทบอลิซึมที่ไม่ดีได้รับขนาดยา 600 มก. / 150 มก. การได้รับสารออกฤทธิ์จะสูงกว่าการได้รับยาในกลุ่ม clopidogrel 300 มก. / 75 มก. นอกจากนี้ PAH มีค่าเท่ากับ 32% (24 ชั่วโมง) และ 61% (วันที่ 5) ซึ่งเป็นค่าที่สูงกว่าที่พบในกลุ่มผู้ที่ได้รับสารเมแทบอลิซึมที่ไม่ดีที่ได้รับการรักษาด้วยขนาดยา 300 มก. / 75 มก. และใกล้เคียงกับกลุ่มอื่นๆ ของเมแทบอลิซึม CYP2C19 ที่ได้รับการรักษาด้วยขนาดยา 300 มก. / 75 มก. ผลลัพธ์จากการศึกษาทางคลินิกไม่ได้กำหนดขนาดยาที่เหมาะสมสำหรับประชากรผู้ป่วยรายนี้
สอดคล้องกับผลลัพธ์ข้างต้น การวิเคราะห์เมตาซึ่งรวมถึงการศึกษา 6 ชิ้นที่มีทั้งหมด 335 คนที่ได้รับการรักษาด้วย clopidogrel ที่สภาวะคงตัว พบว่าการได้รับสารออกฤทธิ์ลดลง 28% สำหรับสารเมแทบอลิซึมระดับกลาง และ 72% สำหรับเมแทบอลิซึมระดับกลาง ในขณะที่การยับยั้งการรวมตัวของเกล็ดเลือด (5 μM ADP) ลดลงโดยมีความแตกต่างใน PAH 5.9% และ 21.4% ตามลำดับเมื่อเทียบกับสารเมแทบอลิซึมที่กว้างขวาง
อิทธิพลของยีน CYP2C19 ต่อผลลัพธ์ทางคลินิกในผู้ป่วยที่ได้รับ clopidogrel ยังไม่ได้รับการประเมินในการทดลองทางคลินิกแบบสุ่มตัวอย่างแบบสุ่มและแบบสุ่มในอนาคต อย่างไรก็ตาม มีการวิเคราะห์ย้อนหลังจำนวนหนึ่งเพื่อประเมินผลกระทบนี้ในผู้ป่วยที่ได้รับ clopidogrel ซึ่งมีผลทางพันธุกรรม : CURE (n = 2721), CHARISMA (n = 2428), CLARITY-TIMI 28 (N = 227), TRITON-TIMI 38 (N = 1477) และ ACTIVE-A (n = 601) และกลุ่มประชากรที่ตีพิมพ์จำนวนหนึ่ง การศึกษา
ในการศึกษา TRITON-TIMI 38 และในการศึกษา 3 กลุ่ม (Collet, Sibbing, Giusti) กลุ่มผู้ป่วยที่มีสารเมแทบอลิซึมระดับกลางและช้ารายงานว่ามีอุบัติการณ์โรคหัวใจและหลอดเลือดสูงขึ้น (ความตาย กล้ามเนื้อหัวใจตายและโรคหลอดเลือดสมอง) หรือหลอดเลือดตีบตัน เปรียบเทียบ ไปจนถึงสารเมแทบอลิซึมที่กว้างขวาง
ในการศึกษา CHARISMA และในการศึกษาตามรุ่น (Simon) พบว่ามีอุบัติการณ์ของเหตุการณ์เพิ่มขึ้นเฉพาะในสารเมแทบอลิซึมที่ไม่ดีเมื่อเทียบกับสารเมแทบอลิซึมที่กว้างขวาง
ในการศึกษา CURE, CLARITY, ACTIVE-A และหนึ่งในการศึกษาตามรุ่น (Trenk) ไม่มีการเพิ่มขึ้นของอุบัติการณ์ของเหตุการณ์ตามสถานะของเมแทบอลิซึม
ไม่มีการวิเคราะห์ใดที่มีขนาดเพียงพอในการตรวจหาความแตกต่างในผลลัพธ์ของสารเมแทบอลิซึมที่ไม่ดี
ประชากรพิเศษ
เภสัชจลนศาสตร์ของสารออกฤทธิ์ของ clopidogrel ไม่เป็นที่รู้จักในกลุ่มประชากรพิเศษเหล่านี้
ไตล้มเหลว
หลังจากได้รับ clopidogrel 75 มก. / วันซ้ำในผู้ที่มีความผิดปกติของไตอย่างรุนแรง (creatinine clearance 5 ถึง 15 มล. / นาที) การยับยั้งการรวมตัวของเกล็ดเลือดที่เกิดจาก ADP ต่ำกว่า (25%) เมื่อเทียบกับที่พบในคนที่มีสุขภาพดี การยืดเวลาเลือดออกคล้ายกับที่พบในคนที่มีสุขภาพดีที่ได้รับ clopidogrel 75 มก. / วัน นอกจากนี้ผู้ป่วยทุกรายยังสามารถทนต่อทางคลินิกได้ดี
ตับไม่เพียงพอ
หลังจากได้รับ clopidogrel 75 มก. / วันซ้ำ ๆ เป็นเวลา 10 วันในผู้ป่วยที่มีความบกพร่องทางตับอย่างรุนแรง การยับยั้งการรวมตัวของเกล็ดเลือดที่เกิดจาก ADP มีความคล้ายคลึงกับที่พบในคนที่มีสุขภาพดี
ค่าเฉลี่ยการยืดเวลาเลือดออกก็ใกล้เคียงกันระหว่างทั้งสองกลุ่ม
แข่ง
ความชุกของอัลลีล CYP2C19 ที่นำไปสู่กิจกรรมการเผาผลาญ CYP2C19 ที่ลดลงและระดับกลางนั้นแตกต่างกันไปตามเชื้อชาติ / ชาติพันธุ์ (ดูเภสัชพันธุศาสตร์) จากวรรณกรรม มีข้อมูลที่จำกัดในกลุ่มประชากรเอเชียเพื่อประเมินความหมายทางคลินิกของการสร้างยีน CYP นี้ต่อเหตุการณ์ทางคลินิก
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ในการศึกษาที่ไม่ใช่ทางคลินิกในหนูและลิงบาบูน การปรับเปลี่ยนค่าพารามิเตอร์ของตับเป็นผลที่สังเกตได้บ่อยที่สุด ซึ่งเกิดขึ้นสำหรับขนาดยาที่สูงกว่าขนาดยา 75 มก. / วันอย่างน้อย 25 เท่า ให้แก่มนุษย์ และเป็นผลที่ตามมาของ ผลกระทบต่อเอนไซม์เมตาบอลิซึมของตับ ไม่พบผลของ clopidogrel ต่อเอนไซม์การเผาผลาญในตับในมนุษย์ในปริมาณที่ใช้ในการรักษา
ในปริมาณที่สูงมาก มีรายงานความสามารถในการทนต่อกระเพาะอาหารได้ไม่ดี (โรคกระเพาะ การกัดเซาะของกระเพาะอาหาร และ/หรือการอาเจียน) ในหนูและลิงบาบูน
ไม่พบผลการก่อมะเร็งหลังการให้ clopidogrel ในหนูทดลองเป็นเวลา 78 สัปดาห์ และในหนูทดลองเป็นเวลา 104 สัปดาห์ จนถึงขนาด 77 มก. / กก. / วัน (คิดเป็นอย่างน้อย 25 เท่าของการได้รับยาในขนาดยาทางคลินิก 75 มก. / วัน ในมนุษย์)
Clopidogrel ประเมินในชุดของการศึกษาความเป็นพิษต่อยีนใน หลอดแก้ว และใน vivหรือไม่แสดงกิจกรรมที่เป็นพิษต่อยีน
Clopidogrel ไม่แสดงผลใดๆ ต่อภาวะเจริญพันธุ์ในหนูเพศผู้และเพศเมีย และไม่แสดงผลการก่อมะเร็งในหนูหรือกระต่าย เมื่อให้นมหนู clopidogrel ทำให้เกิดความล่าช้าเล็กน้อยในการพัฒนาลูกหลาน การศึกษาเภสัชจลนศาสตร์เฉพาะที่ดำเนินการกับ clopidogrel ที่ติดฉลากได้แสดงให้เห็นว่าสารประกอบหลักและสารเมแทบอไลต์ของมันถูกขับออกมาในนม ดังนั้นจึงไม่สามารถยกเว้นผลกระทบโดยตรง (ความเป็นพิษเล็กน้อย) หรือโดยอ้อม (ความสามารถในการรับประทานที่ไม่ดี)
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
นิวเคลียส:
แมนนิทอล (E421);
แมคโครกอล 6000;
เซลลูโลส microcrystalline;
น้ำมันละหุ่งไฮโดรเจน
ไฮดรอกซีโพรพิลเซลลูโลสทดแทนต่ำ
การเคลือบผิว:
ไฮโปรเมลโลส (E464);
แลคโตสโมโนไฮเดรต;
ไตรอะซิติน (E1518);
ไทเทเนียมไดออกไซด์ (E171);
เหล็กออกไซด์แดง (E172)
น้ำยาขัดเงา:
ขี้ผึ้ง carnauba
06.2 ความเข้ากันไม่ได้
ไม่เกี่ยวข้อง
06.3 ระยะเวลาที่ใช้ได้
3 ปี
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
ในตุ่ม PVC / PVDC / อะลูมิเนียม เก็บที่อุณหภูมิต่ำกว่า 30 องศาเซลเซียส
ในตุ่มอลูมิเนียม / อะลูมิเนียม ยานี้ไม่ต้องการสภาวะในการเก็บรักษาพิเศษใด ๆ
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
PVC / PVDC / แผลอลูมิเนียมหรืออลูมิเนียม / แผลอลูมิเนียมในกล่องกระดาษแข็งที่บรรจุเม็ดเคลือบฟิล์ม 7, 14, 28, 30, 84, 90 และ 100
PVC / PVDC / แผลพุพองอลูมิเนียมหรือแผลพุพองขนาดเดียวที่มีรูพรุนอลูมิเนียมในกล่องกระดาษแข็งที่มีเม็ดเคลือบฟิล์ม 50x1
ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
06.6 คำแนะนำในการใช้งานและการจัดการ
ยาที่ไม่ได้ใช้และของเสียที่ได้จากยานี้ต้องกำจัดตามระเบียบข้อบังคับของท้องถิ่น
07.0 ผู้ทรงอำนาจการตลาด
ซาโนฟี่ แคลร์ SNC
54, rue La Boétie
F-75008 ปารีส
ฝรั่งเศส
08.0 หมายเลขอนุญาตการตลาด
EU / 1/98/069 / 001a - กล่องเม็ดเคลือบฟิล์ม 28 เม็ดใน PVC / PVDC / Al ตุ่ม
034128013
EU / 1/98/069 / 001b - กล่องเม็ดเคลือบฟิล์ม 28 เม็ดในกล่องอลูมิเนียม / อะลูมิเนียม
EU / 1/98/069 / 002a - กล่องเม็ดเคลือบฟิล์ม 50x1 ใน PVC / PVDC / Al ตุ่ม
034128025
EU / 1/98/069 / 002b - กล่องยาเม็ดเคลือบฟิล์ม 50x1 ในกล่องอลูมิเนียม / อะลูมิเนียม
EU / 1/98/069 / 003a - กล่อง 84 เม็ดเคลือบฟิล์มใน PVC / PVDC / Al ตุ่ม
034128037
EU / 1/98/069 / 003b - กล่อง 84 เม็ดเคลือบฟิล์มในอลูมิเนียม / อลูมิเนียมพอง
EU / 1/98/069 / 004a - กล่อง 100 เม็ดเคลือบฟิล์มใน PVC / PVDC / Al ตุ่ม
EU / 1/98/069 / 004b - กล่อง 100 เม็ดเคลือบฟิล์มในอลูมิเนียม / อลูมิเนียมพอง
EU / 1/98/069 / 005a - กล่อง 30 เม็ดเคลือบฟิล์มใน PVC / PVDC / Al ตุ่ม
EU / 1/98/069 / 005b - กล่องบรรจุยาเม็ดเคลือบฟิล์ม 30 เม็ดในกล่องอลูมิเนียม / อะลูมิเนียม
EU / 1/98/069 / 006a - กล่อง 90 เม็ดเคลือบฟิล์มใน PVC / PVDC / Al ตุ่ม
EU / 1/98/069 / 006b - กล่อง 90 เม็ดเคลือบฟิล์มในอลูมิเนียม / อลูมิเนียมพอง
EU / 1/98/069 / 007a - กล่องบรรจุยาเม็ดเคลือบฟิล์ม 14 เม็ดใน PVC / PVDC / Al ตุ่ม
EU / 1/98/069 / 007b - กล่องบรรจุยาเม็ดเคลือบฟิล์ม 14 เม็ดในกล่องอลูมิเนียม / อะลูมิเนียม
EU / 1/98/069 / 011a - กล่องบรรจุเม็ดเคลือบฟิล์ม 7 เม็ดใน PVC / PVDC / Al ตุ่ม
EU / 1/98/069 / 011b - กล่องบรรจุเม็ดเคลือบฟิล์ม 7 เม็ดในกล่องอลูมิเนียม / อลูมิเนียมพอง
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
วันที่ได้รับอนุญาตครั้งแรก: 15 กรกฎาคม 1998
วันที่ต่ออายุครั้งล่าสุด: 15 กรกฎาคม 2551
10.0 วันที่แก้ไขข้อความ
D.CCE ตุลาคม 2015